A hidradenite supurativa (HS) é uma doença inflamatória cutânea, crônica, debilitante, potencialmente mutilante.1–3 Longo atraso entre o início da HS e seu diagnóstico é comum,1,4,5 e parece ter impacto na resposta ao tratamento com biológicos.5 Atualmente, o adalimumabe é o único agente biológico aprovado para o tratamento da HS moderada a grave.
Estudo retrospectivo foi conduzido para analisar a subpopulação de pacientes com HS tratados com adalimumabe em centro terciário de Lisboa, Portugal, entre 2016 e 2019. Foram recuperadas informações epidemiológicas, clínicas e terapêuticas. A atividade da HS e a resposta ao adalimumabe foram monitoradas no momento inicial e nas semanas 16 (S16), 24 (S24) e 52 (S52). Exame clínico inicial e um mínimo de 16 semanas de seguimento foram necessários para a inclusão no estudo. Pacientes que necessitaram de aumento das doses de adalimumabe e casos de HS paradoxal foram excluídos. Os pacientes podiam receber tratamentos adjuvantes quando considerados adequados. Utilizaram‐se instrumentos de avaliação de gravidade, especificamente Hurley Staging System, International Hidradenitis Suppurativa Severity Score System (iHS4), Dermatology Life Quality Index (DLQI) e escala visual analógica para dor (EVA dor). A resposta ao tratamento foi avaliada utilizando a escala Hidradenitis Suppurativa Clinical Response (HISCR).
Para a análise estatística, utilizou‐se o software IBM SPSS Versão 24. O teste t de amostras independentes foi usado para testar as diferenças entre variáveis contínuas e categóricas com nível de significância de 0,05. O teste exato de Fischer foi usado para avaliar diferenças entre duas variáveis categóricas, com nível de significância de 0,05, bicaudal.
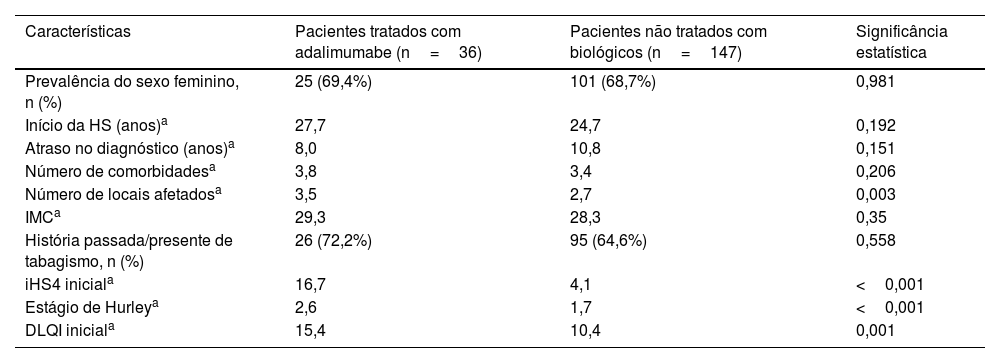
Dos 198 pacientes com HS, 51 iniciaram tratamento com agente biológico e, desses, 36 estavam em uso de adalimumabe e atendiam aos critérios do estudo. A comparação entre esses 36 pacientes tratados com adalimumabe e os 147 pacientes sem tratamento biológico pode ser observada na tabela 1. Ao nível basal, a gravidade era significantemente maior no grupo adalimumabe, usando tanto critérios objetivos (Hurley: 2,6 vs. 1,7; p <0,001; iHS4: 16,7 vs. 4,1; p <0,001) como subjetivos (DLQI: 15,4 vs. 10,4, p=0,002). A maioria dos pacientes em uso de adalimumabe apresentava doença grave (iHS4> 10: 75%; n=27; iHS4 ≤ 10: 25%; n=9), 58,3% (n=21) classificada como estágio Hurley III e 41,7% (n=15) como Hurley II.
Caracterização epidemiológica e clínica dos pacientes com HS tratados ou não com adalimumabe
| Características | Pacientes tratados com adalimumabe (n=36) | Pacientes não tratados com biológicos (n=147) | Significância estatística |
|---|---|---|---|
| Prevalência do sexo feminino, n (%) | 25 (69,4%) | 101 (68,7%) | 0,981 |
| Início da HS (anos)a | 27,7 | 24,7 | 0,192 |
| Atraso no diagnóstico (anos)a | 8,0 | 10,8 | 0,151 |
| Número de comorbidadesa | 3,8 | 3,4 | 0,206 |
| Número de locais afetadosa | 3,5 | 2,7 | 0,003 |
| IMCa | 29,3 | 28,3 | 0,35 |
| História passada/presente de tabagismo, n (%) | 26 (72,2%) | 95 (64,6%) | 0,558 |
| iHS4 iniciala | 16,7 | 4,1 | <0,001 |
| Estágio de Hurleya | 2,6 | 1,7 | <0,001 |
| DLQI iniciala | 15,4 | 10,4 | 0,001 |
IMC, índice de massa corporal; HS, hidradenite supurativa.
Na S16, o HISCR foi alcançado em 27 pacientes (75%). Esse percentual foi similar em pacientes com doença moderada (89%, n=8) e doença grave (70,4%, n=19; p> 0,05). O iHS4 médio foi reduzido de 16,7 para 7,2 (p <0,001). Digno de nota, o tempo desde o início da HS até o diagnóstico foi similar em pacientes que atingiram (6,7 anos vs. 11,8; p=0,282). Na S24, houve redução do iHS4 (média iHS4=6,5; p <0,001). Na S52, a média do iHS4 foi de 4,7 (p <0,001) e HISCR ainda foi alcançado em 76,7% (n=23/30) dos pacientes. Entre o momento inicial e a S52, a DLQI e a EVA da dor passaram de um valor médio de 15,4 para 10,5 (p=0,001) e de 4,4 para 1,8 (p <0,001), respectivamente.
Nas primeiras 16 semanas, para controlar com sucesso a atividade inflamatória da HS, foram empregados tratamentos adjuvantes, transitórios, em 72% dos casos (n=26). Durante o período restante, terapêutica adjuvante foi necessária em 20 pacientes para controlar os episódios de crise.
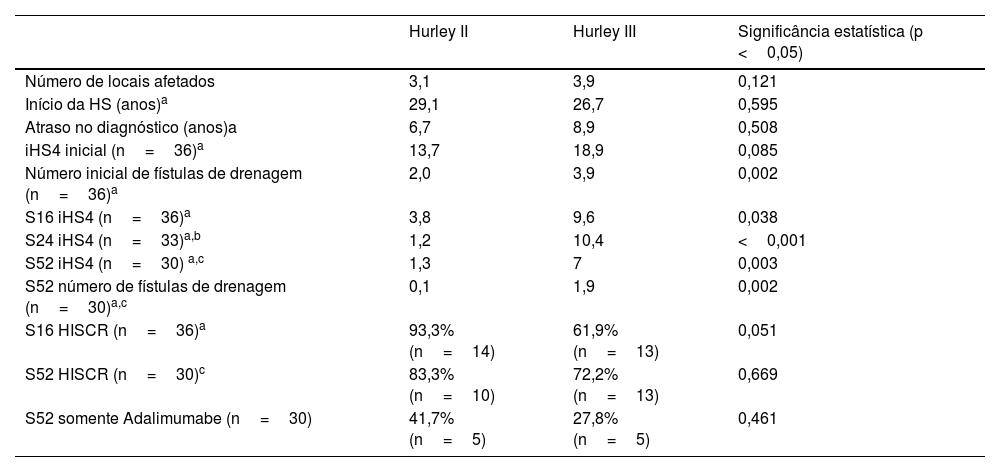
Avaliando as diferenças entre os pacientes estadiados como Hurley II e III (tabela 2), 82% (n=9) dos pacientes do sexo masculino foram classificados como Hurley III, enquanto 48% (n=12) do sexo feminino apresentaram essa gravidade (p=0,044). No momento inicial, os pacientes Hurley II tendiam a apresentar média da gravidade da doença menor (média iHS4: 13,7 vs. 18,8; p=0,085) com número significantemente menor de fístulas de drenagem (2,0 vs. 3,9; p=0,002). Embora ambos os grupos tenham demonstrado melhora da HS com o tratamento, controle significantemente melhor da atividade da doença na S52 foi observado em pacientes Hurley II (iHS4: 1,3 vs. 7; p=0,003). Da mesma maneira, a resposta ao adalimumabe medida pelo HISCR na S16 e S52 foi superior na S16 e similar na S52 em pacientes Hurley II (S16: 93% vs. 61,9%; p=0,051; S52: 83,3% vs. 72,2%; p=0,669).
Caracterização clínica e resposta terapêutica dos grupos com HS Hurley II e Hurley III
| Hurley II | Hurley III | Significância estatística (p <0,05) | |
|---|---|---|---|
| Número de locais afetados | 3,1 | 3,9 | 0,121 |
| Início da HS (anos)a | 29,1 | 26,7 | 0,595 |
| Atraso no diagnóstico (anos)a | 6,7 | 8,9 | 0,508 |
| iHS4 inicial (n=36)a | 13,7 | 18,9 | 0,085 |
| Número inicial de fístulas de drenagem (n=36)a | 2,0 | 3,9 | 0,002 |
| S16 iHS4 (n=36)a | 3,8 | 9,6 | 0,038 |
| S24 iHS4 (n=33)a,b | 1,2 | 10,4 | <0,001 |
| S52 iHS4 (n=30) a,c | 1,3 | 7 | 0,003 |
| S52 número de fístulas de drenagem (n=30)a,c | 0,1 | 1,9 | 0,002 |
| S16 HISCR (n=36)a | 93,3% (n=14) | 61,9% (n=13) | 0,051 |
| S52 HISCR (n=30)c | 83,3% (n=10) | 72,2% (n=13) | 0,669 |
| S52 somente Adalimumabe (n=30) | 41,7% (n=5) | 27,8% (n=5) | 0,461 |
Considerando a última avaliação clínica de todos os pacientes, 78% (n=28) mostraram redução de pelo menos 50% de seu iHS4 no momento inicial (p <0,001). No grupo que não obteve tal resposta (n=8), metade apresentou mais de cinco fístulas de drenagem no momento inicial, e dois pacientes trocaram de tratamento biológico.
Ensaios clínicos mostraram que o adalimumabe é tratamento eficaz para HS moderada a grave em pacientes com resposta inadequada aos tratamentos convencionais,6–8 com taxas de HISCR variando de 40% a 60% em monoterapia.4,6,8,9 Nossos resultados mostraram superioridade em termos de escore alcançado na escala HISCR nas S12/16, S24 e S52 quando comparados aos ensaios clínicos PIONEER I e II e ao estudo multicêntrico de Marzano et al.4,6–8 Os melhores resultados (75% de HISCR na S16) foram associados ao uso de terapêuticas intralesionais e sistêmicas adjuvantes. Acredita‐se que isso pode ser uma medida necessária na prática diária para reduzir ainda mais a inflamação e a dor em casos especialmente graves, auxiliando a ação do adalimumabe. Além disso, como crises ainda podem ser observadas em pacientes recebendo monoterapia com adalimumabe, terapias adjuvantes podem ser necessárias para otimizar o tratamento.
Os resultados deste estudo mostraram resposta maior ao adalimumabe em pacientes Hurley II quando comparados aos pacientes Hurley III, especialmente observável na redução média do escore da iHS4. Além disso, o atraso no diagnóstico de HS foi maior no grupo Hurley III. Esses achados seguem a tendência na hipótese da “janela de oportunidade”, que postulou relação inversa entre a duração da HS e/ou atraso no diagnóstico e a eficácia do adalimumabe.4,9,10 Foi sugerido que iniciar o adalimumabe precocemente, quando a HS é caracterizada por lesões reversíveis, tem o potencial de evitar a progressão da doença, o desenvolvimento de fístulas e deformidades permanentes.4,10 Os pacientes Hurley III apresentam quadro clínico mais grave, o que pode justificar menor eficácia do adalimumabe. Os achados do presente estudo destacam ainda a importância do diagnóstico precoce para o tratamento eficaz, evitando a evolução natural da HS.
Em conclusão, o adalimumabe é tratamento útil e eficaz para a HS, embora acredite‐se que seu uso em monoterapia possa não ser suficiente para o controle ideal em alguns pacientes. O presente estudo apoia a necessidade de um tratamento proativo, ressaltando a importância do encaminhamento precoce, do uso precoce de adalimumabe e do benefício de terapias adjuvantes em pacientes em uso de adalimumabe. Ressalta‐se que as evidências da avaliação na prática diária ainda são escassas, e mais estudos devem ser realizados para propiciar a formulação de diretrizes terapêuticas baseadas em evidências mais adequadas.
Suporte financeiroOs autores não receberam suporte financeiro para a pesquisa, autoria e/ou publicação deste artigo.
Contribuição dos autoresJosé Miguel Neves: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito; elaboração e redação do manuscrito; análise estatística; concepção e planejamento do estudo.
Nélia Cunha: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito; elaboração e redação do manuscrito; análise estatística; concepção e planejamento do estudo.
André Lencastre: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito; elaboração e redação do manuscrito; análise estatística; concepção e planejamento do estudo.
Joana Cabete: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito; elaboração e redação do manuscrito; análise estatística; concepção e planejamento do estudo.
Conflito de interessesOs autores declaram não haver potencial conflito de interesses em relação à pesquisa, autoria e/ou publicação desse artigo.
Como citar este artigo: Neves JM, Cunha N, Lencastre A, Cabete J. Treating hidradenitis suppurativa patients with adalimumab: a real‐life experience of a tertiary care center in Lisboa, Portugal. An Bras Dermatol. 2022;97:816–9.
Trabalho realizado no Departamento de Dermatologia e Venereologia, Hospital de Santo António dos Capuchos, Centro Hospitalar Universitário de Lisboa Central, Lisboa, Portugal.