Hemangioma infantil é o tumor vascular pediátrico mais comum, tem como fatores de risco baixo peso ao nascer, prematuridade, pele branca, sexo feminino, multiparidade e idade materna avançada. O uso de betabloqueadores orais e tópicos, embora recente, tem se apresentado como o tratamento de primeira linha, com segurança e eficácia superiores a terapêuticas anteriormente empregadas, como corticosteroides e cirurgias. Serão descritos dois casos de hemangioma infantil em ponta nasal tratados com propranolol oral, apresentaram ótima resposta terapêutica.
Hemangioma infantil (HI) é o tumor vascular pediátrico mais comum, acomete principalmente cabeça e pescoço, com incidência de 3% a 10%. Sua fisiopatologia ainda não é esclarecida. Os principais fatores de risco são baixo peso ao nascer, prematuridade, pele branca, sexo feminino,1–3 multiparidade e idade materna avançada.1–3
A evolução clínica do HI é dividida em três fases. A fase rápida é caracterizada pela proliferação excessiva logo após o nascimento. Ulcerações, sangramento e obstrução de estruturas vitais também podem ocorrer durante essa fase, especialmente em prematuros. A fase de regressão espontânea − completa ou parcial − envolve maior risco de deformidades e ulceração. A fase de platô (na qual não há regressão ou evolução) surge em aproximadamente 10% dos casos, necessita de intervenção terapêutica, pois há risco de deformação permanente.1–3
Este relato descreve dois casos de HI de ponta nasal tratado com propranolol oral. Ambos mostraram excelentes respostas terapêuticas.
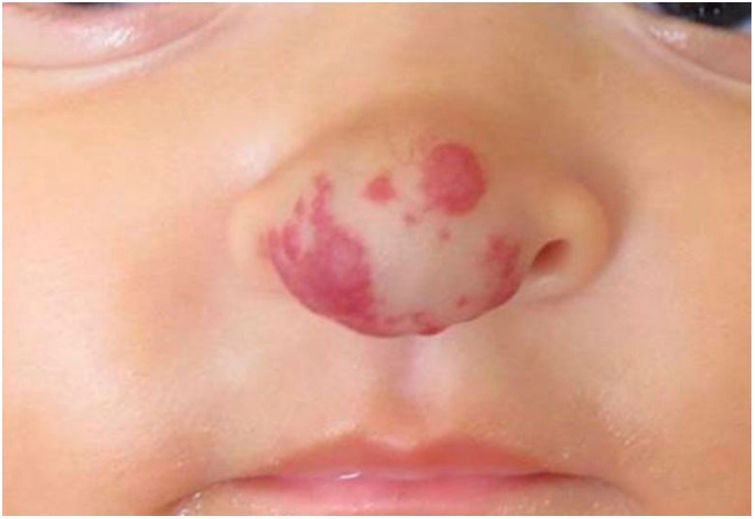
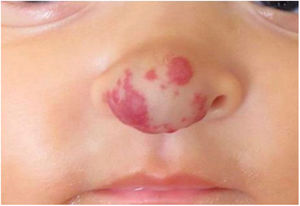
Relatos do casoPaciente de seis meses, sexo feminino, apresentava lesão vascular eritematoviolácea, associada a aumento de volume local, na ponta nasal (fig. 1). A lesão surgiu nos primeiros dias de vida como uma mácula levemente eritematosa e de aumento progressivo. Nascida a termo, adequada para idade gestacional, de genitora multípara (6ª gestação) de 32 anos, sem alterações no período gestacional e no desenvolvimento neuropsicomotor, com cartão de vacinação atualizado.
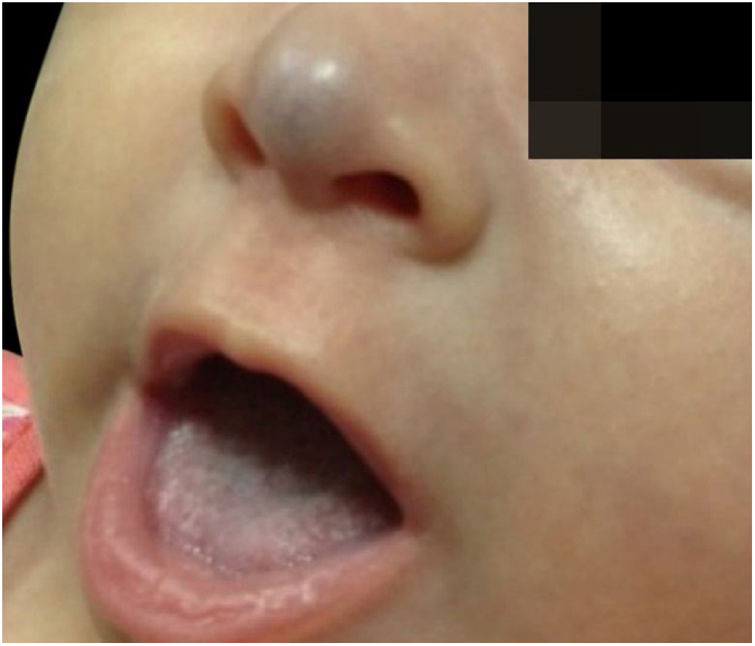
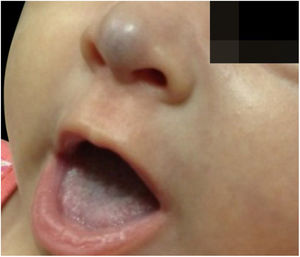
Paciente de dois meses, sexo feminino, apresentava lesão vascular violácea na ponta nasal que ultrapassava os limites anatômicos, surgida nos primeiros dias de vida como mácula discretamente eritematosa, com evolução rápida e progressiva (fig. 2). Nascida pré‐termo (36 semanas), adequada para idade gestacional, de genitora primigesta, de fertilização in vitro, com ameaça de descolamento de placenta e interrupção por oligodrâmnio, sem alterações no desenvolvimento neuropsicomotor, com cartão de vacinação atualizado.
Em ambos os casos, as pacientes foram submetidas à avaliação cardiológica e pulmonar e a exames laboratoriais gerais, que não revelaram alterações. Em relação à terapêutica, a dose alvo de propranolol foi de 2 mg/kg/dia, em duas doses, junto às refeições (primeiras 2 semanas com 0,5 mg/kg/dia com aumento quinzenal progressivo), durante 12 meses. As pacientes foram cuidadosamente monitoradas antes do tratamento e quando houve aumento da dose.
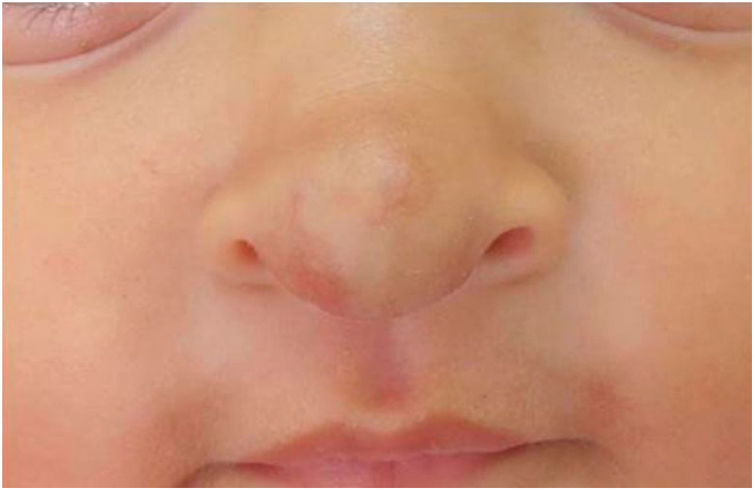
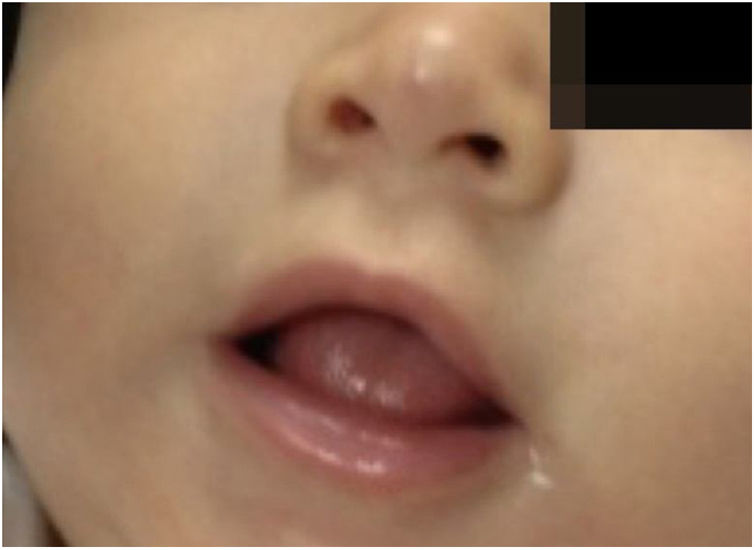
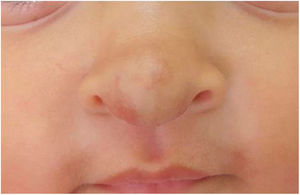
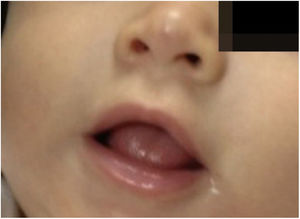
As pacientes não desenvolveram efeito colateral − distúrbios do sono, hipoglicemia ou hipotensão − e obtiveram involução total sem deformidades ou cicatrizes residuais, demonstrou‐se a eficácia do propranolol oral e suas vantagens em relação aos corticosteroides. Os pacientes não apresentaram recidiva nos 3 meses que se seguiram (figs. 3 e 4).
DiscussãoEm vista de possíveis complicações, o tratamento eficaz sem efeitos colaterais é necessário. Há pouco tempo, para HI localizado na ponta nasal, os corticosteroides sistêmicos, a laserterapia e a excisão cirúrgica eram as opções terapêuticas mais comuns para retardar ou interromper o crescimento do tumor vascular e possibilitar sua remoção. Doses elevadas de corticosteroides durante períodos prolongados são frequentemente acompanhadas por diversos efeitos colaterais, principalmente em crianças, como diminuição da formação óssea e aumento da sua absorção, fraqueza proximal e redução da atividade bactericida, o que facilita infecções. Além disso, as consequências podem incluir aumento da gliconeogênese hepática, aumento da resistência à insulina, psicose e alterações do humor. Da mesma forma, a terapia a laser e a remoção cirúrgica podem levar a cicatrizes inestéticas.4–6
Assim, o uso de medicamentos eficazes com menos efeitos colaterais é primordial. Os betabloqueadores, especificamente o propranolol, tornaram‐se a primeira linha de terapia e foram aprovados pela Food and Drug Administration em março de 2014. No entanto seu uso no Brasil ainda não é difundido.6,7
Os beta‐bloqueadores (BBs) são antagonistas beta‐adrenérgicos que geram ações sistêmicas, inclusive redução do débito cardíaco por meio da diminuição da atividade do nó sinoatrial. Isso provoca hipotensão, o que gera vasoconstrição periférica reflexa, que acredita ser responsável pela involução do hemangioma. Além disso, os BBs podem gerar broncoconstrição, aumento da retenção de sódio e volume plasmático secundário à redução da perfusão renal, bem como diminuição da glicogenólise e secreção de glucagon, predispõem à hipoglicemia. Especificamente em relação ao tratamento da IH, os BBs têm sido relacionados a hipoglicemia, pesadelos e hipotensão.3,6,8
Em relação aos riscos envolvidos, é necessário fazer avaliação cardiológica e pulmonar antes do tratamento. Inicialmente, um eletrocardiograma (ECG) deve ser solicitado e a pressão arterial (PA) e a frequência cardíaca (FC) devem ser verificadas, combinadas com exame físico cardiológico e pulmonar detalhado. No início do tratamento (a primeira dose ou após um aumento na dose) devem ser verificadas a cada hora durante 4 horas: temperatura, FC, frequência respiratória e ausculta pulmonar. Muitos autores recomendam que o ECG e a glicemia capilar também sejam feitos antes da administração, e após 120 e 240 minutos, para evitar o risco de hipotensão, broncoespasmo e hipoglicemia.3,8,9
Em comparação com os corticosteroides, os BBs induzem resposta mais rápida, com taxa de resposta em cerca de 90%. Além disso, há menor risco de recidiva e menor necessidade de intervenção cirúrgica.3,8,10 Em nossa experiência, o propranolol resultou em excelente resposta terapêutica e segurança, como exemplificado pelos dois casos supracitados.
Suporte financeiroNenhum.
Contribuição dos autoresMariana Carvalho Costa: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Odil Garrido Campos de Andrade: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; revisão crítica da literatura; revisão crítica do manuscrito.
Lethícia de Castro Pereira: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito; revisão crítica da literatura.
Izelda Maria Carvalho Costa: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Conflitos de interesseNenhum.
Como citar este artigo: Costa MC, Andrade OGC, Pereira LC, Costa IMC. Success in the use of oral propranolol in the treatment of Infantile hemangioma in nasal tip − report of two cases. An Bras Dermatol. 2020;95:207–9.
Trabalho realizado no Hospital Universitário de Brasília, Brasília, DF, Brasil.