A pitiríase rubra pilar (PRP) é dermatose inflamatória eritemato‐papuloescamosa rara.1
Desde a aprovação das vacinas de mRNA para a COVID‐19, a comunidade dermatológica tem se esforçado para caracterizar os efeitos cutâneos adversos associados à sua administração.
Relatamos um caso de PRP após administração da vacina mRNA Pfizer‐BioNTech COVID‐19 com refratariedade à terapia sistêmica de primeira linha, mas que foi tratada com sucesso com ustequinumabe.
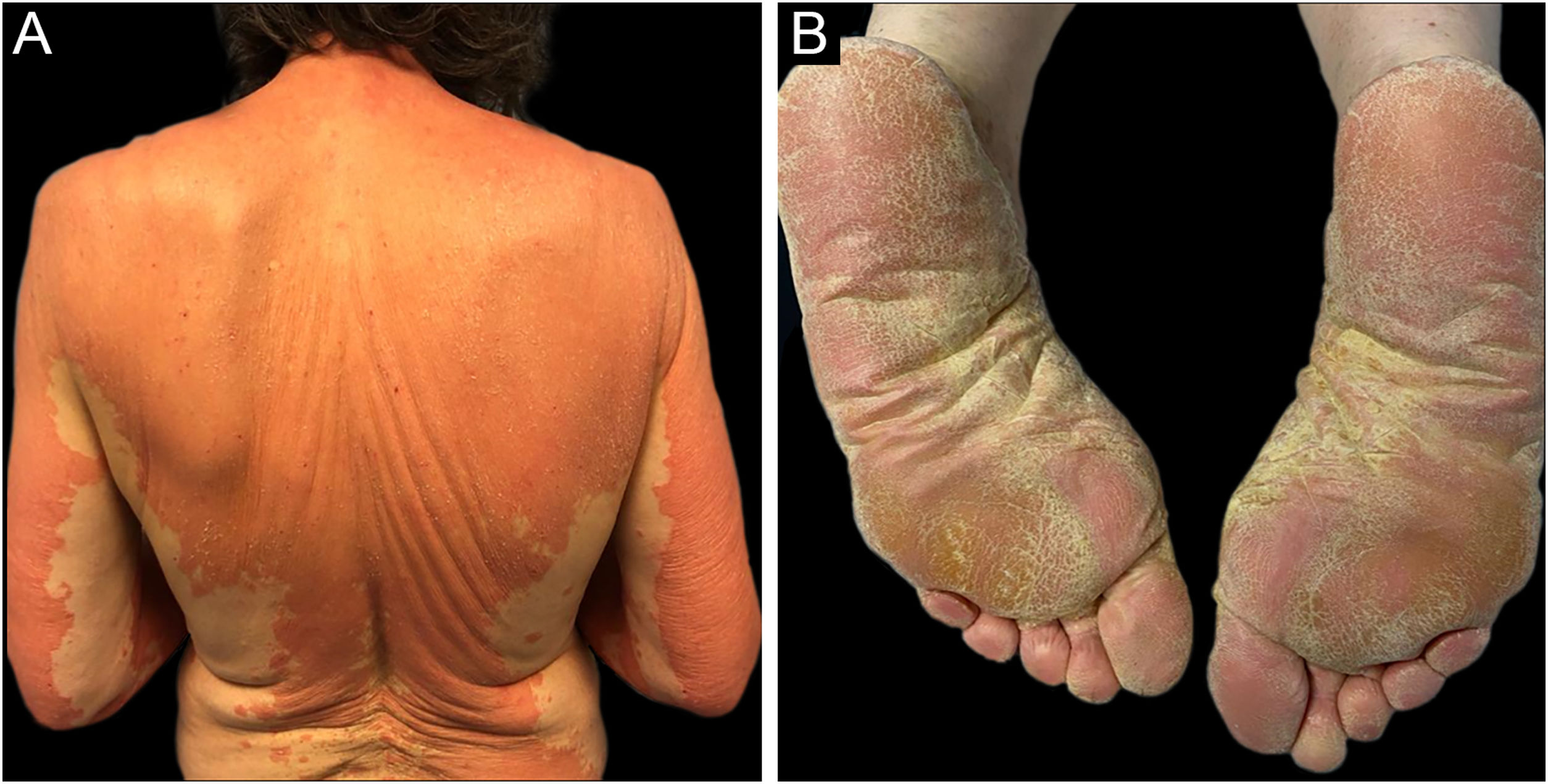
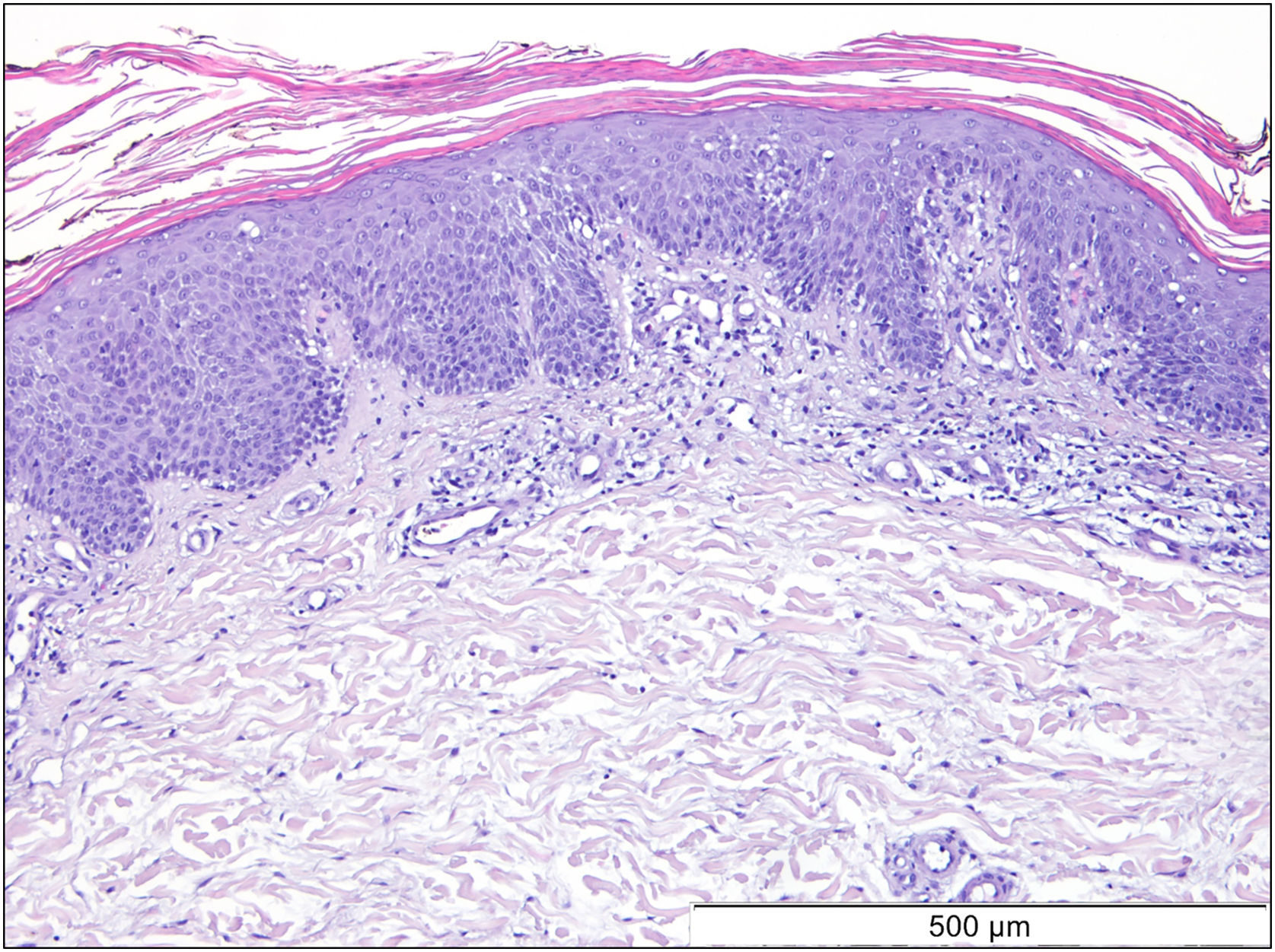
Paciente do sexo feminino, caucasiana, de 69 anos, sem histórico médico relevante, foi encaminhada para atendimento virtude de erupção cutânea generalizada com seis meses de evolução que não melhorou com corticosteroides tópicos e sistêmicos altamente potentes (1 mg/kg/dia) ou ciclosporina oral (4 mg /kg/dia). A paciente relatou erupção cutânea escamosa eritematosa facial dois dias após receber a primeira dose da vacina Pfizer‐BioNTech contra COVID‐19. Poucos dias após a segunda dose da vacina, a paciente notou piora da erupção, com progressão para tronco e membros; relatava prurido intenso e negou antecedentes pessoais ou familiares de doenças de pele ou infecções recentes. Ao exame físico, ela apresentava placas descamativas confluentes de coloração alaranjada/avermelhada bem demarcadas que se estendiam do couro cabeludo até os braços e regiões proximais das coxas com áreas preservadas. Havia placas eritematosas dispersas na parte inferior das pernas e ceratodermia palmoplantar de aspecto céreo e coloração alaranjada/avermelhada (fig. 1). Os exames de sangue mostraram leucopenia (3.150 mm3) com contagem normal de eosinófilos. Os testes sorológicos para vírus e o estudo imunológico estendido foram negativos. A tomografia computadorizada não apresentou nada digno de nota. O exame histopatológico revelou acantose moderada, alguns cones epidérmicos alargados, hiperceratose e paraceratose com pequeno grau de espongiose (fig. 2). Na derme superficial havia pequeno infiltrado celular inflamatório crônico perivascular. O teste genético foi negativo para mutações CARD14.
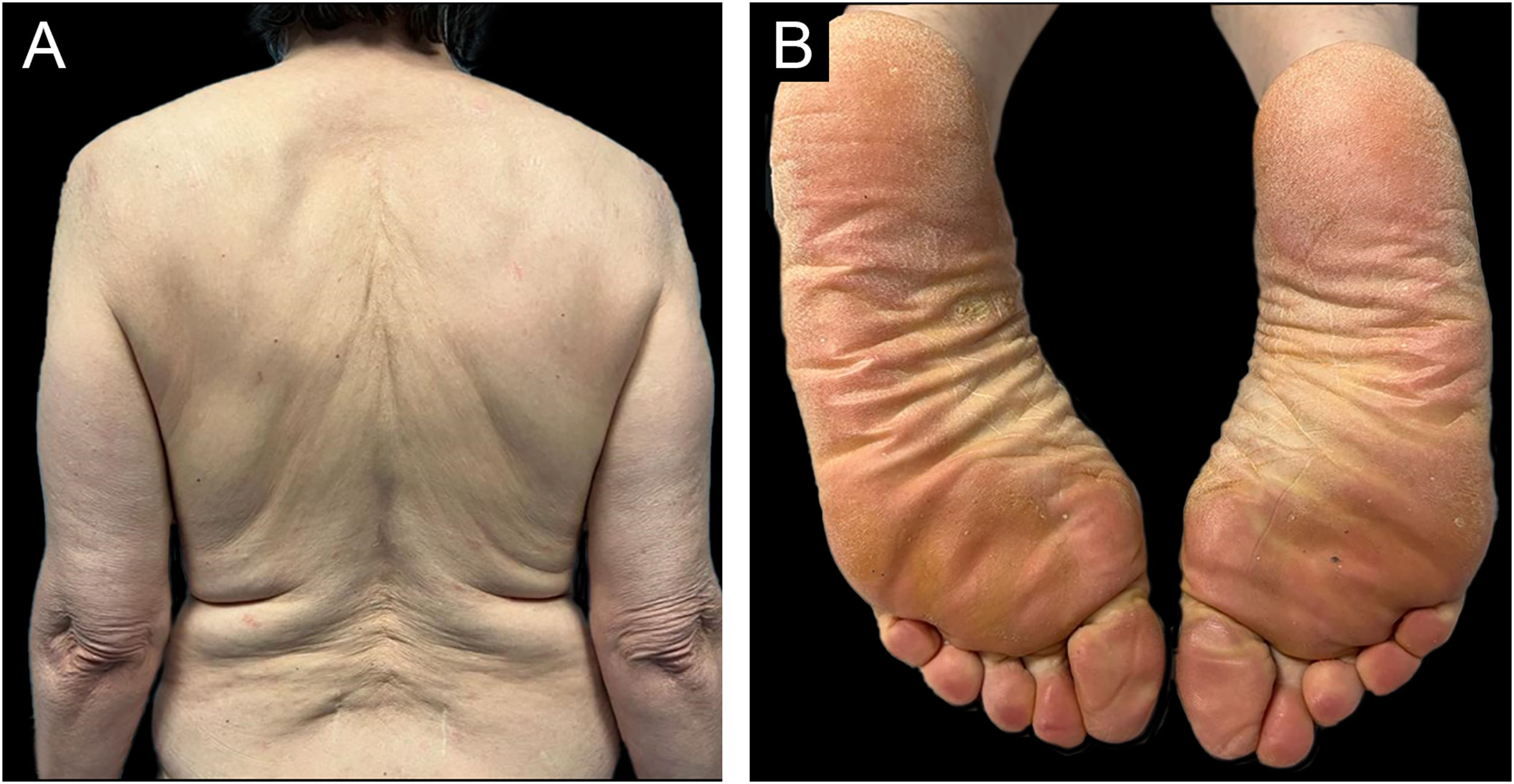
A paciente foi inicialmente tratada com metotrexato (MTX), 12,5 mg, uma vez por semana, durante quatro semanas. No entanto, foi necessário aumentar a dose para 15 mg durante 12 semanas, sem melhora. Terapia com psoraleno e ultravioleta A (PUVA) tópico de mãos e pés foi realizada concomitantemente ao MTX, sem benefício adicional. Posteriormente, foi prescrita acitretina 25 mg em dias alternados, mas a paciente interrompeu 15 semanas depois em decorrência de resposta insatisfatória e de aumento das transaminases (dez vezes acima do limite da normalidade), que normalizou após a retirada do medicamento. Como a paciente apresentou refratariedade às terapias sistêmicas de primeira linha, decidiu‐se iniciar a terapia com ustequinumabe (45 mg na semana 0, semana 4 e depois a cada 12 semanas). Na semana 4 de ustequinumabe foi alcançada resposta quase completa, observando‐se apenas eritema residual da face (fig. 3). A resposta foi mantida durante seis meses de seguimento e nenhuma outra vacina contra COVID‐19 foi administrada.
A etiologia e a patogênese da PRP permanecem obscuras, e a maioria dos casos é esporádica, embora infecções, medicamentos, neoplasias malignas e vacinas sejam todos possíveis desencadeadores.1 Desde a aprovação das vacinas contra SARS‐CoV‐2, foi relatado número crescente de casos de PRP induzidos pela vacina contra COVID‐19.2,3 Uma relação causal é sugerida no presente caso, de acordo com a literatura existente, o fato de a PRP ser condição rara e a estreita relação temporal entre o surgimento da dermatose e a vacinação contra COVID‐19.
O tratamento da PRP é desafiador em virtude da falta de evidências; a referência para o tratamento são os retinoides orais seguidos de metotrexato.1 Na maioria dos casos de PRP induzidos pela vacina contra a COVID‐19, o tratamento foi sistêmico, incluindo retinoides, corticosteroides e metotrexato.2,3 Mais recentemente, para pacientes com falha terapêutica ou contraindicação para terapias convencionais, os imuno‐biológicos surgiram como alternativa promissora.2,4 Inicialmente, esses tratamentos eram em sua maioria empíricos, porém Feldmeyer et al. identificaram níveis mais elevados de expressão de citocinas pró‐inflamatórias inatas e citocinas adaptativas de células T (especialmente as citocinas Th17, IL‐17 e IL‐22) na pele lesionada da PRP, sugerindo o papel da via IL‐23‐Th17 na patogênese da doença.5 De fato, os antagonistas da interleucina 17 (IL‐17), IL‐23 e IL‐12/23 têm sido utilizados com sucesso.2–4,6
A resposta da paciente ao ustequinumabe após falha das terapias convencionais fornece evidências adicionais para o papel da via IL‐23‐Th17 na patogênese da doença e a eficácia dos agentes anti‐IL12/23.
Suporte financeiroNenhum
Contribuição dos autoresBárbara Vieira Granja: Concepção e planejamento do estudo; elaboração e redação do manuscrito ou revisão crítica de conteúdo intelectual importante; revisão crítica da literatura; aprovação da versão final do manuscrito.
Patrícia Amoedo: Concepção e desenho do estudo; elaboração e redação do manuscrito ou revisão crítica de conteúdo intelectual importante; aprovação da versão final do manuscrito.
Nuno Preto Gomes: Elaboração e redação do manuscrito ou revisão crítica de conteúdo intelectual importante; aprovação da versão final do manuscrito.
Catarina Costa: Revisão crítica de conteúdo intelectual importante; aprovação da versão final do manuscrito.
Filomena Azevedo: Participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação da versão final do manuscrito.
Sofia Magina: Participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Vieira‐Granja B, Amoedo P, Gomes NP, Costa C, Azevedo F, Magina S. Pityriasis rubra pilaris after COVID‐19 vaccination: successful treatment with Ustekinumab. An Bras Dermatol. 2024;99:652–4.
Trabalho realizado no Centro Hospitalar Universitário de São João, Porto, Portugal.