Anticorpos monoclonais (mAbs) vêm, desde o final da década de 1990, cada vez mais sendo usados em terapias antitumorais, sendo parte da vertente de tratamentos antineoplásicos denominada terapia‐alvo. Uma vez que apresentam a vantagem de serem direcionados direta e majoritariamente à lesão e a seu microambiente, seu uso reduz o dano a células saudáveis e boa parte dos efeitos adversos das terapias não específicas.1
Ao se ligar à porção extracelular dos receptores do fator de crescimento epitelial (EGFR) e interromper o acoplamento de seus ligantes habituais, os anticorpos monoclonais anti‐EGFR impedem o seguimento das reações em cascata deflagradas por sua ativação. Em tese, a ativação desses receptores que, sabidamente, fazem parte de uma família composta por quatro membros distintos, mas que compartilham elementos estruturais em comum, culmina em proliferação celular, angiogênese, inibição do apoptose e metastatização. Por esse motivo, o bloqueio do EGFR vem sendo usado como terapia‐alvo para uma série de neoplasias que cursam com a superexpressão do EGFR, que é, por si só, considerada critério de pior prognóstico.2,3
A inibição do EGFR afeta, também, a proliferação de células não neoplásicas, em virtude da presença natural desses receptores em queratinócitos, glândulas sebáceas e folículos pilosos. Posto isso, essa modalidade terapêutica apresenta potencial para deflagrar efeitos cutâneos adversos que, embora geralmente sejam bem tolerados e autolimitados, quando graves podem restringir o uso dos medicamentos.4
Entre as reações dermatológicas mais comuns está a erupção acneiforme que surge na região do tronco e da face, sem a presença de comedões. O acometimento ungueal, de cabelos e surgimento de telangiectasias também podem compor o quadro; paroníquia, granuloma piogênico, alopecia, tricomegalia de cílios e hipertricose na face também podem ser vistas. Estudos demonstram que o alongamento e a retificação dos cílios, associados à alteração na textura dos cabelos, podem estar presentes com modificações ultraestruturais e subclínicas. Outro efeito menos comum é o surgimento de nevos melanocíticos e angioedema.5
Efeitos de três fármacos que atuam inibindo o EGFR panitumumabe, erlotinibe e gefitinibe já foram avaliados por meio de microscopia eletrônica de varredura, tendo sido observados canais e torções de fios. Por meio dessas investigações, foram evidenciadas alterações que geraram variantes clínicas ou subclínicas do fenótipo descrito como pili canaliculi, caracterizadas por cabelos crespos ou ondulados.6
O cetuximabe é anticorpo monoclonal inibidor do EGFR e, em combinação com quimioterapia, é aprovado como primeira linha no tratamento de câncer colorretal metastático com expressão do receptor em questão, e até individualmente em pacientes intolerantes à quimioterapia.
Mesmo tendo mecanismos de ação semelhantes aos de fármacos cujos efeitos nos cabelos já foram observados, especula‐se se as diferenças estruturais entre o cetuximabe e elas possam evocar efeitos distintos. Nesse contexto, este trabalho visa a observação, por meio de microscopia eletrônica de varredura, da ultraestrutura tridimensional dos cílios e dos cabelos de paciente em uso da terapia em questão.
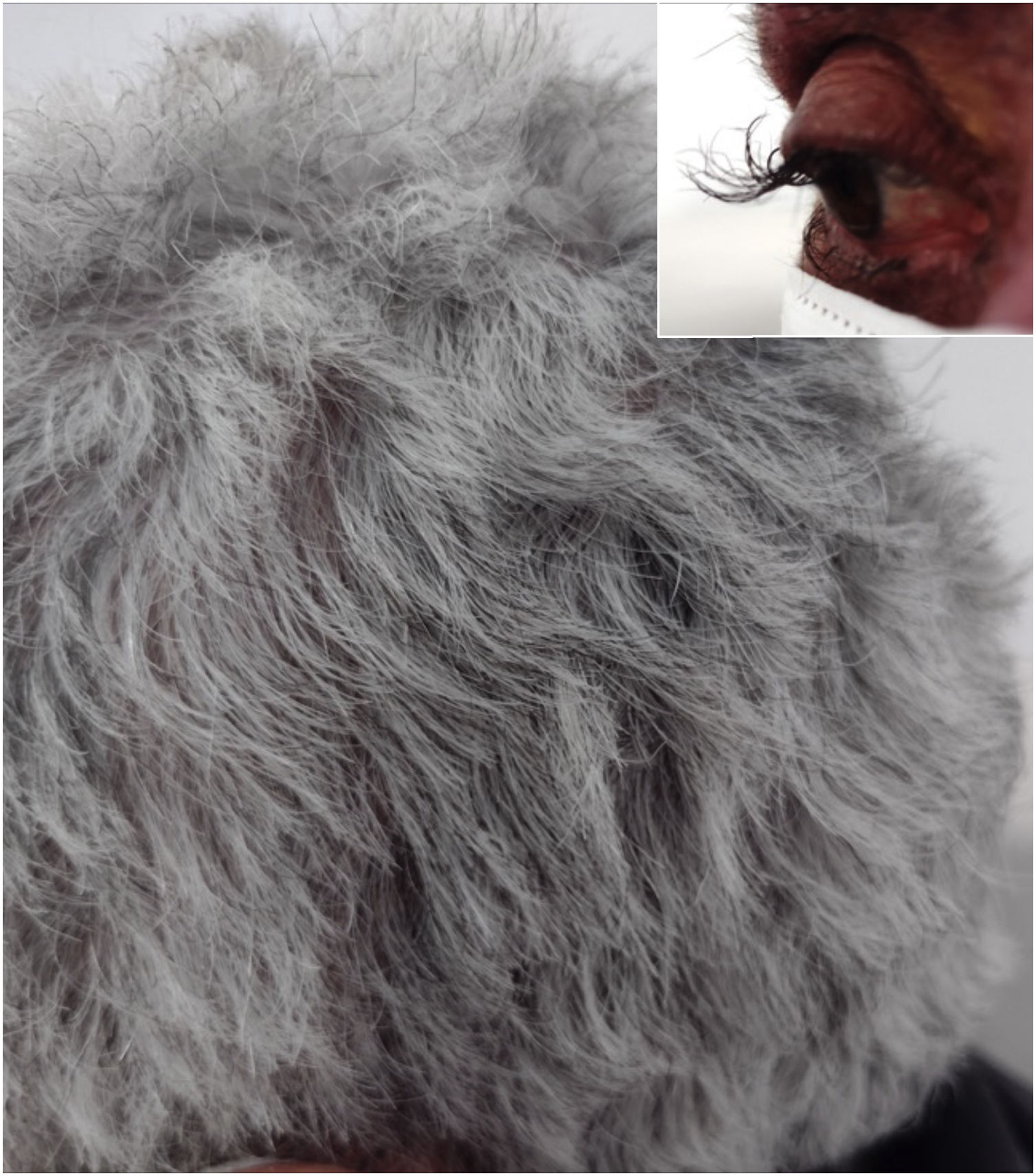
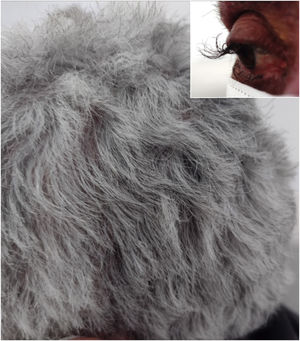
Examinamos paciente do sexo feminino de 64 anos, a qual apresentou carcinoma de cólon com metástases hepáticas, tratada com quimioterapia (protocolo FOLFIRI: fluorouracil+leucovorin+irinotecan) e cetuximabe havia 12 meses. A paciente foi encaminhada para tratar erupção acneiforme do tronco e face, a qual respondeu ao tratamento com tetraciclina oral (500mg, 2×/dia, por 10 dias). A paciente relatou alteração da ondulação do cabelo (fig. 1), o qual ficou crespo após o início da terapia oncológica. os cílios mudaram a curvatura e ficaram alongados (fig. 1).
Foram coletados cabelos e cílios examinados in natura com microscopia eletrônica de varredura.
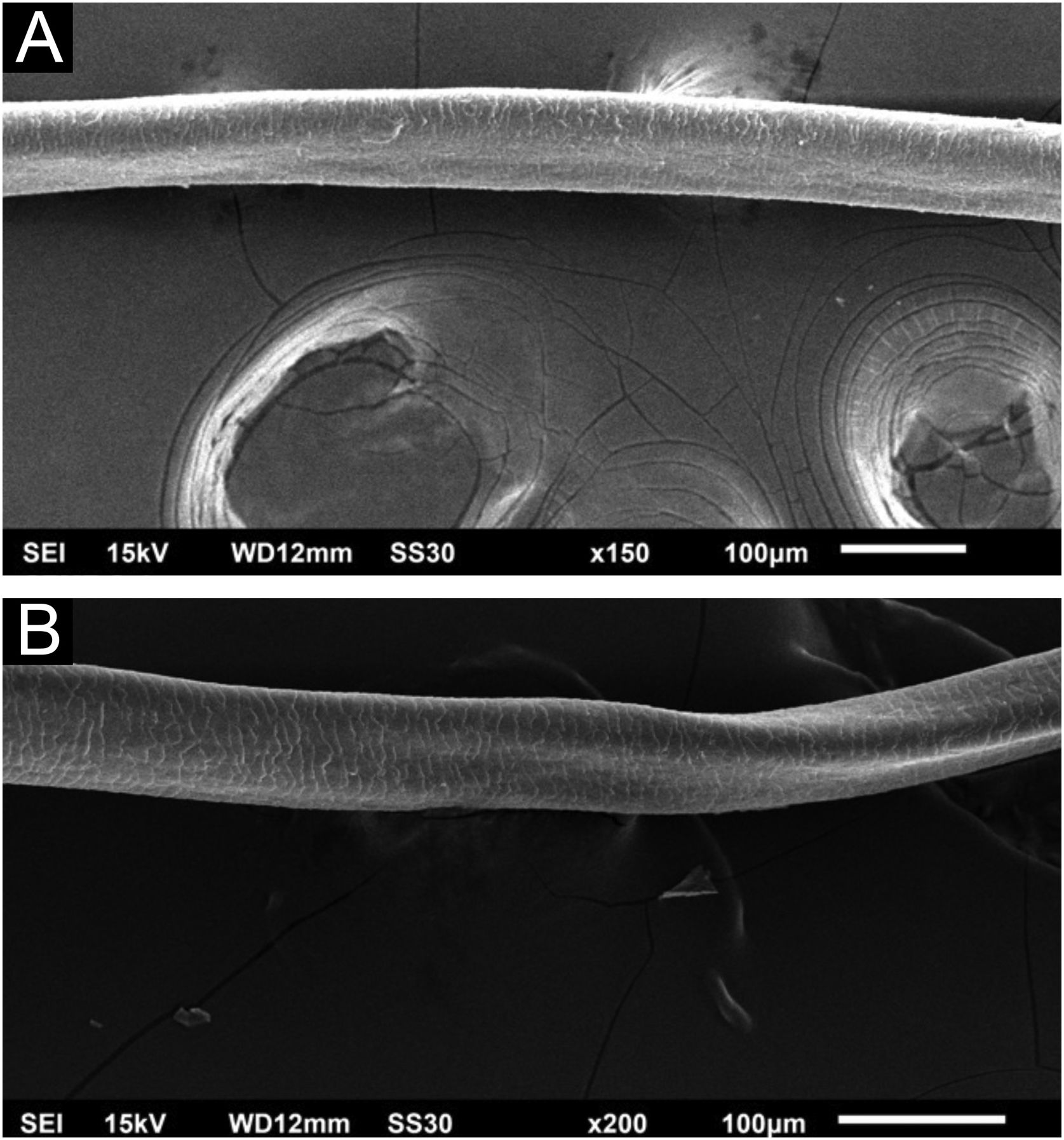
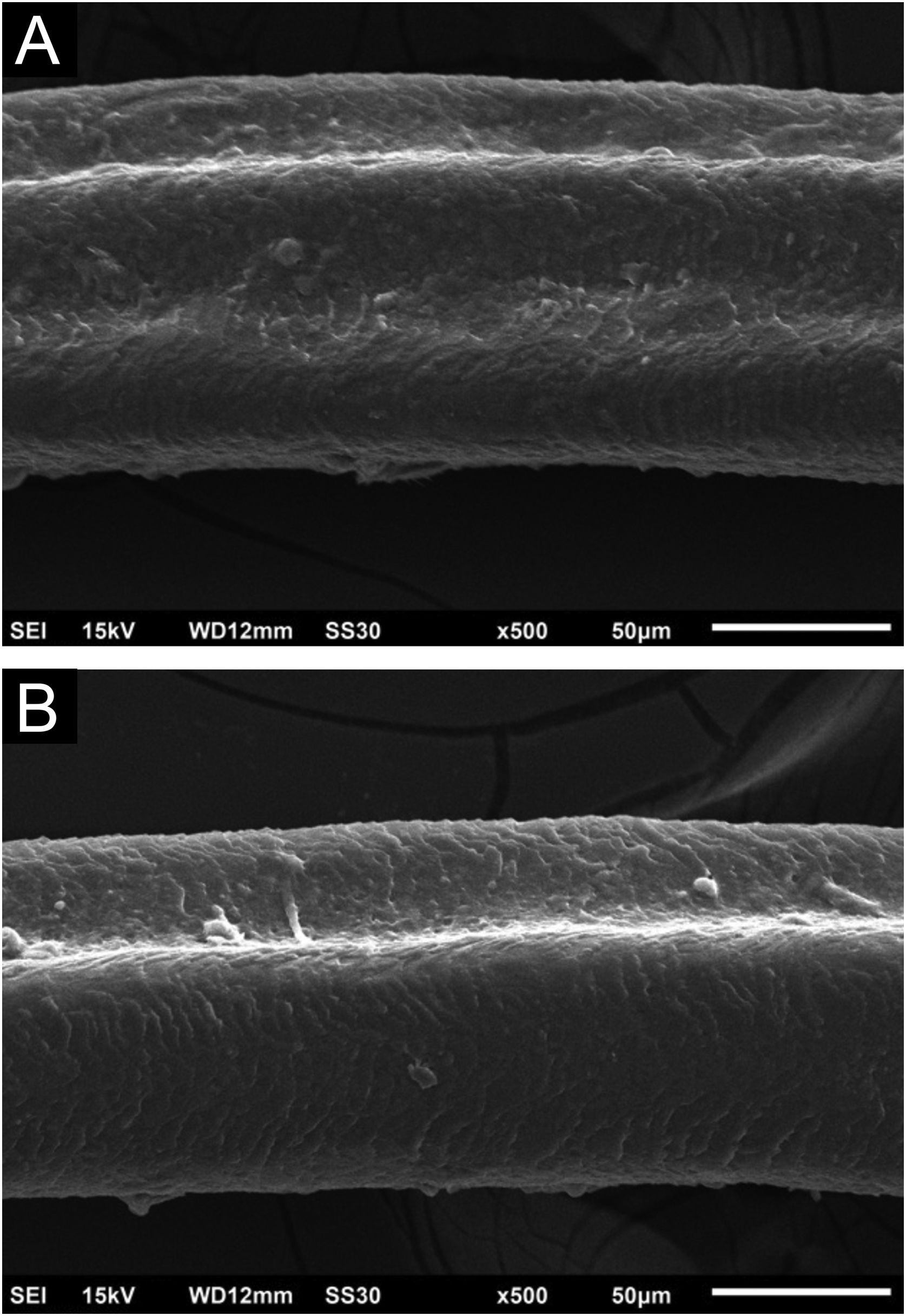
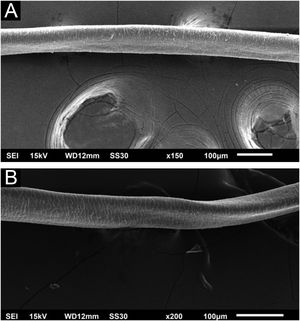
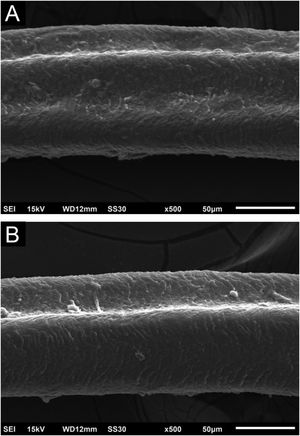
Nos fios de cabelo foram observados, em pequenos aumentos, canais longitudinais nos fios e discretas torções (fig. 2). com grandes aumentos, os canais ficam bem evidentes (fig. 3). O exame de cílios mostra alterações mais pronunciadas, com canais bem desenvolvidos, duplos (fig. 4a) ou únicos (fig. 4b).
Esses achados mostram que a alteração estimulada pelo cetuximabe provoca canais nas hastes, os quais mudam a elasticidade dos fios, alterando sua curvatura ou tornando‐os crespos. Essas alterações são sobreponíveis às provocadas pelo panitumumabe6 e pelos inibidores orais de EGF, e semelhante a formas genéticas de pili canaliculi, que ficam no espectro dos cabelos impenteáveis. As torções encontradas foram discretas, não caracterizando também pili torti, pois teriam que girar 180°.7
Tanto com cetuximabe quanto com panitumumabe,6 os cílios são ultraestruturalmente mais afetados, com canais mais proeminentes. Os autores supõem que possa ser decorrente de sua fase anágena mais lenta ou curta.
As outras medicações utilizadas concomitantemente, seguindo o protocolo de doença metastática de cólon, não devem ser a causa das alterações dos pelos que relatamos, pois são características de inibidores do EGFR.
Suporte financeiroNenhum.
Contribuição dos autoresHiram Larangeira de Almeida Jr.: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Debora Sarzi Sartori: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito;
Felipe Yusuke Sato Shinzato: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Samuel da Silva Julião: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Sílvia Saueressig: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Almeida Jr HL, Sartori DS, Shinzato FYS, Julião SS, Saueressig S. Pili canaliculi caused by cetuximab – A three‐dimensional ultrastructural analysis. An Bras Dermatol. 2024;99:442–5.
Trabalho realizado na Pós‐Graduação em Saúde e Comportamento da Universidade Católica de Pelotas, Pelotas, RS, Brasil.