O metotrexato (MTX) é um tratamento alternativo para pacientes com dermatite atópica (DA) moderada/grave.
ObjetivoAvaliar o efeito do MTX na expressão cutânea de citocinas e quimiocinas envolvidas na resposta inflamatória em indivíduos adultos com DA tratados com metotrexato por 24 semanas.
MétodosFoi realizado um estudo de coorte prospectivo em instituição única com 12 adultos com DA moderada/grave que receberam MTX oral (15mg/semana por 24 semanas) e 10 controles pareados não atópicos. A comparação foi feita em biopsias de pele lesada e não lesada, pré e pós‐tratamento com MTX. Foram analisadas a espessura epidérmica média e a expressão de IL‐31, IL‐31RA, OSMR, TSLP, Ki67, IL‐4 mRNA, IL‐6, IL‐10, TNF‐α, IFN‐γ, TARC e CCL‐22.
ResultadosHouve redução da espessura média da epiderme (p=0,021), aumento da expressão de IL‐31RA (imuno‐histoquímica) na epiderme (p=0,016) e diminuição da expressão gênica de IL‐31 (p=0,019) na pele com lesada da DA pós‐tratamento com MTX. Não foram identificadas alterações significantes na expressão cutânea dos demais marcadores avaliados.
Limitações do estudoPequeno tamanho da amostra e duração limitada do seguimento.
ConclusõesO tratamento com MTX em adultos com DA moderada/grave reduziu a hiperplasia epidérmica e alterou a expressão cutânea de citocinas e receptores inflamatórios relacionados principalmente ao prurido, incluindo IL‐31 e IL‐31RA.
Registro do estudoClinicalTrials.gov Identificador: NCT03327116.
A dermatite atópica (DA) é doença cutânea crônica e pruriginosa com fisiopatologia complexa. Vários fatores estão envolvidos, incluindo defeitos fundamentais da barreira cutânea e disfunção imunológica que resulta em inflamação, bem como lesões eczematosas típicas.1–3
Aumento nas citocinas e quimiocinas Th2 (IL‐4, IL‐10, IL‐13) e Th22 (IL‐22)4,5 é observado na fase aguda da DA. Além disso, ocorre aumento da expressão das citocinas Th1 (IL‐12, IFN‐γ) e Th17 (IL‐17) na fase crônica. Essas observações são vistas principalmente em estudos com foco em crianças6 e na população asiática.7
Outras citocinas foram identificadas na inflamação em DA. Essas incluem TSLP (linfopoietina estromal tímica) e IL‐31. Os queratinócitos epidérmicos expressam TSLP, promovendo assim a ativação de células dendríticas mieloides, bem como células Th2 e Th22. Como resultado, há indução de prurido.8,9 A expressão de IL‐31 promove inflamação mediada por células Th2. Também pode haver aqui uma associação com prurido.10 A sinalização ocorre por meio de um complexo receptor heterodimérico de subunidades do receptor M de oncostatina (OSMR) e do receptor alfa de IL‐31 (IL‐31RA).11
O tratamento da DA deve se concentrar no controle da inflamação e na reparação das alterações da barreira cutânea. Como resultado, o metotrexato (MTX) pode servir como tratamento para pacientes com DA que são refratários à terapia tradicional.2,12,13 Os autores já demonstraram esse achado anteriormente.14
O efeito do MTX foi avaliado na expressão cutânea de citocinas e quimiocinas envolvidas na resposta inflamatória em indivíduos adultos com DA que receberam tratamento com MTX por um total de 24 semanas.
MétodosDesenho do estudo e amostraUm estudo prospectivo em instituição única foi realizado no Departamento de Dermatologia. A população do estudo incluiu 12 adultos (seis do sexo feminino; seis do masculino) com DA moderada a grave (de acordo com os critérios de Hanifin & Rajka). Foi avaliado o uso de MTX em um total de 24 semanas.
Os critérios de elegibilidade incluíram indivíduos com pelo menos 18 anos de idade, com DA moderada/grave com base nos escores de gravidade: EASI (Eczema Area and Severity Index) ≥ 7,1 e SCORAD (SCOring Atopic Dermatitis) ≥ 25. Foi necessário que as mulheres em idade reprodutiva utilizassem métodos anticoncepcionais eficazes e fossem confirmadas como não grávidas através de teste de gravidez no sangue negativo antes do início do tratamento. Os critérios de exclusão incluíram indivíduo com qualquer doença ou condição que contraindicasse o uso de MTX (p. ex., pancitopenia), infecção por HIV ou outra condição imunossupressora, fototerapia, uso de corticosteroide sistêmico, uso de ciclosporina e azatioprina ou terapia imunobiológica nas 12 semanas anteriores ao início do tratamento com MTX, como detalhado em outra publicação.14,15
O escore EASI inicial médio dos pacientes com DA foi de 28,9±9,9 e o SCORAD inicial médio foi de 57,2±7,8.14 A dose de MTX inicial (dose de teste oral) foi de 7,5mg na semana 1, aumentada para 15mg semanalmente. O ácido fólico oral foi administrado uma vez por semana (5mg) 48 a 72 horas após a administração do MTX. Durante o tratamento, os indivíduos continuaram com as medicações tópicas padrão de tratamento da DA, incluindo corticosteroides tópicos, valerato de betametasona 0,1% creme, acetato de hidrocortisona 1,0% creme, inibidores de calcineurina e emolientes.
Os indivíduos foram biopsiados em dois locais diferentes (pele lesada e pele sem lesão clínica). Para a biopsia da pele lesada, foi selecionada uma região corporal não fotoexposta, principalmente na região lombar. A investigação foi realizada no pré‐tratamento e após 24 semanas de uso de MTX. Amostras de pele de 10 controles não atópicos, pareados por sexo e idade, realizadas em local anatômico semelhante de pacientes com DA, foram utilizadas para padronizar as análises.
Todos os indivíduos leram o termo de consentimento livre e informado e concordaram em participar do estudo. O estudo foi aprovado pelo Comitê de Ética local (CAPPESq 13368); Identificador ClinicalTrial.gov NCT03327116.
Espessura epidérmica média e imunohistoquímicaAmostras de pele de 4mm foram obtidas e incluídas em parafina para avaliação por imuno‐histoquímica. DAB (3,3’ diamibenzidina, D5637, Sigma, St. Louis, MO, EUA) foi utilizado como solução cromógena, como descrito anteriormente.15,16 Após a imunomarcação, as lâminas foram escaneadas usando Pannoramic Scan – 3Dhitech slide scanner (3DHistech Ltd., Budapeste, Hungria).
As fotos foram avaliadas para marcações imuno‐histoquímicas e espessura média da epiderme usando o programa Image‐Pro Plus, versão 4.5.0.29 (Media Cybernetics Inc., Bethesda, Maryland, EUA).17
A espessura média da epiderme foi calculada traçando‐se duas linhas: uma na parte superior da epiderme e outra na parte inferior da epiderme, seguindo a membrana basal. A distância média entre essas duas linhas foi obtida com a função da distância média do programa Image‐Pro‐Plus. Essa função mede a distância ponto‐a‐ponto entre as duas linhas; a cada variação de ângulo, gera um valor médio e calcula a espessura média da epiderme.
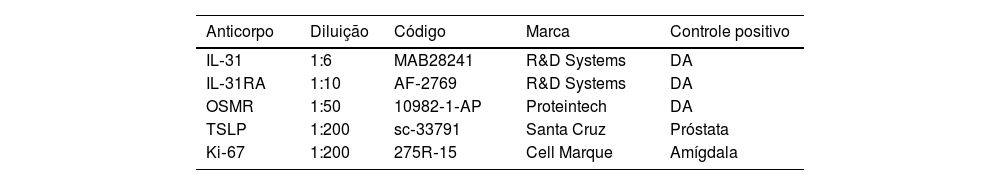
Os anticorpos primários IL‐31, IL‐31RA, OSMR, TSLP e Ki‐67 estão listados na tabela 1.
Anticorpos utilizados para a análise imuno‐histoquímica
| Anticorpo | Diluição | Código | Marca | Controle positivo |
|---|---|---|---|---|
| IL‐31 | 1:6 | MAB28241 | R&D Systems | DA |
| IL‐31RA | 1:10 | AF‐2769 | R&D Systems | DA |
| OSMR | 1:50 | 10982‐1‐AP | Proteintech | DA |
| TSLP | 1:200 | sc‐33791 | Santa Cruz | Próstata |
| Ki‐67 | 1:200 | 275R‐15 | Cell Marque | Amígdala |
DA, dermatite atópica.
A expressão do mRNA por PCR em tempo real foi realizada utilizando amostras de pele que foram armazenadas em solução RNAlater (Sigma, Steinheim, Alemanha) e congeladas a−80°C. O RNA total foi extraído utilizando um kit RNAeasy Plus Mini (Qiagen, Valencia, CA, EUA). O cDNA foi sintetizado utilizando o ISCRIPT cDNA KIT (Bio‐rad, Hercules, CA, EUA).
A síntese dos primers sense e antisense para IL‐4, IL‐6, IL‐10, IL‐31, IL‐31RA, TNF‐α, IFN‐γ, TARC, CCL‐22 e controles internos GAPDH (gliceraldeído‐3‐fosfato desidrogenase) foi realizada por Invitrogen (Carlsbad, CA, EUA).15
A amplificação por PCR foi conduzida em um sistema Applied Biosystems 7500 usando os primers e reagentes de detecção por fluorescência SYBR Green (Applied Biosystems, Carlsbad, CA, EUA). O protocolo de ciclagem consistiu em 10 minutos a 95°C, seguidos de 40 ciclos de 15 segundos a 95°C e 60 segundos a 60°C.
O software Sequence Detection System (SDS; Applied Biosystems) foi usado para analisar os resultados que foram normalizados.18
Análise estatísticaA comparação entre amostras relacionadas (mesmo indivíduo, pré‐tratamento vs. pós‐tratamento) foi realizada utilizando o teste não paramétrico de Wilcoxon. Para amostras não relacionadas, foi utilizado o teste de Mann‐Whitney. Um valor alfa de 0,05 foi utilizado em todas as amostras.
ResultadosEspessura média da epidermeA espessura média da epiderme na pele lesada de indivíduos com DA antes do tratamento foi de 127,6±194,3μm. A espessura média da epiderme na pele lesada em indivíduos com DA após o tratamento com MTX foi de 100,3±80,7μm. A espessura média da epiderme foi significantemente menor na pele lesada pós‐tratamento (diferença média=31,3μm, IC 95%: 15,0–92,7; p=0,021).
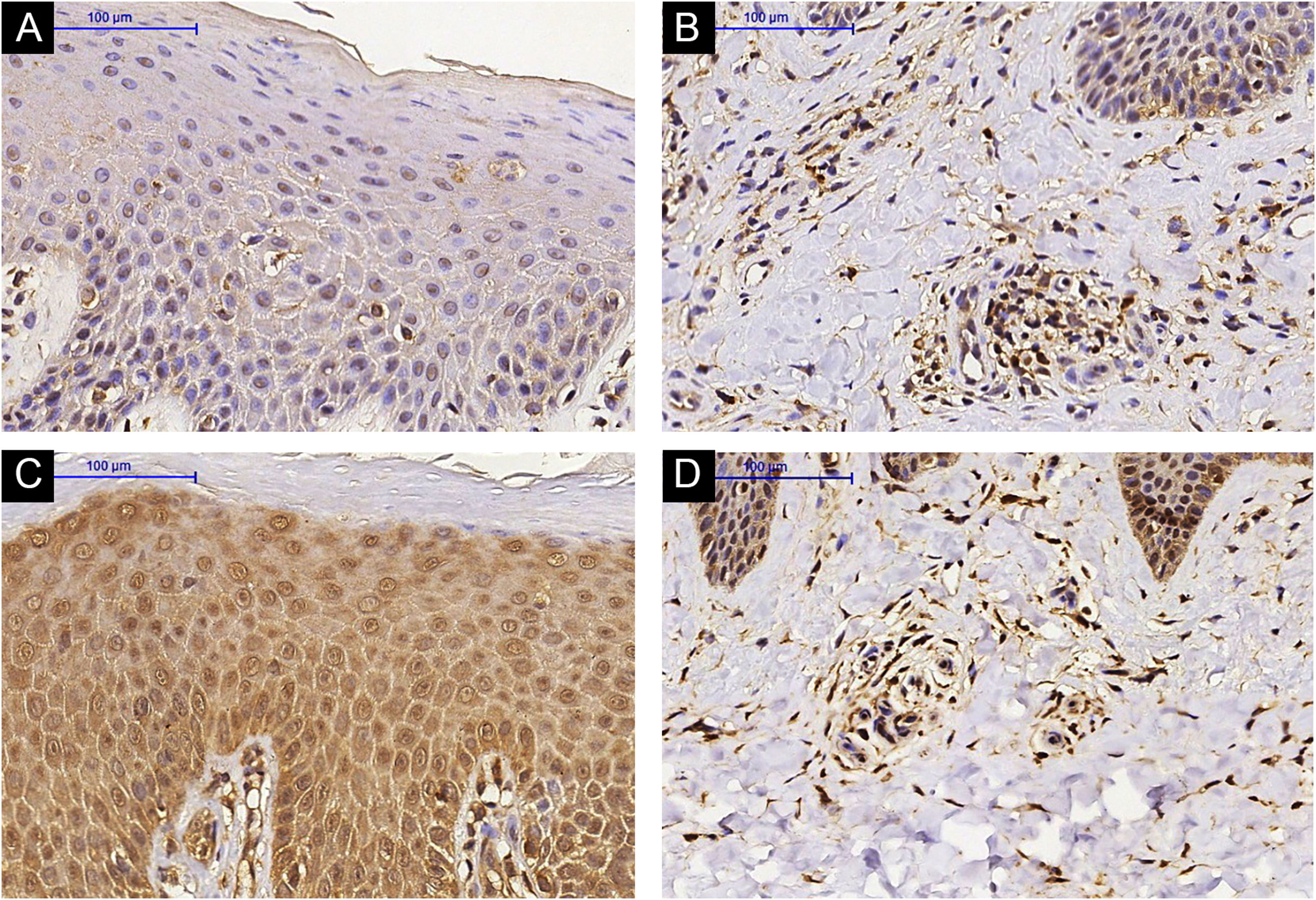
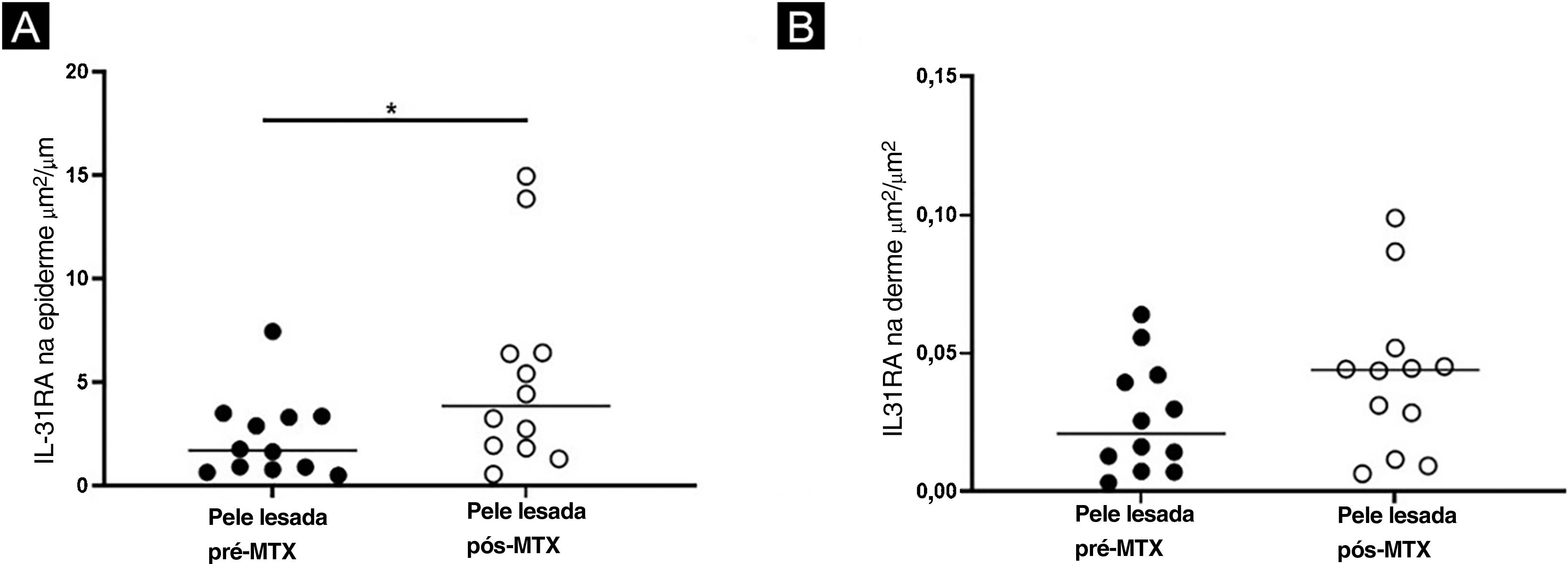
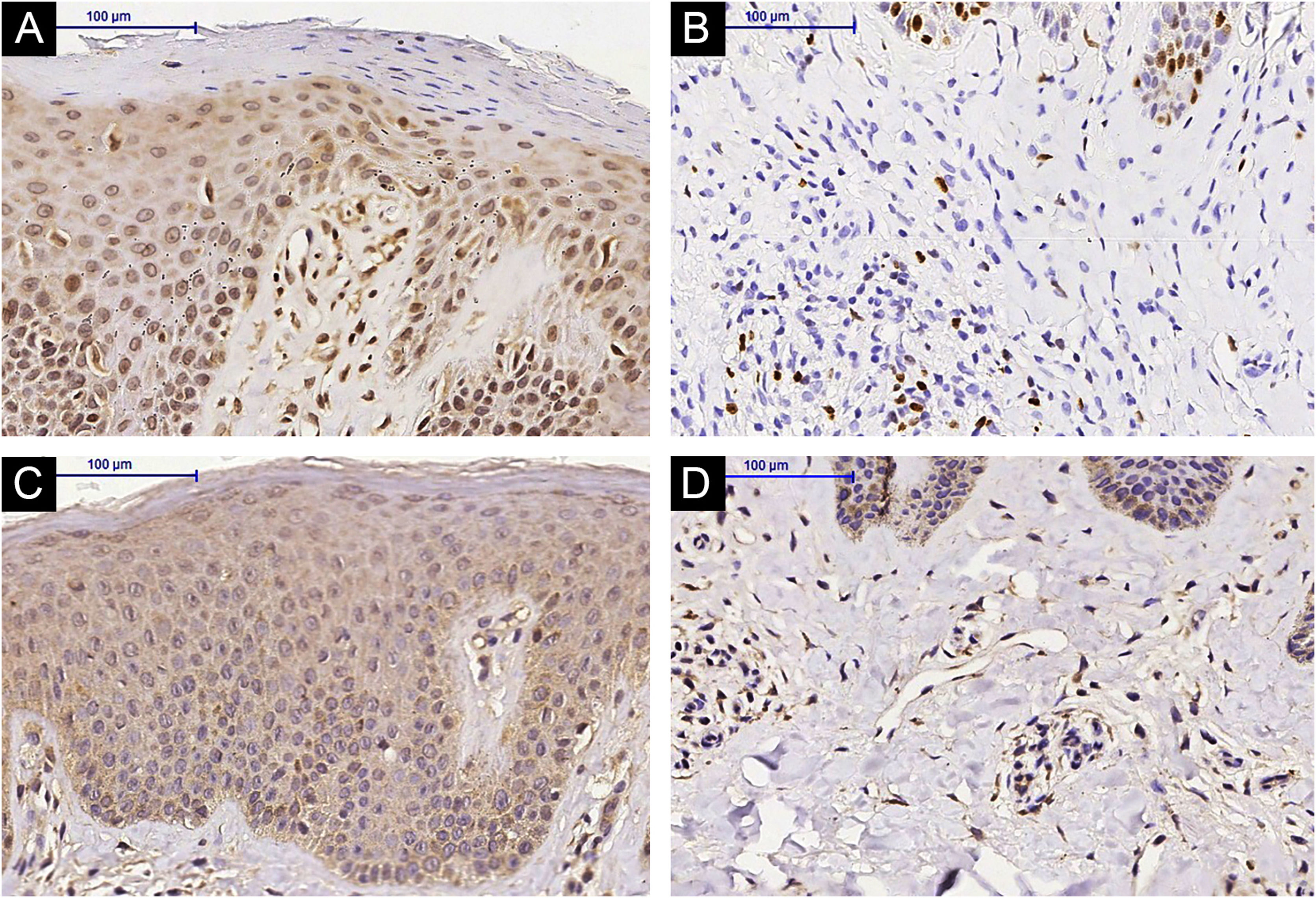
Imuno‐histoquímicaHouve aumento da expressão de IL‐31RA na epiderme (p=0,016) de indivíduos com DA pós‐tratamento com MTX e não foi observada nenhuma diferença significante na derme superficial (p=0,151) – figuras 1 e 2. A expressão cutânea dos outros marcadores não revelou alterações significantes (figs. 3 e 4: IL‐31; OSMR, TSLP e Ki‐67).
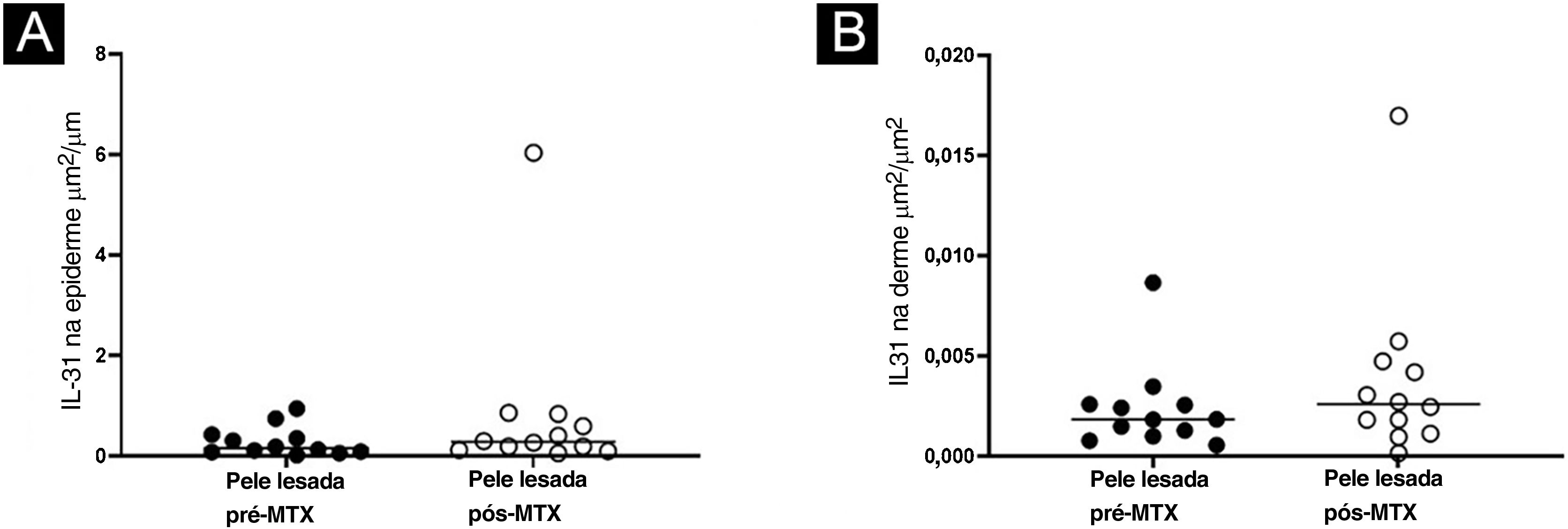
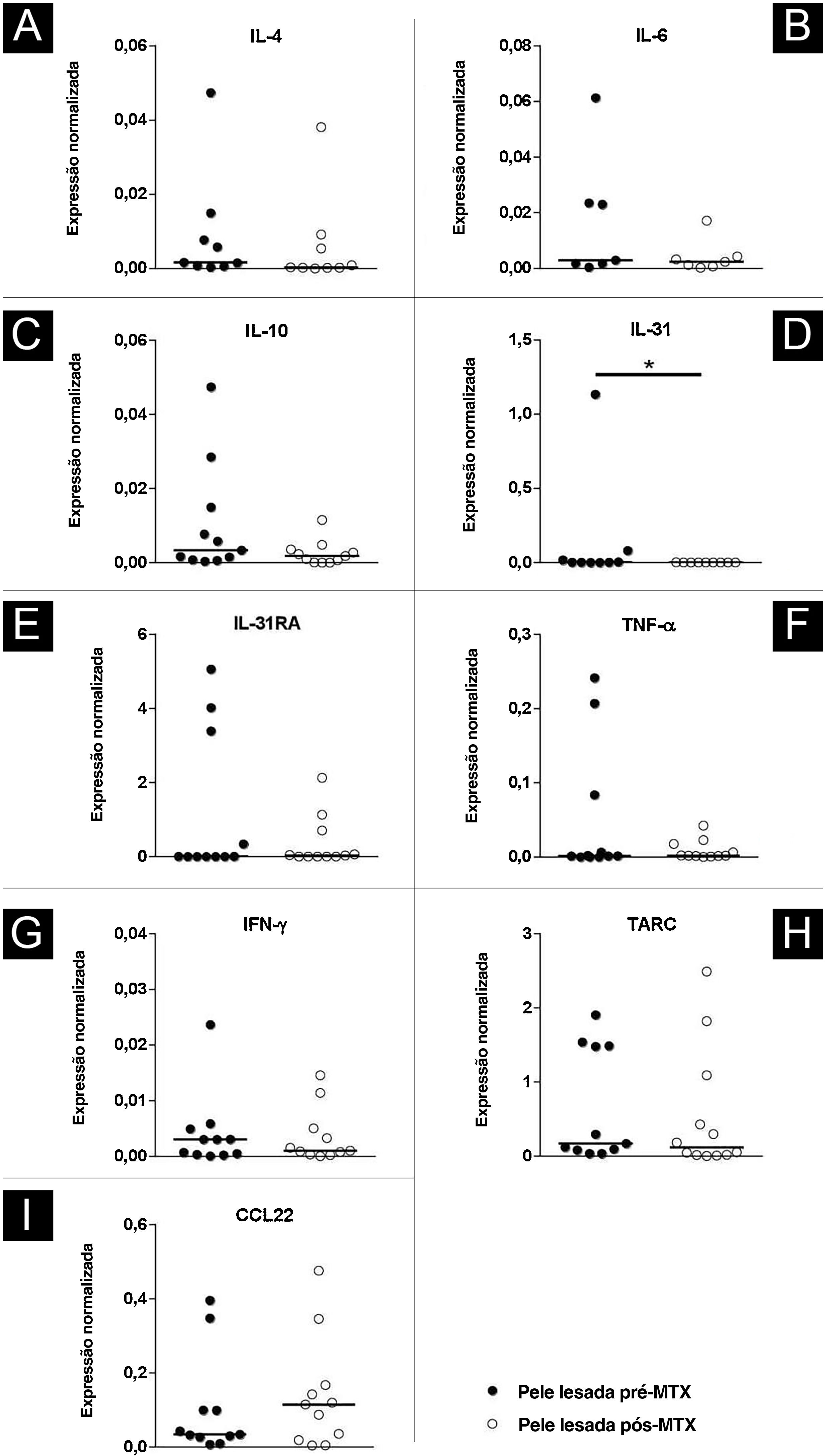
Houve diminuição na expressão gênica de IL‐31 (p=0,019) na pele lesada de indivíduos com DA 24 semanas após a terapia com MTX. A expressão cutânea dos demais marcadores avaliados (IL‐4, IL‐6, IL‐10, IL‐31RA, TNF‐α, IFN‐γ, TARC e CCL‐22) não apresentou resultados significantes (fig. 5).
Perfil da expressão de IL‐4 (A), IL‐6 (B), IL‐10 (C), IL‐31(D), IL‐31RA (E), TNF‐α (F), IFN‐γ (G), TARC (H) e CCL‐22 (I) comparando a pele lesada de indivíduo com dermatite atópica (DA) pré‐tratamento com metotrexato (MTX) e pós‐tratamento com MTX utilizando PCR em tempo real. Houve diminuição estatisticamente significante na expressão de IL‐31 na pele lesada após o tratamento. A expressão normalizada foi calculada conforme descrito anteriormente.18 As linhas representam as medianas das citocinas nas amostras de pele (*p <0,05).
A DA é doença cutânea crônica pruriginosa comumente observada em crianças; entretanto, pode persistir ou ocorrer na idade adulta. A qualidade de vida é significantemente afetada.19,20 O tratamento de primeira linha inclui corticosteroides tópicos e uso de emolientes. Em casos moderados a graves refratários ao tratamento convencional, medicamentos de segunda linha, como o MTX, podem ser utilizados.12,13
Há poucos estudos avaliando o efeito do MTX nos mediadores inflamatórios cutâneos envolvidos em pacientes com DA. Schram et al. randomizaram adultos com DA para receber MTX ou azatioprina por 12 semanas e encontraram redução nos níveis séricos de TARC (quimiocina do timo regulada por ativação) em ambos os grupos.21 Roekevisch et al. estudaram os efeitos de MTX e azatioprina em pacientes adultos com DA e observaram redução significante em TARC, CTACK (quimiocina cutânea para atração de células T ou quimiocina [C‐C motif] ligante 27 – CCL27), IL‐13 e fator de crescimento do endotélio vascular (VEGF).22
Anteriormente, os autores demonstraram a eficácia do MTX na DA moderada/grave, encontrando redução nos escores de prurido e gravidade dos sintomas.14 Aqui, os autores mostram que alterações cutâneas podem ser detectadas em indivíduos com DA que estão recebendo MTX. Também identificaram redução da espessura média da epiderme da pele com lesões de DA, aumento da expressão de IL‐31RA por imuno‐histoquímica e diminuição da expressão gênica de IL‐31 por RT‐PCR.
A redução na espessura média da epiderme da pele lesada na DA não foi demonstrada anteriormente e pode estar associada à melhora dos sinais e sintomas (prurido) observada em pacientes com DA.14 Resultados semelhantes foram relatados com outras modalidades de tratamento, incluindo fototerapia tópica (PUVA), laser excímero, crisaborol tópico e dupilumabe.23–26
A redução do prurido observada após o tratamento com MTX pode ser influenciada, em parte, pela redução da expressão gênica da IL‐31. A IL‐31 está envolvida na polarização imunológica para o perfil Th2 na fase aguda da DA, bem como no prurido de pacientes com DA.10,27,28 A sinalização ocorre por meio de um receptor heterodimérico. A subunidade IL‐31RA parece desempenhar papel mais importante na patogênese da DA do que a subunidade OSMR.11,29,30
A identificação do aumento da expressão de IL‐31RA na epiderme, evidenciada pela imuno‐histoquímica, sugere mecanismo compensatório da IL‐31RA, dada a redução da expressão gênica de IL‐31. A regulação positiva de IL‐31RA pode ocorrer após alguns estímulos: Mike et al. demonstraram regulação positiva de IL‐31RA após estimulação de IL‐4 em células dendríticas derivadas da medula óssea de murinos.31 Além disso, Edukulla et al. observaram que em camundongos IL‐4 e IL‐13 poderiam aumentar a expressão de IL‐31RA em macrófagos da medula óssea e peritoneal.32
As limitações potenciais do presente estudo incluem o pequeno tamanho da amostra e duração limitada do seguimento. É possível que um estudo em larga escala com seguimento mais longo permitisse rastrear alterações na expressão cutânea de marcadores inflamatórios na DA em pacientes em uso de MTX. Novas terapias direcionadas em andamento e medicina de precisão podem melhorar o tratamento da DA,13 aliviando o curso crônico e o estigma dessa doença recalcitrante e pruriginosa. Uma vez que o acesso a essas terapias direcionadas ainda é limitado, justifica‐se a identificação do impacto imunológico das terapias disponíveis, como o MTX, para a DA.
ConclusãoO MTX administrado a indivíduos com DA moderada/grave reduziu a hiperplasia epidérmica e alterou a expressão de citocinas e receptores inflamatórios relacionados ao prurido, incluindo IL‐31 e IL‐31RA.
Suporte financeiroEste estudo foi financiado pelo Fundo de Apoio à Dermatologia de São Paulo (23–2015).
Contribuições dos autoresLuciana Paula Samorano: Revisão crítica da literatura; obtenção, análise e interpretação de dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; elaboração e redação do manuscrito; análise estatística; concepção e planejamento do estudo.
Kelly Cristina Gomes Manfrere: Obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa.
Naiura Vieira Pereira: Obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa.
Roberto Takaoka: Obtenção, análise e interpretação de dados; participação efetiva na orientação da pesquisa.
Neusa Yuriko Sakai Valente: Obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa.
Mirian Nacagami Sotto: Obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa.
Luiz Fernando Ferraz Silva: Participação intelectual em conduta propedêutica e/ou terapêutica dos casos estudados; concepção e planeamento do estudo; participação efetiva na orientação da pesquisa.
Maria Notomi Sato: Obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa.
Valeria Aoki: Aprovação da versão final do manuscrito; revisão crítica da literatura; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica dos casos estudados; revisão crítica do manuscrito; concepção e planejamento do estudo.
Conflito de interessesNenhum.
Como citar este artigo: Samorano LP, Manfrere KCG, Pereira NV, Takaoka R, Valente NYS, Sotto MN, et al. Methotrexate for refractory adult atopic dermatitis leads to alterations in cutaneous IL‐31 and IL‐31RA expression. An Bras Dermatol. 2024;99:72–9.
Trabalho realizado na Faculdade de Medicina, Universidade de São Paulo, São Paulo, SP, Brasil.