O nevo sebáceo de Jadassohn é definido como malformação congênita rara caracterizada como hamartoma não hereditário das estruturas anexiais da pele. Sua etiologia ainda não foi bem compreendida, mas acredita‐se que esteja relacionada com mutações pós‐zigóticas nos genes HRAS, NRAS e KRAS.
ObjetivoDescrever a manifestação clínica do nevo sebáceo, bem como as principais técnicas de manejo abordadas na literatura médica. Ademais, o presente estudo discorre acerca de um relato de caso de nevo linear congênito na região retroauricular esquerda em paciente do sexo masculino, sem manifestações extracutâneas.
MetodologiaRealizou‐se revisão narrativa da literatura.
DiscussãoO nevo sebáceo manifesta‐se sob a forma de lesões de aspecto linear ou oval, com textura lisa ou verrucosa, geralmente alopécicas e de coloração bastante variável. Outrossim, o nevo sebáceo é um dos componentes da chamada síndrome do nevo linear ou síndrome de Schimmelpenning‐Feuerstein‐Mims, a qual está associada a complicações multissistêmicas. O tratamento das lesões ainda é controverso; contudo, a maioria dos especialistas aponta a excisão cirúrgica como o método de tratamento mais adotado, além de um acompanhamento multidisciplinar quando estabelecido o diagnóstico de síndrome de Schimmelpenning‐Feuerstein‐Mims.
ConclusãoA síndrome do nevo linear é manifestação rara; todavia, seu diagnóstico deve ser considerado em crianças nascidas com nevo sebáceo. Ainda não há consenso sobre a melhor terapêutica, mas a remoção cirúrgica demonstra ser uma opção viável.
O nevo sebáceo, também conhecido como nevo organoide, nevo de Jadassohn ou nevo pilosiringossebáceo, é caracterizado como hamartoma congênito raro, não hereditário, resultante da hiperplasia de elementos epiteliais, sebáceos, foliculares e apócrinos da pele.1–4 A etiologia dessa doença ainda não foi completamente esclarecida e, assim, carece de maiores investigações; contudo, estudos recentes sugerem a associação de mutação somática pós‐zigótica relacionada aos genes HRAS (cromossomo 11p15), NRAS (cromossomo 1p13) e KRAS (cromossomo 12p12)5,6 na gênese dessa afecção, por condicionarem o processo de proliferação celular.6,7 A manifestação clínica ocorre na forma de placas com alopécia parcial ou total, de formato linear ou oval, com coloração variando de tonalidade cor da pele, laranja‐amarelada ou como máculas preto‐acastanhadas, de aspecto liso, mamilonado ou verrucoso, a depender do grau de desenvolvimento da lesão.3,8,9 As regiões geralmente acometidas são o couro cabeludo, seguido por área pré‐auricular, face e região cervical. No entanto, diversos estudos relatam sua ocorrência em outras áreas menos frequentes, como mucosas, tronco e extremidades, de modo que, quando encontradas nesses locais, as lesões se distribuem seguindo a orientação das linhas de Blaschko.2,3,10 O nevo sebáceo pode estar relacionado com manifestações extracutâneas com o acometimento de diferentes órgãos e, nesse caso, constitui‐se um quadro clínico mais complexo, recebendo a denominação de síndrome do nevo linear ou síndrome de Schimmelpenning‐Feuerstein‐Mims.3,6
ObjetivoO presente estudo reporta os principais aspectos do nevo sebáceo e da síndrome do nevo sebáceo de Jadassohn, delineando suas características, manifestações clínicas e enfatizando as alternativas terapêuticas.
MetodologiaTrata‐se de estudo do tipo revisão bibliográfica, com enfoque narrativo. Realizou‐se pesquisa na plataforma PubMed, em maio de 2021, restringindo os resultados aos últimos cinco anos (2016‐2021), com as seguintes expressões em língua inglesa: “Nevus sebaceous”, “sebaceous nevus”, “syndrome Schimmelpenning” e “sebaceous nevus Jadassohn”.
Foram empregados como critério de inclusão os artigos estritamente relacionados ao tema. A triagem dos trabalhos pautou‐se nos títulos e/ou resumos, na disponibilidade do artigo integral e na publicação nos idiomas inglês, português, espanhol e francês. Retiraram‐se aqueles que não preencheram as especificações previamente deliberadas. Foram encontrados 128 artigos e, desses, 64 foram selecionados e 64 excluídos. Dos 64 artigos selecionados, após leitura e análise crítica, escolheram‐se 24 para a redação deste estudo. Posteriormente, com o objetivo de ampliar a perspectiva da pesquisa, foram incluídas as obras de Happle,11 Basu et al.,12 McCalmont1 e Kang et al.13
HistóricoEm 1895, o dermatologista alemão Josef Jadassohn realizou a descrição do nevo organoide, subclassificação do nevo epidérmico, como malformação congênita envolvendo estruturas anexiais, principalmente as glândulas sebáceas.3,14–16 Posteriormente, em 1957, Gustav Schimmelpenning realizou a avaliação de uma paciente portadora de lesões de pele e com manifestações de comprometimento neurológico decorrentes de malformação craniana e, e, virtude da não correspondência deste com nenhum outro quadro clínico anteriormente descrito, Schimmelpenning o categorizou como uma facomatose neurocutânea.5,11 Em 1962, Feuerstein e Mims relacionaram um caso de nevo linear com sintomas de convulsão e retardo mental.5 Desde então, criou‐se a chamada tríade clássica utilizada para diagnóstico, composta por comprometimento neurológico, convulsão e retardo mental associados à presença de nevo sebáceo.11 Entretanto, estudos subsequentes evidenciaram que as manifestações extracutâneas da síndrome de Schimmelpenning‐Feuerstein‐Mims são bem mais variadas.3
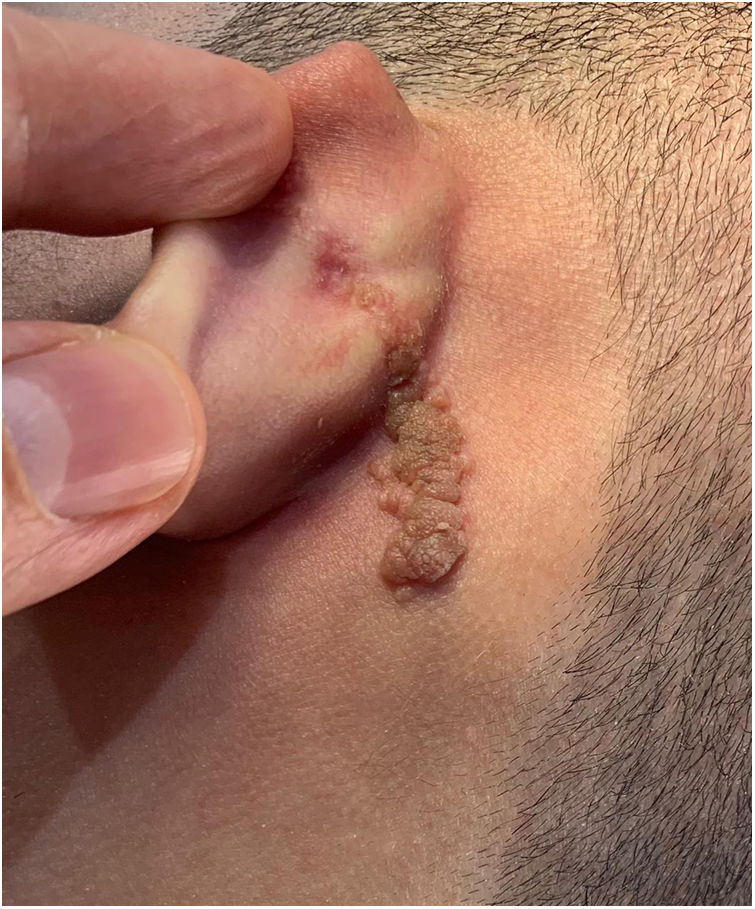
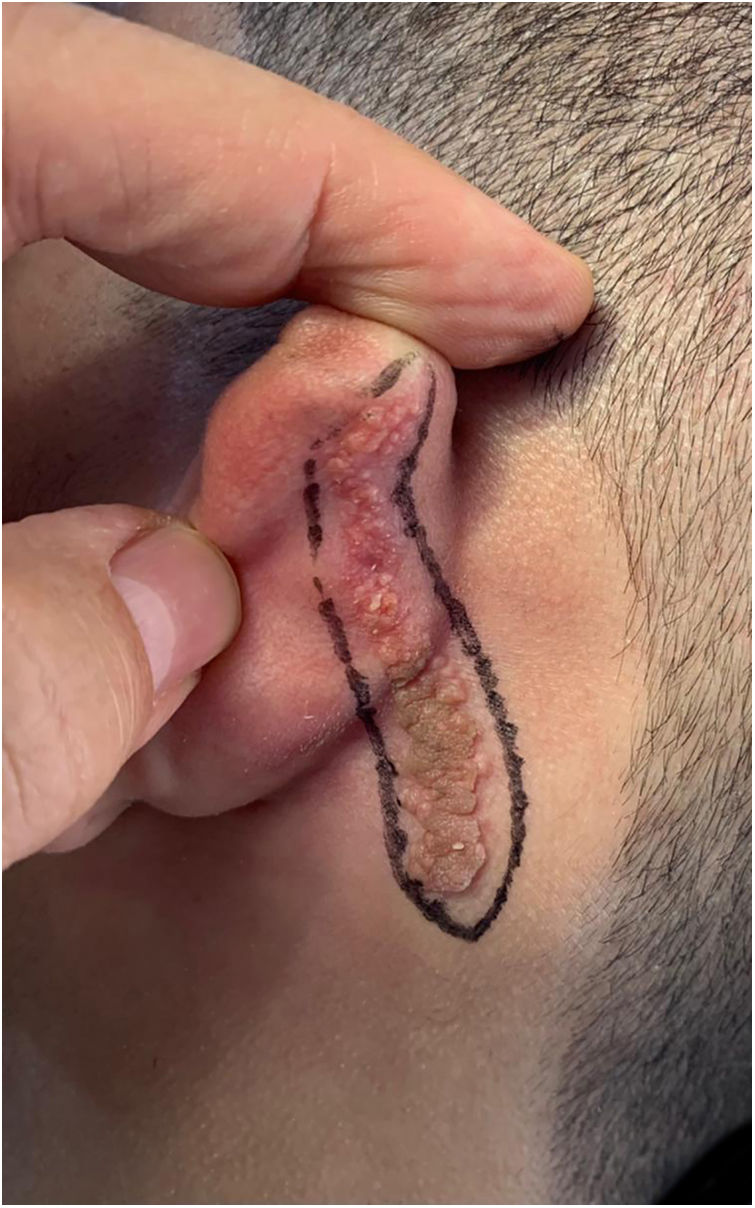
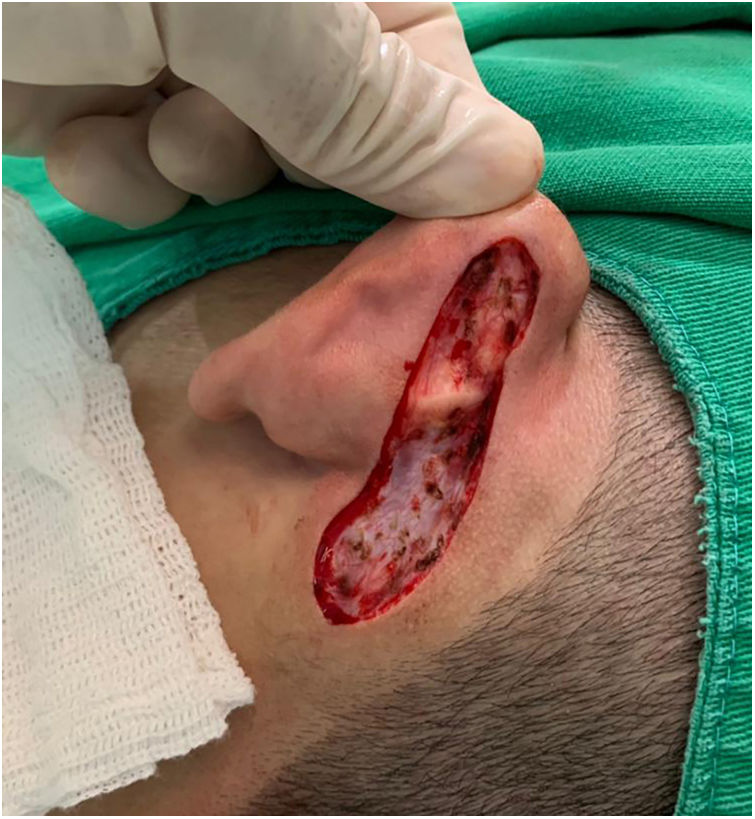
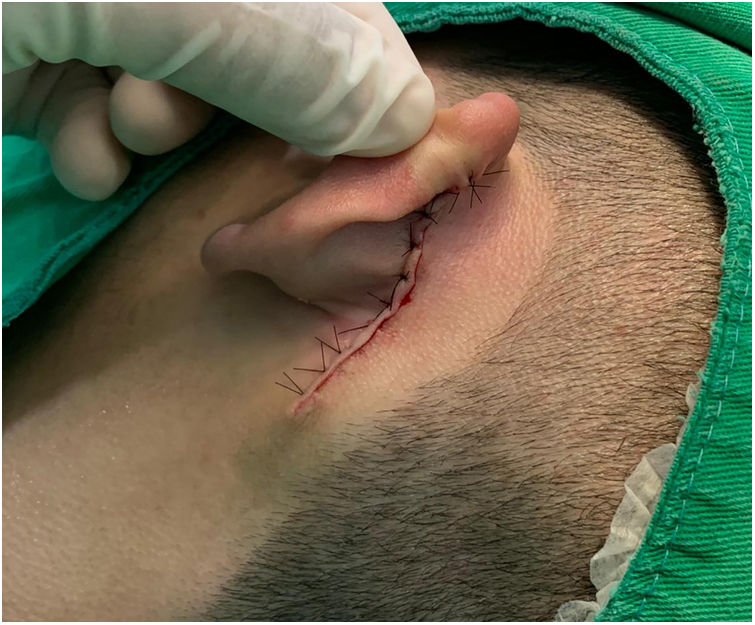
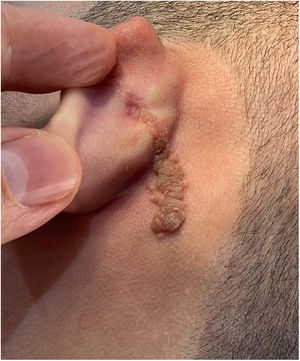
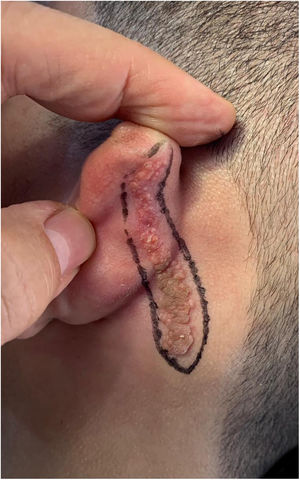
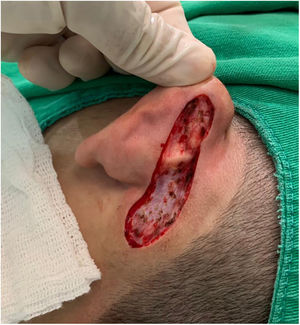
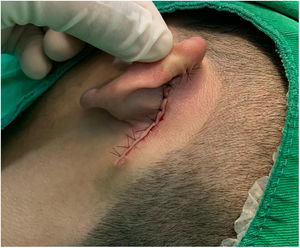
Relato do casoPaciente de 18 anos do sexo masculino, hígido e sem outras queixas, foi avaliado para um quadro de lesão congênita unilateral na região retroauricular esquerda. O exame físico revelou uma lesão linear que consistia em pápulas pigmentadas, levemente avermelhadas e acastanhadas, de aspecto verrucoso e com bordos bem definidos (fig. 1). Por meio da avaliação clínica, não foi relatada progressão da lesão, exceto pelo próprio crescimento físico do paciente. Na avaliação sistêmica não houve a detecção de nenhuma anormalidade. O paciente desejava a remoção da lesão por motivos estéticos e em razão de traumas por repetição. Ademais, havia preocupação parental em virtude de história positiva para óbito de um familiar em decorrência de melanoma, cujo indivíduo também era portador de nevos. A lesão sofreu exérese cirúrgica em caráter ambulatorial, com margem de segurança de 5mm até ao nível da fáscia muscular (figs. 2 e 3), com fechamento primário (fig. 4).
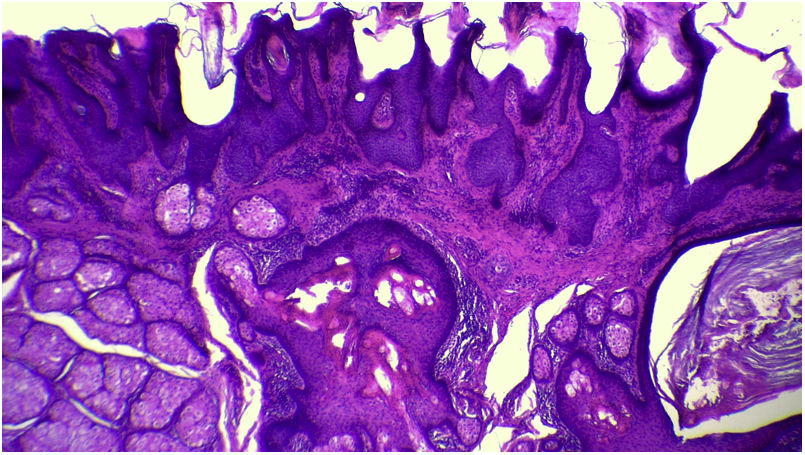
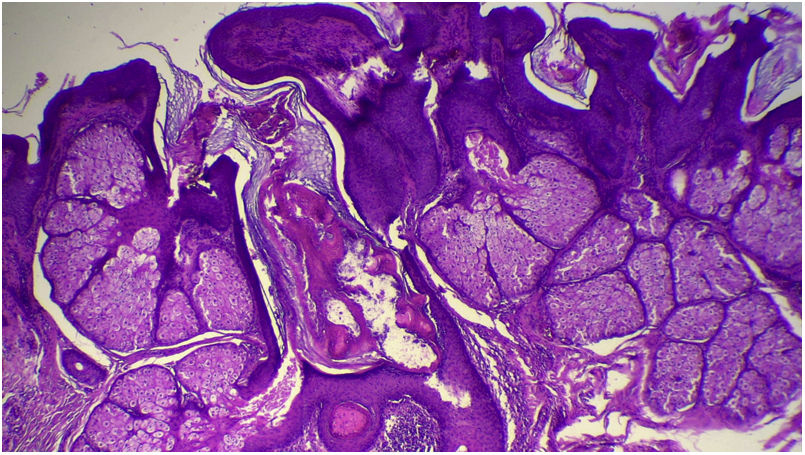
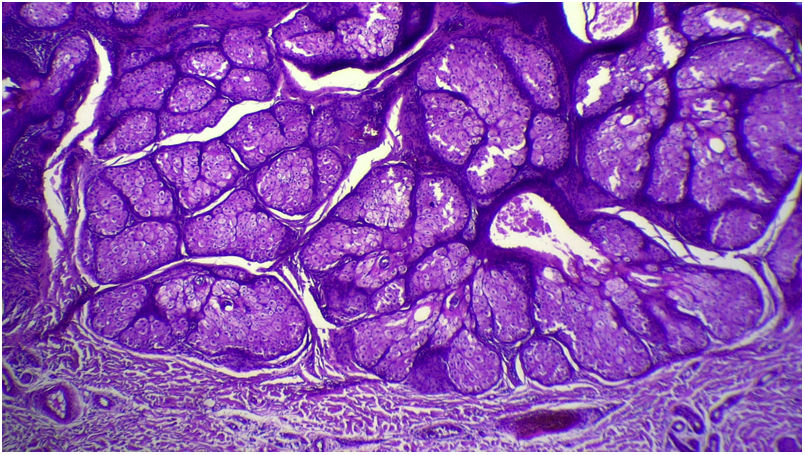
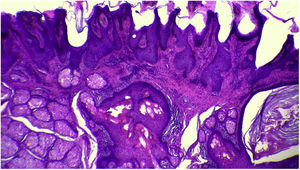
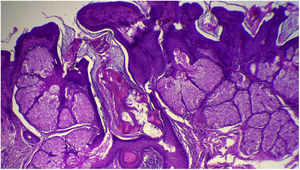
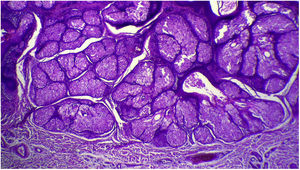
A avaliação anatomopatológica revelou discreta hiperceratose acompanhada de acantose em razão do aumento da espessura da epiderme. Além disso, pôde‐se evidenciar a presença de papilomatose demonstrada por intensas sinuosidades na junção dermoepidérmica, corroborada clinicamente pelo aspecto verrucoso da lesão (fig. 5). Foi possível notar, ainda, a hiperplasia das glândulas sebáceas, bem como a superficialização dessas estruturas anexiais (figs. 6 e 7). Desse modo, os achados histopatológicos foram consistentes com nevo sebáceo.
A incidência do nevo sebáceo em recém‐nascidos é estimada entre 0,1% e 0,3%,13 não demonstrando distinção por sexo ou etnia.2,12 Apesar de haver descrição de casos familiares, a lesão tem manifestação randômica.13 Em relação às principais áreas de acometimento, 62,5% das lesões estão no couro cabeludo, 24,5% no segmento cefálico, 4,7% no tronco e 4,2% na região cervical.17 Além do comprometimento cosmético, uma das maiores preocupações relacionadas a essa doença deve‐se à sua capacidade de gerar neoplasias secundárias.18 Estudos apontam que esse fenômeno ocorre em cerca de 10 a 20% dos casos, em sua maioria com pacientes com mais de 40 anos.12,19 Entretanto, a maioria das neoplasias secundárias é de natureza benigna, de modo que apenas aproximadamente 3% dos casos têm algum grau de malignidade, sendo considerados incidências raras.19 Dentre os principais tumores carcinogênicos, podem‐se citar: carcinoma basocelular (1,1%) e carcinoma espinocelular (0,57%), seguidos por carcinoma sebáceo e carcinoma apócrino.20 Como neoplasias secundárias de menor incidência referidas na literatura, tem‐se carcinoma sebáceo, carcinoma de células escamosas, carcinoma microcístico e melanoma.2,15,16,19,21
Apresentação clínicaAs afecções do nevo sebáceo se manifestam desde o nascimento ou pouco depois deste.2,16 A manifestação clínica das lesões pode ser subdividida em três estágios ou fases de evolução clínica com base no aspecto morfológico e na faixa etária do indivíduo acometido, ainda que a idade não estabeleça uma relação de maneira absoluta com as manifestações clínicas.21 O primeiro estágio corresponde à manifestação após o nascimento e se estende durante a infância, período em que as lesões apresentam‐se em formato de disco ou de pequenas manchas associadas, lisas ou parcialmente sem pelos e com coloração variando entre pálido, ligeiramente amarelado, amarelado‐rosado, laranja‐amarelado ou marrom.6,15 Durante a puberdade, o segundo estágio é caracterizado pela hiperplasia das glândulas sebáceas e demais estruturas anexiais em virtude da influência hormonal.6,15 Estudos apontam para a existência de receptores andrógenos no nevo sebáceo,4 de modo que as lesões assumem aspecto verrucoso e coloração mais intensa, em função dos processos de hiperceratose, papilomatose e acantose.6,14,15 Por fim, o terceiro estágio corresponde ao período de vida adulta, com maior risco de desenvolvimento de neoplasias secundárias.6,15
Em geral, lesão em forma linear do nevo é relatada na síndrome de Schimmelpenning‐Feuerstein‐Mims e, como parte componente, distúrbios multissistêmicos, os quais já foram descritos para uma grande diversidade de órgãos, como os sistemas nervoso, ocular, cardiovascular, muscular, urogenital, ósseo, dentre outros.14,15,22,23 Com o objetivo de facilitar a identificação e o diagnóstico clínico, a tabela 1 ilustra os principais distúrbios já identificados e relacionados com a síndrome de Schimmelpenning‐Feuerstein‐Mims, dentre as quais destacam‐se como mais frequentemente relatadas na literatura: raquitismo hipofosfatêmico, deficiência mental e cognitiva, coloboma e estrabismo.5,11,22
Manifestações clínicas extracutâneas da síndrome do nevo sebáceo5,11,22
| Esqueléticas | Cifoescoliose |
| Defeitos craniofaciais | |
| Deformidades nos membros | |
| Luxação de quadril | |
| Protuberância frontal | |
| Raquitismo hipofosfatêmico | |
| Neurológicas | Agenesia do corpo caloso |
| Agiria, microgiria ou paquigiria cortical | |
| Atrofia cerebral generalizada | |
| Convulsões | |
| Deficiência mental | |
| Deficiência cognitiva | |
| Displasia dos vasos cerebrais | |
| Hamartoma da glândula pineal | |
| Hamartoma do tálamo esquerdo | |
| Hemimegalencefalia | |
| Heterotopia cerebral | |
| Síndrome de Dandy‐Walker | |
| Oculares | Coloboma |
| Defeitos no nervo óptico | |
| Estrabismo | |
| Lipodermoide epibulbar | |
| Microftalmia | |
| Opacidade córnea | |
| Trato geniturinário | Criptorquidia |
| Hidronefrose | |
| Hipospádia | |
| Nefroblastomatose | |
| Obstrução da junção ureteropélvica | |
| Rim cístico | |
| Rim em ferradura | |
| Sistema coletor urinário duplicado | |
| Tumores testiculares e paratesticulares | |
| Cardiovasculares | Coarctação da aorta |
| Defeito do septo ventricular | |
| Hipoplasia aórtica | |
| Intraorais | Aplasia dos dentes |
| Cistos ósseos | |
| Esmalte hipoplásico | |
| Hemi‐hiperplasia da língua | |
| Sistema linfático | Linfedema |
| Quilotórax |
Em relação aos achados anatomopatológicos, a principal avaliação para orientação da conduta terapêutica refere‐se à análise do risco de desenvolvimento de neoplasias secundárias, o qual é baixo para carcinomas secundários e alto para neoplasias benignas.2 Nesse sentido, as principais neoplasias benignas relatadas são o tricoblastoma (TB) e o siringocistoadenoma papilífero (SCAP), seguidos por tricolemoma, adenoma sebáceo, tricolemoma desmoplásico, adenoma apócrino e poroma.2,18,23
O TB é definido como tumor tricogênico, formado pela proliferação de células germinativas foliculares.16 Ao exame histológico, o tricoblastoma evidencia células pequenas de morfologia arredondada a oval, agrupadas e separadas por estroma fibroso, com epitélio escamoso estratificado e áreas de necrose com calcificação.24
Siringocistoadenoma papilífero é resultante de neoplasia das glândulas sudoríparas apócrinas e écrinas, e se manifesta como manchas isoladas ou na forma de múltiplos nódulos formados por vesículas ou exsudato.16 Histologicamente, o SCAP é caracterizado como tumor anexial apócrino com projeções papilares e ductos císticos, os quais são recobertos por células colunares ou cuboidais, de citoplasma basofílico, possuindo, frequentemente, conexão com a epiderme.12
Quanto às neoplasias malignas, carcinoma basocelular (CBC) é a mais relatada, ainda que sua ocorrência seja considerada rara.2 O CBC tem significativa semelhança histológica com o tricoblastoma, de tal modo que suposições apontam para superestimação de sua real incidência como neoplasia secundária.2 A diferenciação ocorre pela análise da presença de estroma mixoide, além de retração do tecido estromal ao redor dos aglomerados celulares basaloides, estruturas típicas de CBC.24
No que se refere à perspectiva genética, diversos estudos apontam a relação entre o surgimento do nevo sebáceo, de maneira isolada ou como síndrome multissistêmica, e mutações nos genes HRAS, KRAS e NRAS, de tal modo que há a substituição do aminoácido glicina pelo aminoácido arginina, que por sua vez leva à ativação da via MAPK e PI3K‐AKT,7,16 com consequente aumento da proliferação celular nas células mutadas,6,7 o que foi confirmado por análise genética de células sanguíneas e tecidos oriundos de áreas não afetadas, corroborando a teoria do mosaicismo genético.15,25 A tabela 2 ilustra as neoplasias mais recorrentes na literatura médica associadas ao nevo sebáceo.2,12,23
Principais neoplasias secundárias2,12,23
| Benignas | Malignas |
|---|---|
| Adenoma sebáceo | Carcinoma anexial |
| Carcinoma apócrino | |
| Carcinoma basocelular | |
| Carcinoma de células escamosas | |
| Carcinoma mucoepidermoide | |
| Proliferação de células basaloides | Carcinoma sebáceo |
| Ceratoacantoma | |
| Sebaceoma | |
| Siringocistoadenoma papilífero | |
| Tricoblastoma | |
| Triquilemoma dermoplástico | |
| Verruca vulgaris |
Do mesmo modo que outros nevos epidérmicos, o nevo sebáceo pode ser permanentemente tratado com excisão de espessura total,13 em pacientes que se queixam de desconforto estético e psicológico.15 A remoção da lesão para fins profiláticos ainda é amplamente debatida.13 Buscando evidenciar e avaliar essa discussão, o artigo de Wali, Felton e McPherson, publicado em 2018, discorre sobre pesquisa realizada por meio de um questionário enviado para dermatologistas e cirurgiões plásticos do Reino Unido com o intuito de apurar a melhor intervenção atual para o gerenciamento do nevo sebáceo.26 Os resultados mostrados foram divergentes entre os dois grupos de especialistas, de modo que, enquanto mais de 90% dos cirurgiões plásticos julgaram a excisão profilática como a melhor conduta, apenas um terço dos dermatologistas apresentaram o mesmo posicionamento.26 Ademais, os cirurgiões plásticos recomendaram mais comumente a excisão na infância, em contrapartida aos dermatologistas, que optaram por esperar até a idade adulta.26
Além da excisão, outros métodos são frequentemente utilizados para tratamento e melhora da lesão de Jadassohn, como curetagem, cauterização, crioterapia, terapia fotodinâmica,15,25,27 ácido salicílico tópico, retinoides tópicos e sistêmicos, aplicação tópica de análogo da vitamina D, tratamento a laser e dermoabrasão.3,15,25
Em indivíduos que apresentam maior comprometimento dos sistemas, em virtude da síndrome de Schimmelpenning‐Feuerstein‐Mims, é recomendado orientar conduta multidisciplinar para o tratamento, com a colaboração de dermatologista, pediatra, neurologista, oftalmologista, geneticista7 ou qualquer outro subespecialista, caso seja necessário.2,7 O uso da dermatoscopia para monitoramento de possíveis complicações também é indicado.16,28
ConclusãoAinda que a síndrome de Schimmelpenning‐Feuerstein‐Mims apresente manifestação rara, é importante salientar que seu diagnóstico seja considerado em crianças nascidas com nevo sebáceo, quando também associado a anormalidades em nível sistêmico, exigindo, assim, correta avaliação e manejo com o intuito de minimizar complicações extracutâneas. Mesmo não havendo consenso acerca da melhor opção terapêutica para o nevo sebáceo, a remoção cirúrgica é frequentemente relatada como uma alternativa viável diante do aspecto estético e do bem‐estar do paciente no que se refere à sua autoestima, além do risco de malignidade da lesão, mesmo que esse seja extremamente baixo.
Suporte financeiroNenhum.
Contribuição dos autoresManoel Pereira da Silva Neto: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; participação efetiva na orientação da pesquisa; elaboração e redação do manuscrito; revisão crítica da literatura; revisão crítica do manuscrito.
Barbara Rodovalho de Assis: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito; revisão crítica da literatura; revisão crítica do manuscrito.
Gustavo Rodrigues Andrade: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito; revisão crítica da literatura; revisão crítica do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Neto MPS, Assis BR, Andrade GR. Sebaceous nevus of Jadassohn: review and clinical‐surgical approach. An Bras Dermatol. 2022;97:628–36.
Trabalho realizado no Instituto de Cirurgia Plástica Manoel Pereira e no Hospital São Marcos, Uberaba, MG, Brasil.