O herpes anogenital é uma das infecções sexualmente transmissíveis mais prevalentes no mundo. Apresenta diversas manifestações clínicas, desde quadros de primoinfecção herpética a formas recidivantes, dentre as quais o herpes mucocutâneo crônico. Essa apresentação é rara, caracterizada por duração de mais de quatro semanas, geralmente associada a quadros de imunossupressão e a resistência ao tratamento anti‐herpético clássico. O presente estudo apresenta série de dez casos de herpes mucocutâneo crônico com discussão sobre seus aspectos clínicos, laboratoriais e terapêuticos.
O herpes mucocutâneo crônico (HMCC) é a infecção causada pelos herpes‐vírus (HSV) tipo 1 e 2, com duração de mais de quatro semanas, resistente ao tratamento anti‐herpético clássico.1
O HMMC apresenta manifestações clínicas atípicas, com necessidade de confirmação por métodos complementares citológicos, laboratoriais ou anatomopatológicos.1 Em geral, é caracterizado clinicamente por lesões ulceradas dolorosas, de crescimento progressivo, que ocasionalmente evoluem para formas verrucosas, vegetantes ou tumorais, principalmente na síndrome de reconstituição imune do vírus HIV.1,2 O tratamento é desafiador: o hospedeiro costuma apresentar imunossupressão pronunciada, dificultando a resposta de defesa eficaz contra o agente agressor e a cicatrização eficiente da lesão. Por outro lado, é cada vez mais descrita a resistência viral intrínseca aos medicamentos clássicos, como aciclovir e valaciclovir.3–6
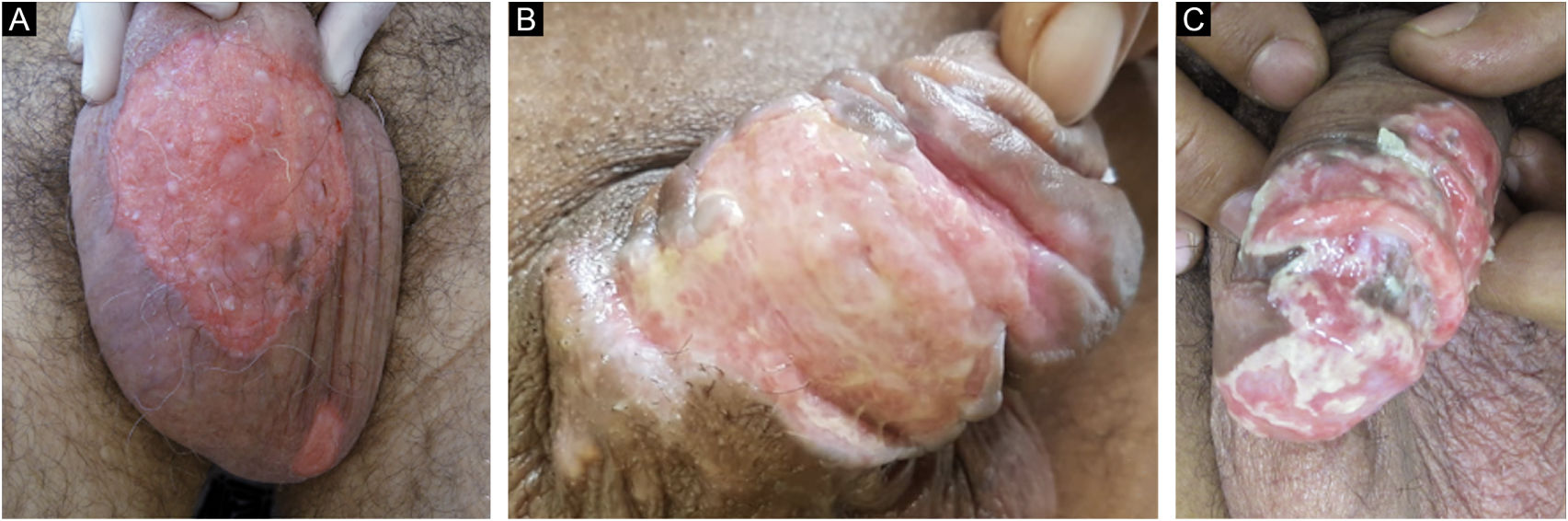
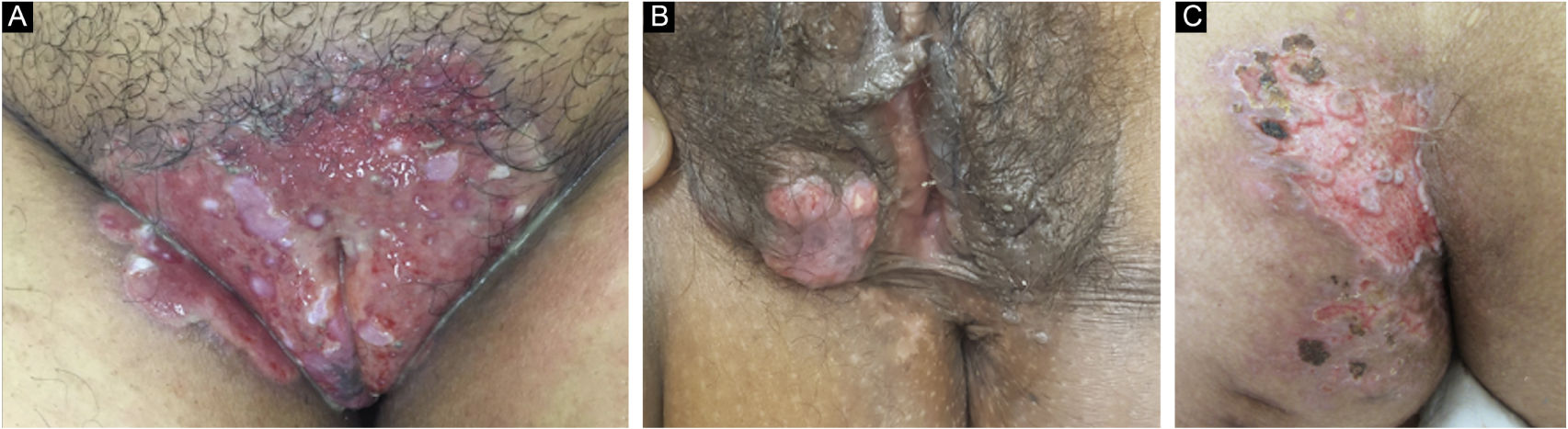
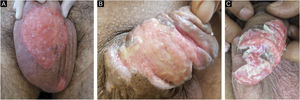
Dez pacientes com diagnóstico clínico e laboratorial de HMCC foram incluídos em estudo retrospectivo em clínica de dermatologia de hospital terciário em São Paulo (Brasil) entre janeiro de 2013 e novembro de 2020. Os dados detalhados constam na tabela 1, e aspectos clínicos estão mostrados nas figuras 1 e 2. Ressaltamos que todos relataram antecedente de quadro herpético local, indicando que as formas apresentadas de HMCC seriam variantes do herpes recidivante, e não de primoinfecção.
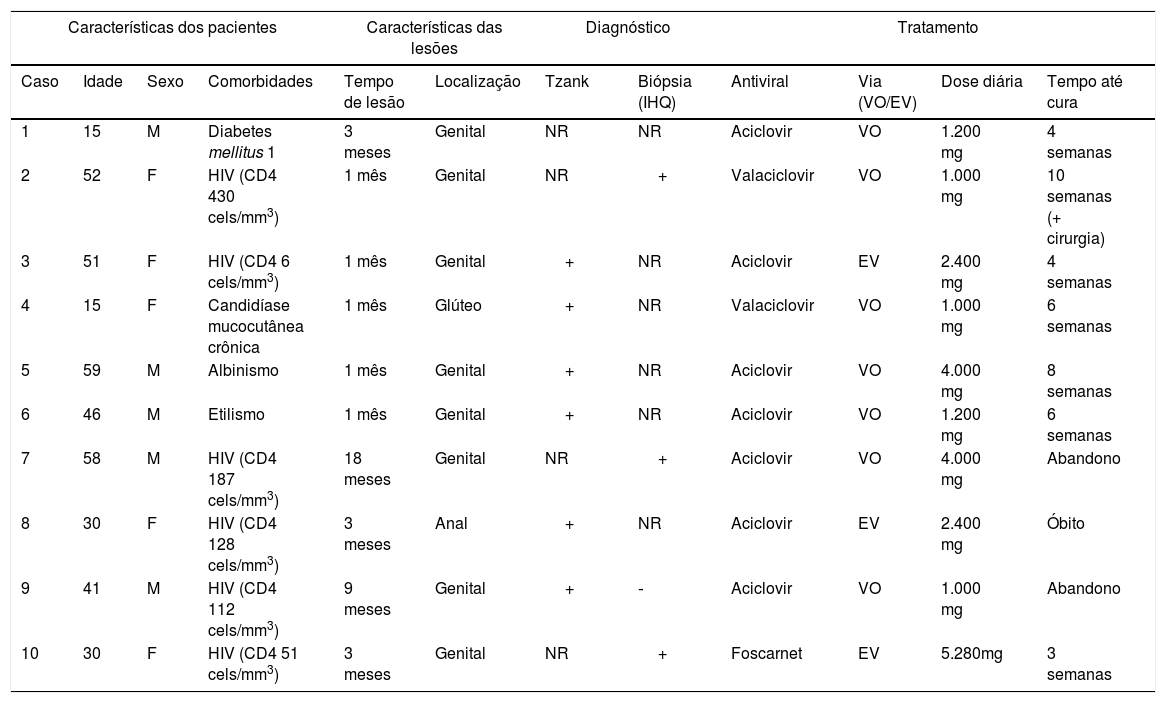
Herpes mucocutâneo crônico: aspectos clínicos dos dez pacientes incluídos, métodos diagnósticos e resposta terapêutica
| Características dos pacientes | Características das lesões | Diagnóstico | Tratamento | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Caso | Idade | Sexo | Comorbidades | Tempo de lesão | Localização | Tzank | Biópsia (IHQ) | Antiviral | Via (VO/EV) | Dose diária | Tempo até cura |
| 1 | 15 | M | Diabetes mellitus 1 | 3 meses | Genital | NR | NR | Aciclovir | VO | 1.200 mg | 4 semanas |
| 2 | 52 | F | HIV (CD4 430 cels/mm3) | 1 mês | Genital | NR | + | Valaciclovir | VO | 1.000 mg | 10 semanas (+ cirurgia) |
| 3 | 51 | F | HIV (CD4 6 cels/mm3) | 1 mês | Genital | + | NR | Aciclovir | EV | 2.400 mg | 4 semanas |
| 4 | 15 | F | Candidíase mucocutânea crônica | 1 mês | Glúteo | + | NR | Valaciclovir | VO | 1.000 mg | 6 semanas |
| 5 | 59 | M | Albinismo | 1 mês | Genital | + | NR | Aciclovir | VO | 4.000 mg | 8 semanas |
| 6 | 46 | M | Etilismo | 1 mês | Genital | + | NR | Aciclovir | VO | 1.200 mg | 6 semanas |
| 7 | 58 | M | HIV (CD4 187 cels/mm3) | 18 meses | Genital | NR | + | Aciclovir | VO | 4.000 mg | Abandono |
| 8 | 30 | F | HIV (CD4 128 cels/mm3) | 3 meses | Anal | + | NR | Aciclovir | EV | 2.400 mg | Óbito |
| 9 | 41 | M | HIV (CD4 112 cels/mm3) | 9 meses | Genital | + | ‐ | Aciclovir | VO | 1.000 mg | Abandono |
| 10 | 30 | F | HIV (CD4 51 cels/mm3) | 3 meses | Genital | NR | + | Foscarnet | EV | 5.280mg | 3 semanas |
M, masculino; F, feminino; NR, não realizado;+, positivo; ‐, negativo; HIV, vírus da imunodeficiência humana; VO, via oral; EV, via endovenosa.
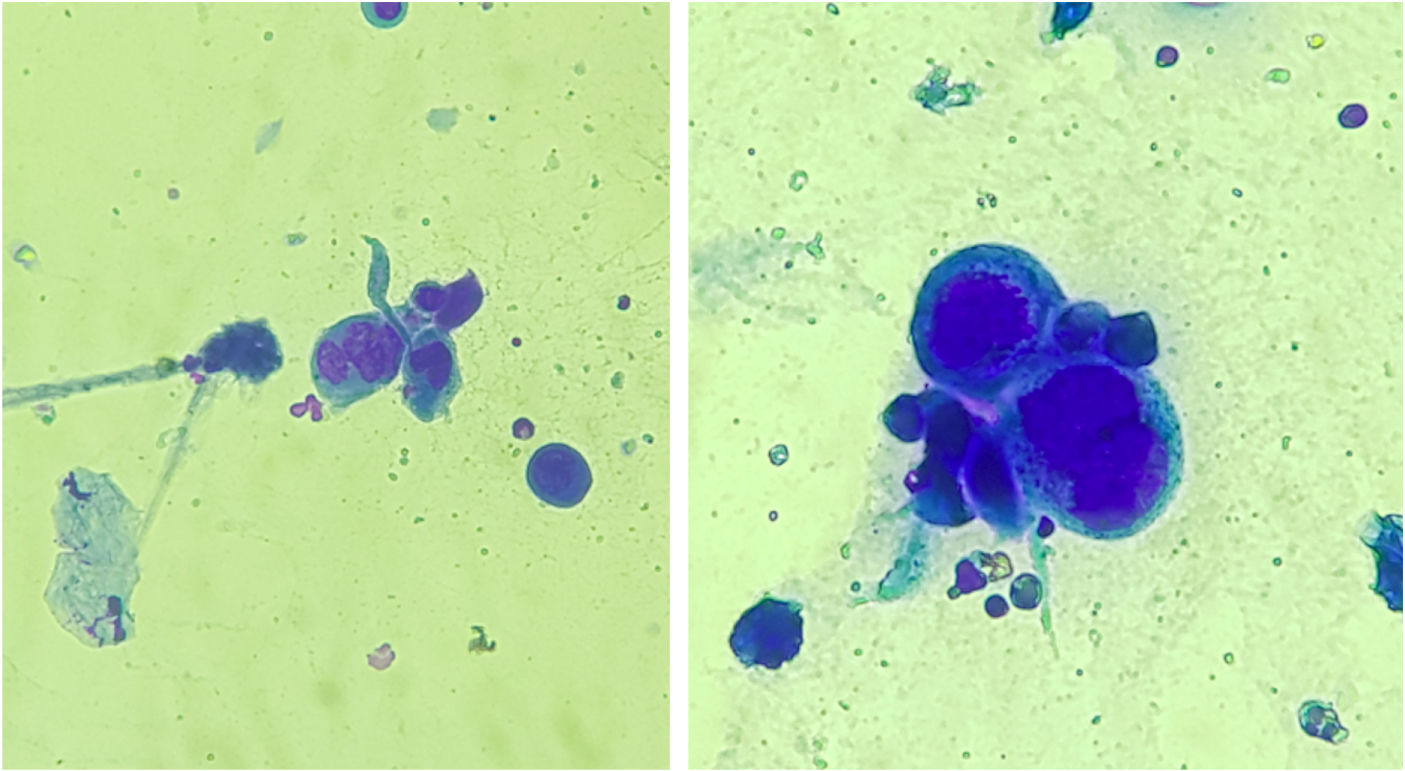
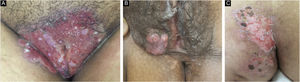
Casos anogenitais por HSV‐2 têm até seis vezes mais episódios de recorrência que os atribuídos ao HSV‐1, além de se manifestarem em forma subclínica em 10 a 25% dos pacientes.7 O citodiagnóstico de Tzank (fig. 3) e a imuno‐histoquímica para HSV1+2 não diferenciam o parasitismo decorrente de HSV1 ou HSV2. O diagnóstico dos casos de HMCC deve ser realizado, preferencialmente, com biópsia de pele, pois a amostra pode também ser analisada pela hibridização in situ e reação em cadeia da polimerase (PCR) em busca da identificação viral.3,4,8 Além disso, o exame descarta diagnósticos diferenciais de úlceras genitais como sífilis, infecção por citomegalovírus, cancro mole, infecções fúngicas ou por protozoários.
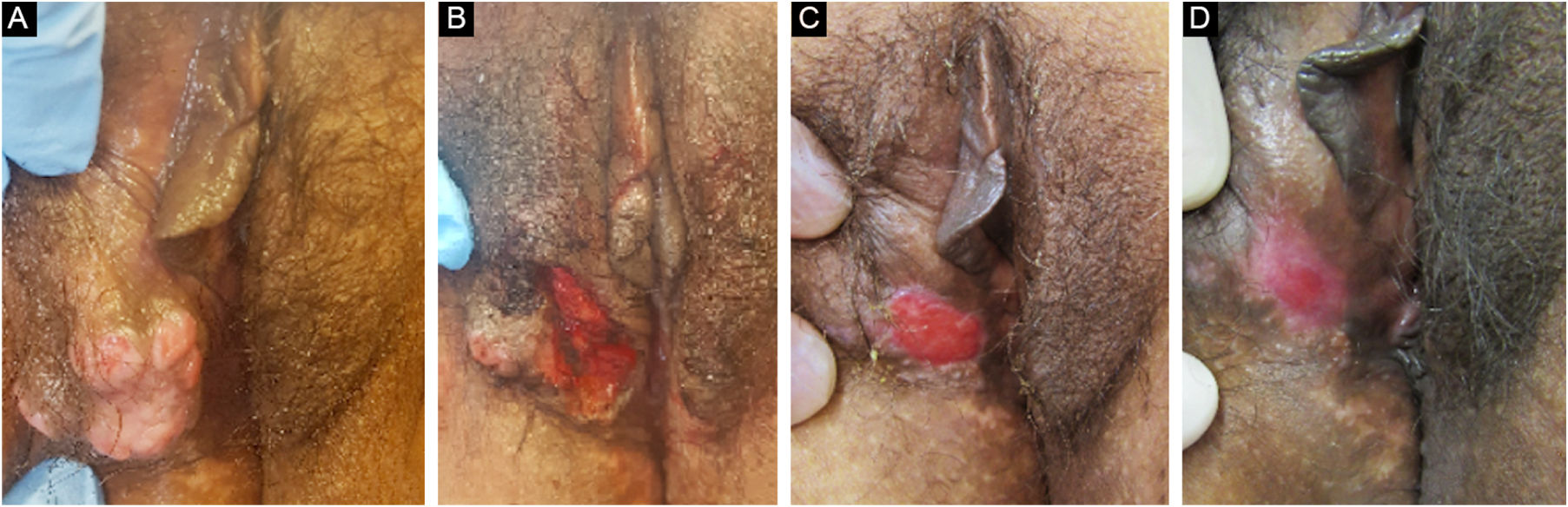
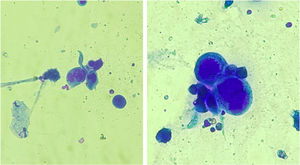
O tratamento empregado em 70% dos casos foi com aciclovir, seguido de valaciclovir em 20% e foscarnete em 10%. Duas pacientes apresentavam forma hipertrófica verrucosa, e a abordagem terapêutica nesses casos foi conforme descrita por diversos autores, com antiviral associado a terapia local (exérese cirúrgica ou imiquimode tópico), apresentando melhora significativa (fig. 4).2,3
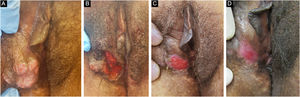
Paciente com herpes mucocutâneo crônico hipertrófico tumoral. (A), Pré‐tratamento. (B), No pós‐operatório imediato da remoção cirúrgica da lesão tumoral. (C), Após quatro semanas da exérese cirúrgica, com ferida operatória em cicatrização. (D), Após 10 semanas do procedimento, com lesão cicatrizada.
O tratamento das formas crônicas ulceradas recomenda o uso de aciclovir oral, na dose diária de 1.000 mg, inicialmente por uma a duas semanas. Essa dose diária pode ser mantida ou aumentada para 4.000 mg, e a medicação pode ser administrada por via intravenosa (10 mg/kg, 3×/dia) em casos de resistência ou para superar problemas de biodisponibilidade, pelo mesmo período. Na persistência de falha terapêutica, indica‐se valaciclovir oral (dose diária de 3.000 mg) ou fanciclovir (dose diária de 550 a 1.500 mg), de uma a duas semanas. Se considerada população viral resistente, cujo principal fator associado é o uso prolongado dos antivirais, é sugerido o uso de antivirais com outros mecanismos de ação, como foscarnet, cidofovir e vidarabina.1,3,4,8 Além dessa abordagem medicamentosa voltada ao combate direto do HSV, é fundamental reverter a imunossupressão do paciente.
O herpes mucocutâneo crônico, apesar de bem estabelecido na literatura, é raro e pouco conhecido. A diversidade de apresentações clínicas e sua resistência terapêutica reforçam o desafio no manejo dessa doença. Assim, conhecer os aspectos aqui detalhados auxilia os médicos no diagnóstico e na conduta, otimizando a terapêutica e diminuindo a morbidade dos pacientes.
Suporte financeiroNenhum.
Contribuição dos autoresKarina Baruel de Camargo Votto Calbucci: Elaboração e redação do manuscrito; obter, analisar e interpretar os dados; revisão crítica da literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
John Verrinder Veasey: Concepção e planejamento do estudo; participação efetiva na orientação da pesquisa; participação intelectual na conduta propedêutica e/ou terapêutica dos casos estudados; elaboração e redação do manuscrito; obter, analisar e interpretar os dados; revisão crítica da literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Calbucci KBCV, Veasey JV. Chronic mucocutaneous anogenital herpes: series of ten cases and literature review. An Bras Dermatol. 2022;97:362–5.
Trabalho realizado na Clínica de Dermatologia, Santa Casa de Misericórdia de São Paulo, SP, Brasil.