Campo de cancerização cutâneo (CCC) compreende área de pele clinicamente normal com células geneticamente alteradas, justificando a alta incidência de neoplasias ou a recorrência de tumores completamente excisados.1 Ceratose actínica (CA) é manifestação da atividade do CCC, cujo tratamento pode contribuir na redução de tumores cutâneos.2
Polypodium leucatomos (PL) contém polifenóis com possível atividade antineoplásica. Tratamento com terapia fotodinâmica (PDT) associada a PL oral durante seis meses reduziu em 88% a contagem de CA facial, o que foi ligeiramente superior ao tratamento com PDT isolada (71%).3 Colchicina tópica promoveu redução na contagem de CAs semelhante a uma sessão de PDT, nos antebraços.4 Mebutato de ingenol (MI) proporciona 42% de clearance total de CAs nos antebraços, com efeito sustentado após seis meses.5
Até o momento, não há estudos comparando colchicina com MI no tratamento do CCC, ou avaliando a eficácia do PL oral.
Realizou‐se ensaio randomizado, autocontrolado, fatorial, duplo‐cego para o tratamento oral e aberto para os tratamentos tópicos, objetivando avaliar a eficácia do creme de colchicina 0,5%, MI 0,05% gel e PL oral, no tratamento de CAs e CCC dos antebraços.
O estudo foi realizado no ambulatório de Dermatologia da Faculdade de Medicina da Universidade Estadual Paulista (UNESP) entre maio de 2019 e dezembro de 2020. Cinquenta indivíduos com três até dez CAs em ambos os antebraços, imunocompetentes, sem outra afecção cutânea foram randomizados para receber PL 500 mg oral, 2×/dia ou um comprimido placebo contendo hidrocelulose na mesma posologia e em cápsulas de idêntica coloração e tamanho (PLAC) durante 60 dias. Após a randomização do tratamento oral, seus antebraços foram randomizados para receber: colchicina 0,5% creme 2×/dia durante 7 dias (COL), MI 0,05% gel (Picato®, LEOPharma®) 1×/dia por dois dias (IM), ou apenas filtro solar (Anthelios XL Protect®) FPS 30 (SC). Todos os pacientes foram orientados a usar filtro solar nos antebraços. Desse modo, seis grupos de antebraços em tratamento foram formados: PL+COL, PL+MI, PL+SC, PLAC+COL, PLAC+MI e PLAC+SC.
Os participantes foram avaliados em D0 para: inclusão, randomização, avaliação clínica: contagem de CAs, escore de gravidade das ceratoses actínicas (EGCA),6 escala de fotoenvelhecimento dos antebraços (EFA)7 e início do tratamento; no D15 para avaliação de eventos adversos (EA); D60 e D180 para nova avaliação clínica.
Doze pacientes foram selecionados por conveniência e biopsiados em D0, D60 e D180, na região central de cada antebraço, em área livre de lesão clinicamente compatível com CA, para avaliação do escore KIN (Keratinocyte Intraepithelial Neoplasia).8
O projeto foi aprovado pelo Comitê de Ética, e o ensaio clínico foi registrado no REBEC (https://ensaiosclinicos.gov.br/rg/RBR‐5q5dg8).
O desfecho primário foi o clearance total de CAs no D60. Os desfechos secundários foram: clearance parcial (–50% CA) e redução da atividade do CCC, analisada pelo EGCA, EFA e KIN, em D60 e D180, com o objetivo de analisar a manutenção da resposta aos tratamentos ao longo do tempo. O tamanho da amostra foi dimensionado para detectar diferença de redução > 20% entre os grupos (poder=0,9; alfa=0,05), resultando em 16 antebraços por grupo (48 pacientes).
Todos os participantes incluídos no estudo fizeram parte da população ITT (intention to treat). A contagem de CA, EGCA, EFA e KIN foi comparada de acordo com o tempo, e os grupos por modelo linear generalizado de efeitos mistos. Valores ausentes/dropouts foram imputados pela análise do modelo misto. A significância foi definida como valor p <0,05 unicaudal.
Houve 77 pacientes elegíveis para o estudo, porém 27 foram excluídos (15 não apresentavam todos os critérios de inclusão em ambos os antebraços e 12 negaram participação. Cinquenta pacientes foram então incluídos, de modo que 25 foram randomizados para o grupo PL e 25 para o grupo PLAC. Os grupos formados foram: PL+COL (17 antebraços), PL+MI (16), PL+SC (17), PLAC+COL (17), PLAC+MI (15) e PLAC+SC (18). Houve quatro dropouts, dois no D60 e dois no D180 (um para cada grupo de tratamento oral), não ligados a EA dos tratamentos.
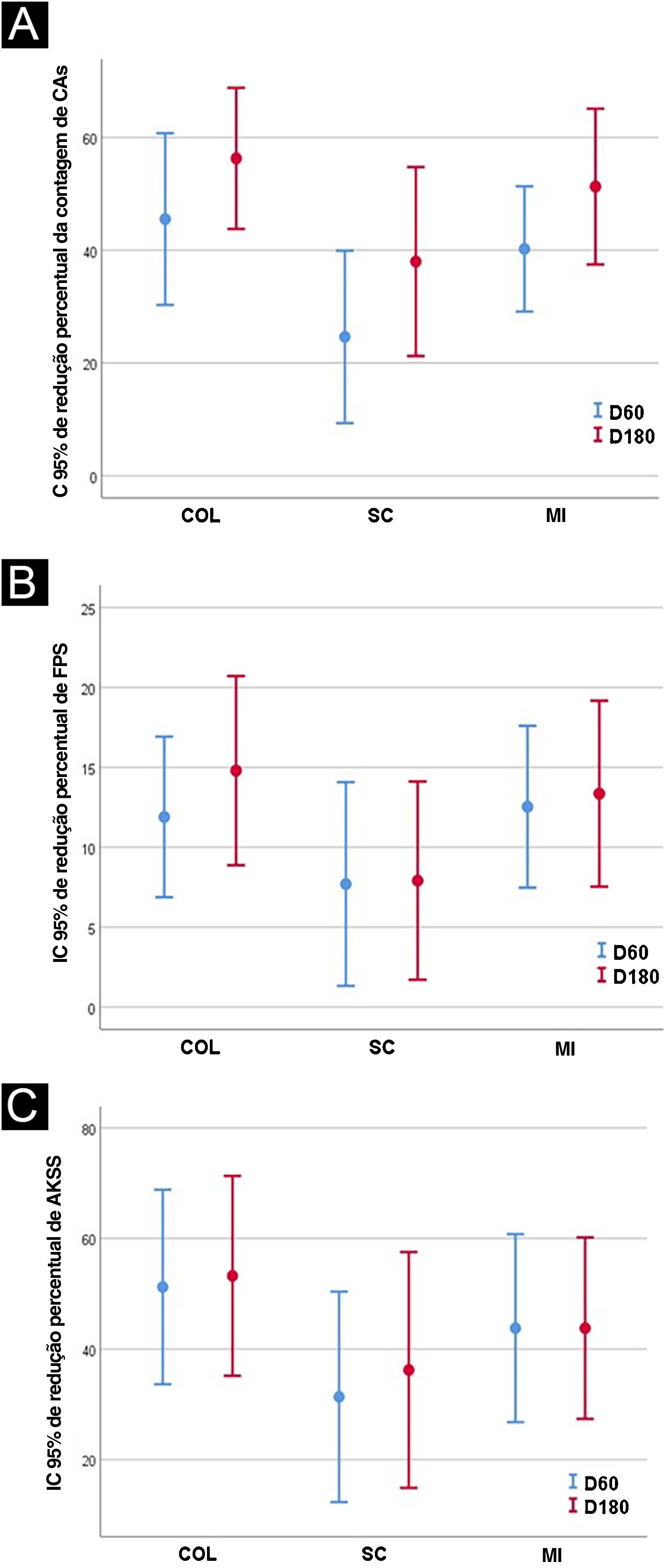
As principais características demográficas dos participantes estão dispostas na tabela 1. Clearance total no D60 foi observado em dois antebraços (8,0%) no grupo PL e 3 (12,0%) no PLAC, sem diferença entre si (p=0,26). Em relação aos tópicos, o clearance total foi obtido em cinco antebraços (14,7%) no grupo COL, 5 (16,1%) no MI, e 1 (2,8%) no SC (p=0,8). Clearance parcial foi alcançado em 11 (44,0%) antebraços no grupo PL, 11 (44,0%) no PLAC (p=0,26); 18 (52,9%) no COL, 17 (54,8%) no MI e 9 (25,7%) no grupo SC (p=0,24).
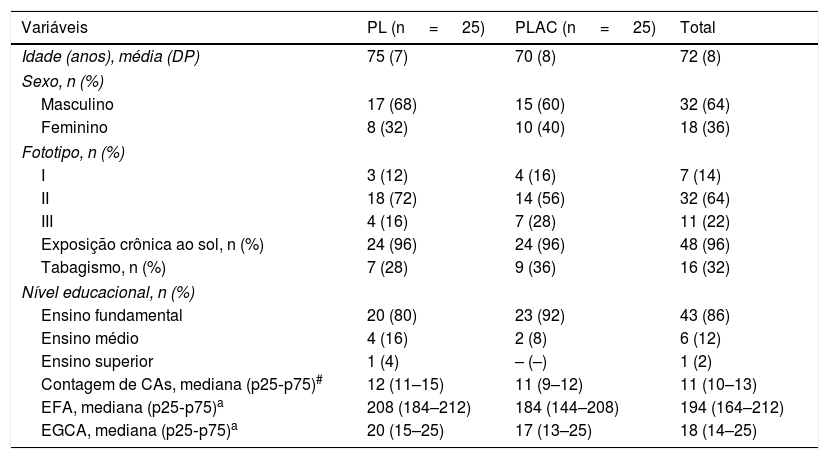
Principais características demográficas dos participantes (n=50)
| Variáveis | PL (n = 25) | PLAC (n = 25) | Total |
|---|---|---|---|
| Idade (anos), média (DP) | 75 (7) | 70 (8) | 72 (8) |
| Sexo, n (%) | |||
| Masculino | 17 (68) | 15 (60) | 32 (64) |
| Feminino | 8 (32) | 10 (40) | 18 (36) |
| Fototipo, n (%) | |||
| I | 3 (12) | 4 (16) | 7 (14) |
| II | 18 (72) | 14 (56) | 32 (64) |
| III | 4 (16) | 7 (28) | 11 (22) |
| Exposição crônica ao sol, n (%) | 24 (96) | 24 (96) | 48 (96) |
| Tabagismo, n (%) | 7 (28) | 9 (36) | 16 (32) |
| Nível educacional, n (%) | |||
| Ensino fundamental | 20 (80) | 23 (92) | 43 (86) |
| Ensino médio | 4 (16) | 2 (8) | 6 (12) |
| Ensino superior | 1 (4) | – (–) | 1 (2) |
| Contagem de CAs, mediana (p25‐p75)# | 12 (11–15) | 11 (9–12) | 11 (10–13) |
| EFA, mediana (p25‐p75)a | 208 (184–212) | 184 (144–208) | 194 (164–212) |
| EGCA, mediana (p25‐p75)a | 20 (15–25) | 17 (13–25) | 18 (14–25) |
PL, grupo P. leucatomos; PLAC, grupo placebo; EFA, escala de fotoenvelhecimento dos antebraços; EGCA, escore de gravidade das ceratoses actínicas.
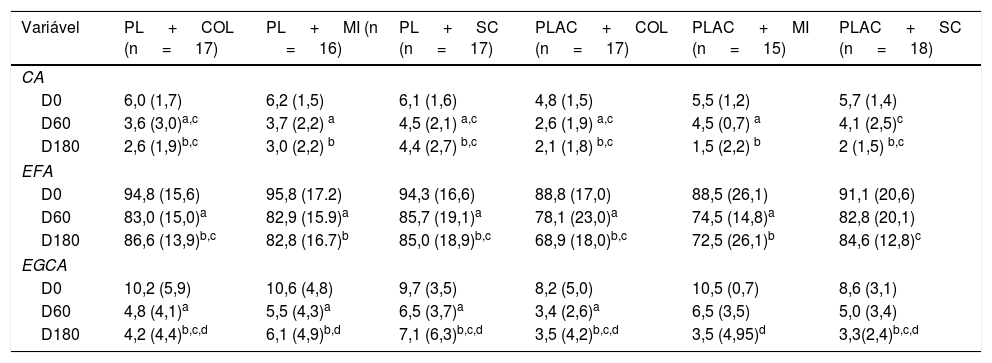
Os resultados após 60 e 180 dias para contagem de AK, escala de fotoenvelhecimento do antebraço e EGCA estão exibidos na tabela 2 e figura 1.
Principais desfechos clínicos decorrentes dos tratamentos (n=100 antebraços)
| Variável | PL + COL (n = 17) | PL + MI (n = 16) | PL + SC (n = 17) | PLAC + COL (n = 17) | PLAC + MI (n = 15) | PLAC + SC (n = 18) |
|---|---|---|---|---|---|---|
| CA | ||||||
| D0 | 6,0 (1,7) | 6,2 (1,5) | 6,1 (1,6) | 4,8 (1,5) | 5,5 (1,2) | 5,7 (1,4) |
| D60 | 3,6 (3,0)a,c | 3,7 (2,2) a | 4,5 (2,1) a,c | 2,6 (1,9) a,c | 4,5 (0,7) a | 4,1 (2,5)c |
| D180 | 2,6 (1,9)b,c | 3,0 (2,2) b | 4,4 (2,7) b,c | 2,1 (1,8) b,c | 1,5 (2,2) b | 2 (1,5) b,c |
| EFA | ||||||
| D0 | 94,8 (15,6) | 95,8 (17.2) | 94,3 (16,6) | 88,8 (17,0) | 88,5 (26,1) | 91,1 (20,6) |
| D60 | 83,0 (15,0)a | 82,9 (15.9)a | 85,7 (19,1)a | 78,1 (23,0)a | 74,5 (14,8)a | 82,8 (20,1) |
| D180 | 86,6 (13,9)b,c | 82,8 (16.7)b | 85,0 (18,9)b,c | 68,9 (18,0)b,c | 72,5 (26,1)b | 84,6 (12,8)c |
| EGCA | ||||||
| D0 | 10,2 (5,9) | 10,6 (4,8) | 9,7 (3,5) | 8,2 (5,0) | 10,5 (0,7) | 8,6 (3,1) |
| D60 | 4,8 (4,1)a | 5,5 (4,3)a | 6,5 (3,7)a | 3,4 (2,6)a | 6,5 (3,5) | 5,0 (3,4) |
| D180 | 4,2 (4,4)b,c,d | 6,1 (4,9)b,d | 7,1 (6,3)b,c,d | 3,5 (4,2)b,c,d | 3,5 (4,95)d | 3,3(2,4)b,c,d |
PL, Polypodium leucatomos; SC, filtro solar FPS 30; MI, mebutato de ingenol; COL, colchicina; CA, contagem de ceratoses actínicas; EFA, escala de fotoenvelhecimento dos antebraços; EGCA, escore de gravidade das ceratoses actínicas.
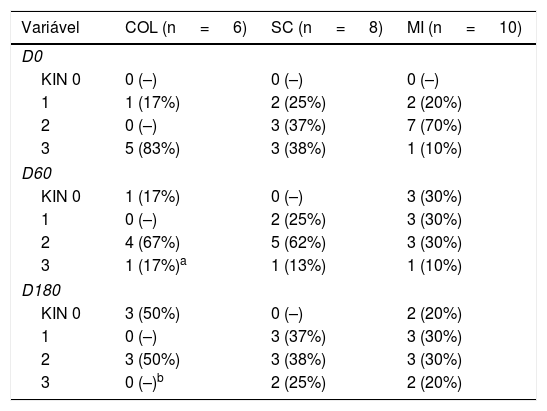
A análise do KIN não mostrou interferência dos tratamentos orais no seu comportamento em D60 e D180, de modo que a avaliação foi subsequentemente realizada apenas com os tópicos. Por outro lado, análise posterior do efeito dos tratamentos tópicos revelou que o COL reduziu o KIN após 60 e 180 dias de tratamento (p <0,05), enquanto os demais tratamentos não apresentaram resposta semelhante (tabela 3).
Resultados do KIN para os grupos COL, SC e MI (n=24 antebraços)
| Variável | COL (n = 6) | SC (n = 8) | MI (n = 10) |
|---|---|---|---|
| D0 | |||
| KIN 0 | 0 (–) | 0 (–) | 0 (–) |
| 1 | 1 (17%) | 2 (25%) | 2 (20%) |
| 2 | 0 (–) | 3 (37%) | 7 (70%) |
| 3 | 5 (83%) | 3 (38%) | 1 (10%) |
| D60 | |||
| KIN 0 | 1 (17%) | 0 (–) | 3 (30%) |
| 1 | 0 (–) | 2 (25%) | 3 (30%) |
| 2 | 4 (67%) | 5 (62%) | 3 (30%) |
| 3 | 1 (17%)a | 1 (13%) | 1 (10%) |
| D180 | |||
| KIN 0 | 3 (50%) | 0 (–) | 2 (20%) |
| 1 | 0 (–) | 3 (37%) | 3 (30%) |
| 2 | 3 (50%) | 3 (38%) | 3 (30%) |
| 3 | 0 (–)b | 2 (25%) | 2 (20%) |
SC, filtro solar FPS30; MI, mebutato de ingenol; COL, colchicina.
Quanto aos EA, dois pacientes (8%) no grupo PLAC apresentaram diarreia e dois no grupo PL (8%), epigastralgia. Em relação aos tópicos, EA moderados locais foram vistos em 13% do grupo MI, 23% e 8% nos grupos COL e SC.
O único ensaio com PL oral no CCC associou‐o a duas sessões de PDT, com maior redução da contagem de CA do couro cabeludo quando comparado a apenas PDT.3 Apesar de nosso estudo ter sido realizado nos antebraços, cujos resultados são menos expressivos, o estudo anterior não foi placebo‐controlado, sugerindo possível viés.
Colchicina tópica em creme a 0,5% 2×/semana durante 10 dias foi comparada com uma sessão de PDT nos antebraços para o tratamento de CA, mostrando clearance total de 17% e redução de 42% da contagem de CA, sem diferenças do PDT.4 Em nosso estudo, clearance total foi comparável (16%). Outra observação é sua superioridade sobre SC mesmo no D180 na contagem de CA e EFA, sugerindo resposta sustentada. Recentemente, a tirbanibulina, um inibidor sintético da polimerização da tubulina semelhante à colchicina, apresentou resultados promissores no tratamento das CAs da face, com clearance total em 54% dos pacientes avaliados dois meses após seu uso tópico a 1% durante cinco dias no tratamento do CCC, o que reforça as evidências positivas quanto ao uso de substâncias antiproliferativas.
O MI já foi comparado com alguns dos tratamentos disponíveis, mostrando eficácia semelhante ao diclofenaco e imiquimode, com o benefício de um regime de tratamento mais curto. Por outro lado, nosso estudo mostrou clearance inferior ao da literatura. Em nosso estudo, as áreas tratadas foram superiores a 25 cm2, recomendada pelo fabricante, o que pode ter reduzido a eficácia do MI pela menor concentração do produto por unidade de área.
A Agência Europeia de Medicamentos suspendeu da comercialização de MI após análise de estudos de fase IV que evidenciaram possível relação com aumento do risco de carcinoma espinocelular.9 Um dos participantes do grupo MI desenvolveu, no D180, um ceratoacantoma no antebraço, salientando a importância do seguimento de longo prazo. Há, portanto, a possibilidade a existência de viés de publicação dos estudos com MI no tratamento da CA, explicando a controvérsia entre os resultados.
A perda da polarização nuclear contribui para caracterizar a atividade do CCC.10 A redução do KIN pela colchicina é evidência de seus efeitos na proliferação de queratinócitos. Esse mesmo parâmetro foi avaliado em estudo anterior, com resultados semelhantes após 60 dias de tratamento.4 Este estudo é o primeiro que avaliou a resposta sustentada da displasia de queratinócitos após o uso de colchicina. Mais estudos são necessários, incluindo posologias e vias diferentes de colchicina tópica, a fim de avaliar a redução histológica de atividade do CCC.
Este estudo tem limitações: foi monocêntrico desenvolvido no SUS, o que minimiza a generalização dos resultados. Além disso, tanto o PL quanto a colchicina foram produzidos em farmácia de manipulação, o que pode infligir certa variabilidade em relação ao produto industrial.
Em conclusão, colchicina apresentou eficácia e tolerabilidade no tratamento de CAs e CCC, melhorando também os sinais de fotodano nos antebraços, podendo representar alternativa no tratamento do CCC, principalmente para a população de baixa renda.
Contribuição dos autoresMiola AC: Concepção e planejamento do estudo; participação efetiva na orientação da pesquisa; obtenção, análise e interpretação dos dados; revisão crítica da literatura; revisão crítica do manuscrito, escrita e aprovação da versão final do manuscrito.
Miot HA: Concepção e planejamento do estudo; participação efetiva na orientação da pesquisa; desenvolvimento do projeto, análise e interpretação dos dados; revisão crítica da literatura; revisão crítica do manuscrito, escrita e aprovação da versão final do manuscrito.
Suporte financeiroFUNADERM (Fundo de Apoio à Dermatologia).
Conflito de interessesNenhum.
Como citar este artigo: Miola AC, Miot HA. Efficacy of oral Polypodium leucotomos, colchicine cream and ingenol mebutate in the treatment of actinic keratoses and cutaneous field cancerization: a randomized clinical trial. An Bras Dermatol. 2023;98:236–9.
Trabalho realizado no Ambulatório de Dermatologia, Faculdade de Medicina, Universidade Estadual Paulista, Botucatu, SP, Brasil.