A alopecia areata (AA) não tem etiopatogenia bem estabelecida e seu tratamento, principalmente na forma crônica, constitui um desafio.1 O espectro clínico da doença varia de placa única à alopecia total (AAT), que atinge todo o couro cabeludo, ou universal (AAU), quando acomete todos os pelos do corpo. A porcentagem de pelos perdidos é um dos fatores prognósticos inquestionáveis, e pode ser medida pelo escore SALT (severity of alopecia tool).2,3 AAU e AAT são os tipos mais refratários ao tratamento, e sua taxa de repilação espontânea é menor que 10%.4
A difenciprona (DPCP) é um dos tratamentos mais estudados para AA extensa, com aplicação semanal, em geral pelo médico.5 A antralina é uma substância antiga, de uso domiciliar e de menor custo, com poucos estudos sobre seu uso em AA.6–10 Ambas as medicações agem pela indução de eczema sobre a área alopécica: a DPCP provocaria uma dermatite de contato (DC) alérgica, e a antralina, uma DC irritativa.
Assim, pode‐se supor que os resultados dos dois medicamentos sejam similares; porém, não existem estudos que comparem a eficácia da antralina e da DPCP no tratamento de AA. O objetivo deste estudo é comparar eficácia, tolerabilidade e segurança das duas substâncias no tratamento da AA extensa crônica (com mais de um ano de duração).
Trata‐se de ensaio clínico randomizado, controlado, realizado no ambulatório de Tricologia da Dermatologia do Hospital do Servidor Municipal de São Paulo. Após aprovação do comitê de ética (CAAE n° 60888516.1.0000.5442) e assinatura de termo de consentimento, 24 pacientes portadores de AA com mais de um ano de duração, SALT ≥ 50 e com mais de 30 dias sem tratamento foram incluídos e alocados aleatoriamente para o recebimento de DPCP (n=13) (com aumento gradual da dose até a obtenção de eczema leve) ou antralina 2% em vaselina por 30min (n=11). Houve controle intrapaciente por meio da aplicação inicial apenas no hemicrânio direito. A porcentagem de repilação foi calculada por examinador único e cego quanto ao grupo de tratamento por meio de fotos. Por causa das características das medicações, não foi possível que o aplicador ou o paciente fossem cegos quanto à substância utilizada. As avaliações deram‐se aos três meses, ou quando houve repilação inicial, e aos seis meses. O tempo de tratamento proposto foi de 24 semanas. O trabalho foi financiado pelo Fundo de Apoio à Dermatologia da Sociedade Brasileira de Dermatologia (FUNADERM).
Dos 24 pacientes incluídos, três tinham AAT (12,5%), 13 apresentavam AAU (54,2%) e oito AA multifocal extensa (33,3%). Os dados clínicos, demográficos e de repilação encontram‐se na tabela 1. Para a comparação de médias foi utilizado teste‐t de Student para amostras independentes; para a comparação de medianas, empregou‐se teste não paramétrico de Wilcoxon e Mann‐Whitney. Para comparar proporções, foi efetuado teste exato de Fisher. Todas as análises foram feitas considerando intenção de tratamento (ITT) e por protocolo. O nível de significância foi de 5% (p<0,05; teste bicaudal).
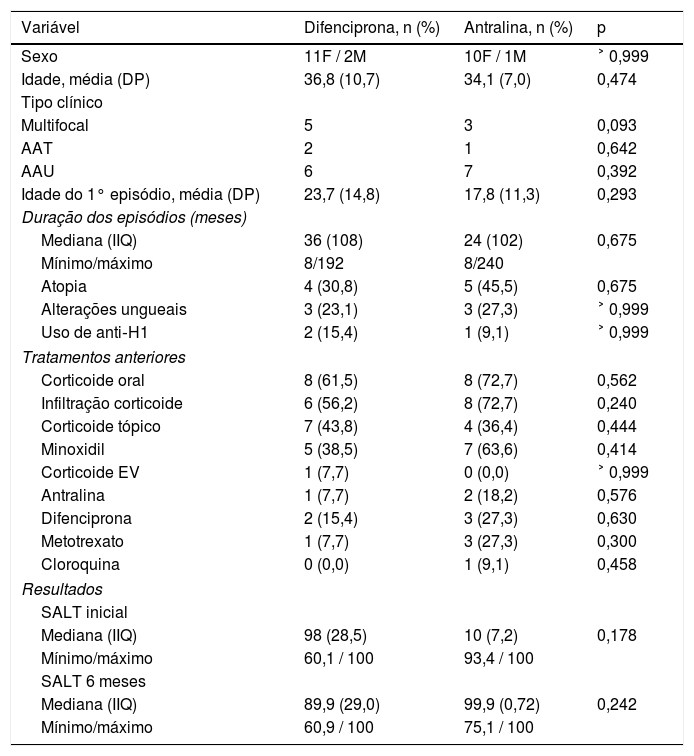
Dados clínicos, epidemiológicos e comparação quanto à repilação dos grupos difenciprona e antralina
| Variável | Difenciprona, n (%) | Antralina, n (%) | p |
|---|---|---|---|
| Sexo | 11F / 2M | 10F / 1M | ˃ 0,999 |
| Idade, média (DP) | 36,8 (10,7) | 34,1 (7,0) | 0,474 |
| Tipo clínico | |||
| Multifocal | 5 | 3 | 0,093 |
| AAT | 2 | 1 | 0,642 |
| AAU | 6 | 7 | 0,392 |
| Idade do 1° episódio, média (DP) | 23,7 (14,8) | 17,8 (11,3) | 0,293 |
| Duração dos episódios (meses) | |||
| Mediana (IIQ) | 36 (108) | 24 (102) | 0,675 |
| Mínimo/máximo | 8/192 | 8/240 | |
| Atopia | 4 (30,8) | 5 (45,5) | 0,675 |
| Alterações ungueais | 3 (23,1) | 3 (27,3) | ˃ 0,999 |
| Uso de anti‐H1 | 2 (15,4) | 1 (9,1) | ˃ 0,999 |
| Tratamentos anteriores | |||
| Corticoide oral | 8 (61,5) | 8 (72,7) | 0,562 |
| Infiltração corticoide | 6 (56,2) | 8 (72,7) | 0,240 |
| Corticoide tópico | 7 (43,8) | 4 (36,4) | 0,444 |
| Minoxidil | 5 (38,5) | 7 (63,6) | 0,414 |
| Corticoide EV | 1 (7,7) | 0 (0,0) | ˃ 0,999 |
| Antralina | 1 (7,7) | 2 (18,2) | 0,576 |
| Difenciprona | 2 (15,4) | 3 (27,3) | 0,630 |
| Metotrexato | 1 (7,7) | 3 (27,3) | 0,300 |
| Cloroquina | 0 (0,0) | 1 (9,1) | 0,458 |
| Resultados | |||
| SALT inicial | |||
| Mediana (IIQ) | 98 (28,5) | 10 (7,2) | 0,178 |
| Mínimo/máximo | 60,1 / 100 | 93,4 / 100 | |
| SALT 6 meses | |||
| Mediana (IIQ) | 89,9 (29,0) | 99,9 (0,72) | 0,242 |
| Mínimo/máximo | 60,9 / 100 | 75,1 / 100 | |
AAT, alopecia areata total; AAU, alopecia areata universal; anti‐H1, anti‐histamínicos; DP, desvio‐padrão; EV, endovenoso; F, feminino; IIQ, intervalo interquartil; M, masculino.
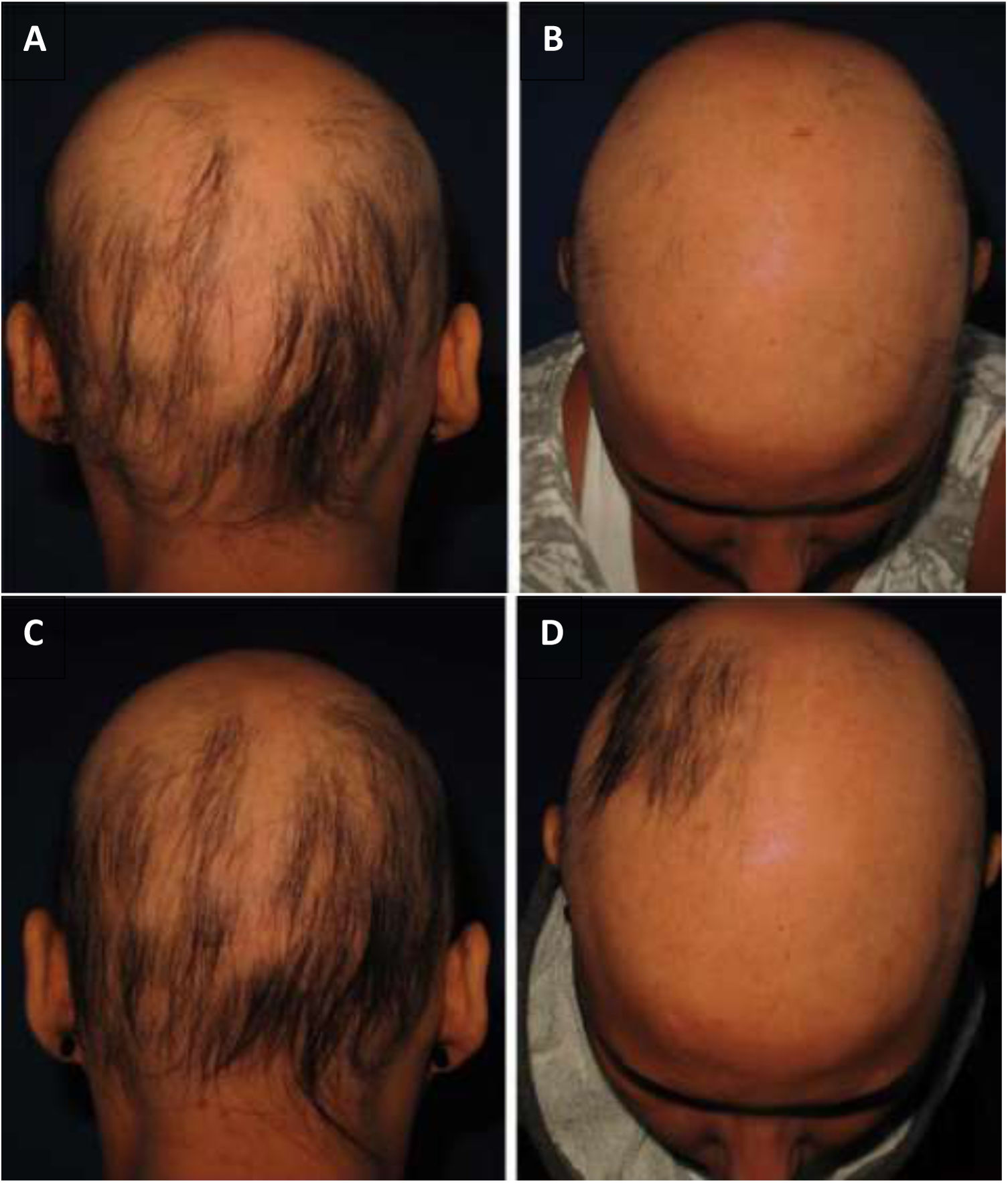
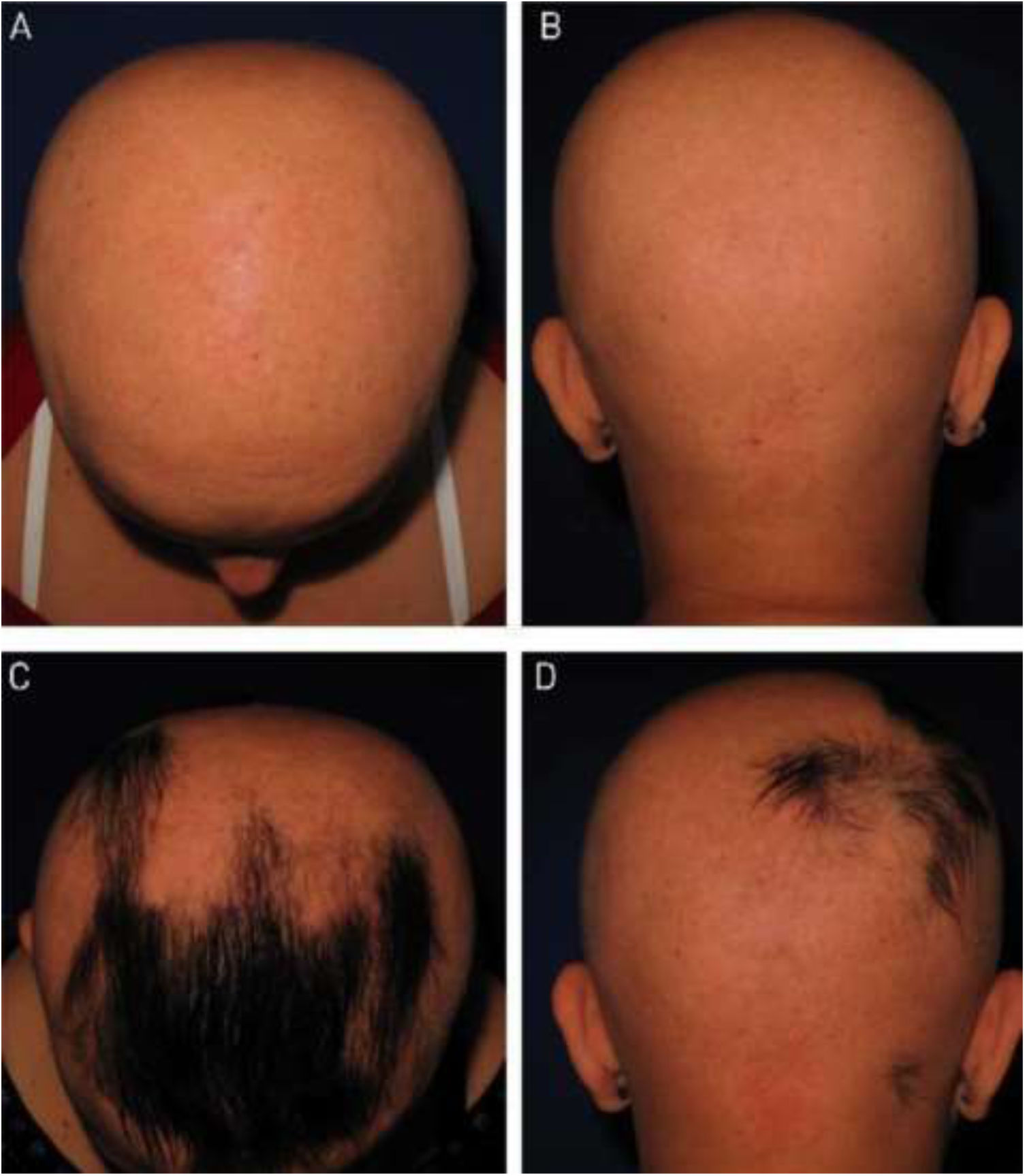
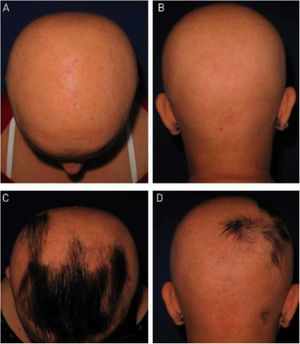
Quanto à repilação, a melhora foi pequena e semelhante nos grupos DPCP e antralina (figs. 1 e 2). O grupo tratado com DPCP apresentou alguma repilação em 38,5% dos casos (5/13), e o grupo antralina em 18,2% (2/11), diferença sem significância estatística (p> 0,05). Nenhum paciente apresentou mais de 75% de repilação neste estudo. Os efeitos colaterais foram semelhantes em ambos os grupos (p=0,121 para três meses e p=0,617 para seis meses).
Recente revisão mostrou 31 estudos utilizando DPCP no tratamento da AA, com 1.638 pacientes tratados, mas nenhum randomizado ou placebo‐controlado. Houve qualquer repilação em 30,7% (22,9%‐39,6%) para pacientes com AAT e AAU, semelhante à taxa encontrada em nosso grupo.5 Nesta revisão, a incidência de eczema grave foi de 30,8%, seguida da linfadenomegalia (25,8%), eczema generalizado (15,8%), hipercromia (12,7%) e sintomas semelhantes à influenza (11,1%).5
Em nossa casuística com DPCP, apenas um paciente apresentou eczema moderado e dois, urticária. No grupo DPCP, houve perda de três pacientes, em sua maioria por problemas em comparecer ao ambulatório semanalmente. Dos 13 pacientes tratados com DPCP, sete finalizaram as 24 semanas de aplicação, com média de 18,4 sessões.
Utilizada em crianças e adultos com AA, existem poucos estudos sobre a antralina, principalmente em adultos.6–10 Özdemir e Balevi (2017) trataram 30 crianças (6,7% com AAU e 3,3% com AAT) com antralina 1% em um hemicrânio por 20‐60 minutos diários. O início da repilação foi notado em média aos três meses de tratamento, e a resposta máxima, aos nove meses. Onze pacientes (36,6%) obtiveram resposta parcial. Nove pacientes (30%) que não responderam ao tratamento em nove meses foram excluídos de análises estatísticas adicionais. Os pacientes que não responderam tinham SALT médio mais alto que aqueles que responderam completa ou parcialmente.8
Quanto à antralina, em nosso estudo dois pacientes (18,2%) apresentaram alguma melhora no SALT. Os 11 apresentaram eritema e prurido, geralmente leves, e apenas um exibiu eczema moderado. A maioria apresentou hiperpigmentação do couro cabeludo, fato esperado e sinal de adesão ao tratamento, que se reverte algumas semanas após a descontinuação da antralina. Neste grupo houve perda de dois pacientes – um por atividade da doença, com piora importante da alopecia, e o outro por problemas pessoais.
Como limitações deste estudo, temos a amostra reduzida, justificada por dificuldades na seleção dos pacientes e pelo orçamento do projeto. A literatura vem trabalhando com amostras pequenas em função das dificuldades mencionadas.5 O tempo de seguimento foi curto, apenas seis meses, muitas vezes por impaciência e ansiedade dos participantes, que solicitavam a troca do tratamento a partir desse período.
A extensão da alopecia dos grupos deste estudo pode justificar a baixa resposta observada. A população estudada é a de pior prognóstico e sem tratamento concomitante, diferente da maioria dos estudos da literatura. Embora não tenhamos conseguido um tempo prolongado de seguimento, este é o primeiro estudo prospectivo que compara a eficácia de DPCP e antralina. Em conclusão, não houve diferença estatística entre as respostas a ambos os tratamentos.
Suporte financeiroFUNADERM ‐ Fundo de Apoio à Dermatologia.
Contribuição dos autoresVanessa Barreto Rocha: Análise estatística; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura.
Priscila Kakizaki: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; obtenção dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito.
Aline Donati: Análise estatística; aprovação da versão final do manuscrito; concepção e planejamento do estudo; análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Carla Jorge Machado: Análise estatística; aprovação da versão final do manuscrito; concepção e planejamento do estudo; análise e interpretação dos dados; participação efetiva na orientação da pesquisa; revisão crítica do manuscrito.
Mario Cezar Pires: Aprovação da versão final do manuscrito; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito.
Leticia Arsie Contin: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; revisão crítica do manuscrito.
Conflito de interessesNenhum.
À farmacêutica Karina de Sá Pedras, da farmácia de manipulação Amphora, pelo fornecimento da antralina abaixo do preço de custo e padronização do material fornecido, sempre o mesmo lote, embalador e tipo de embalagem.
Como citar este artigo: Rocha VB, Kakizaki P, Donati A, Machado CJ, Pires MC, Contin LA. Randomized controlled study comparing the use of diphencyprone and anthralin in the treatment of extensive chronic alopecia areata. An Bras Dermatol. 2021;96:372–6.
Trabalho realizado no Hospital do Servidor Municipal de São Paulo, São Paulo, SP, Brasil.