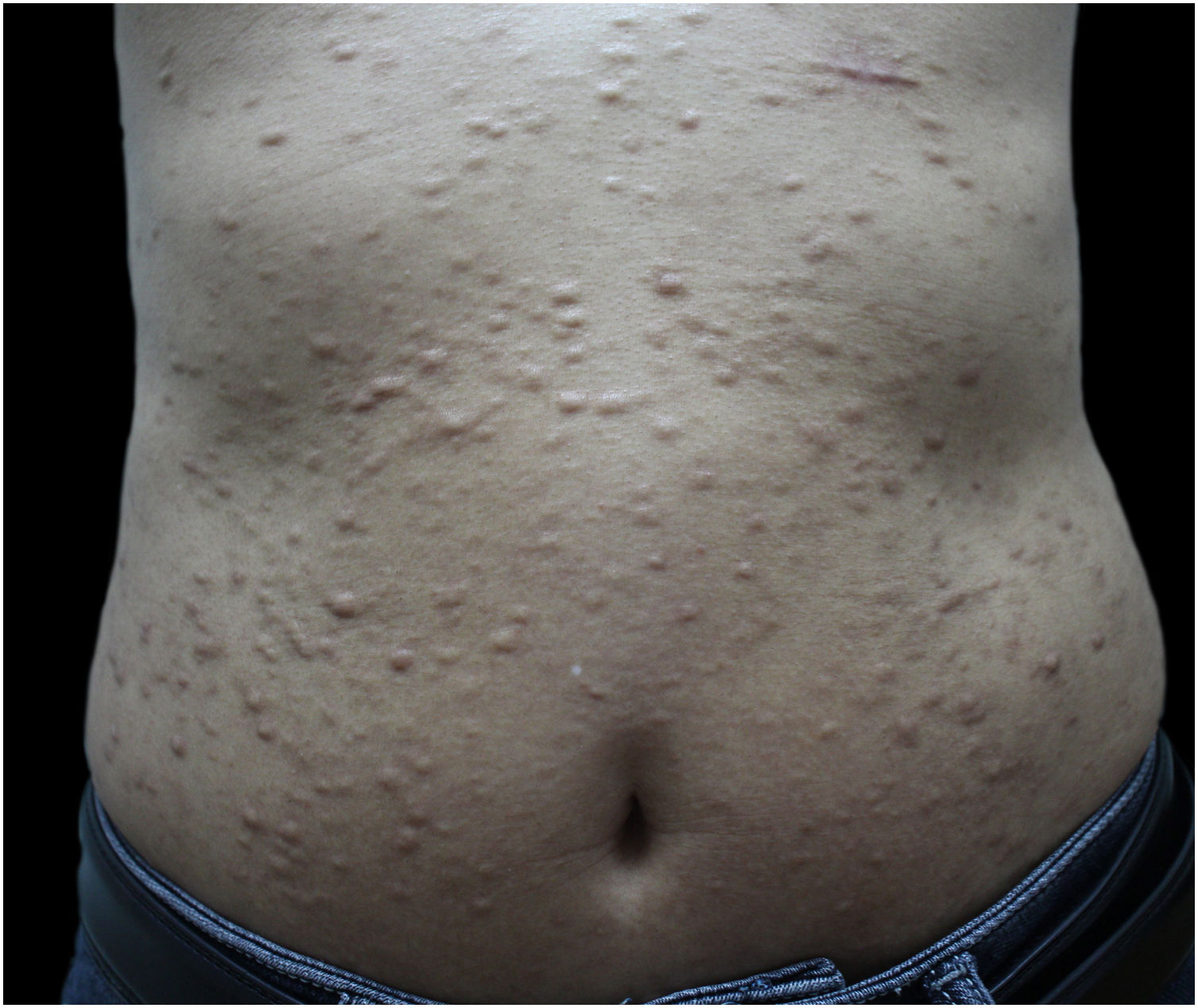
Paciente masculino, de 48 anos, apresentou‐se à clínica dermatológica com história de esclerose sistêmica (ES) há um ano e recebeu dose baixa de prednisona de 20mg/dia por via oral para tratamento da doença. Clinicamente, apresentava‐se com endurecimento e enrijecimento cutâneo difuso, bem como fenômeno de Raynaud, e preenchia os critérios diagnósticos da American College Rheumatology. Há três meses, havia desenvolvido múltiplos nódulos endurecidos e exofíticos no tronco, e membros inferiores e superiores, com preservação da face. As lesões tornaram‐se progressivamente mais endurecidas e numerosas e aumentaram em tamanho. O exame físico mostrou nódulos múltiplos, firmes, elevados e de cor da pele no tórax, abdome e região dorsal, e espalhados pelas extremidades (fig. 1). Os exames laboratoriais revelaram elevada taxa de hemossedimentação (46mm/h). O paciente apresentava anticorpo antinuclear positivo (título 1:640) e anticorpos SCL70 com o componente 3 do complemento diminuído (C3, 0,78g/L), enquanto os títulos de anticorpos anti‐Smith estavam em nível normal. Os exames cardiovascular, respiratório e do esôfago não apresentaram alterações. As funções hepática e renal estavam normais e não havia sinais de crise renal de esclerodermia. O diagnóstico clínico de esclerodermia nodular foi corroborado na histopatologia, que revelou proliferação de miofibroblastos e feixes de colágeno esclerótico e espessado na derme (fig. 2 A,B). Além disso, a coloração de van Gieson mostrou preservação das fibras elásticas, enquanto a coloração violeta cristal foi negativa.
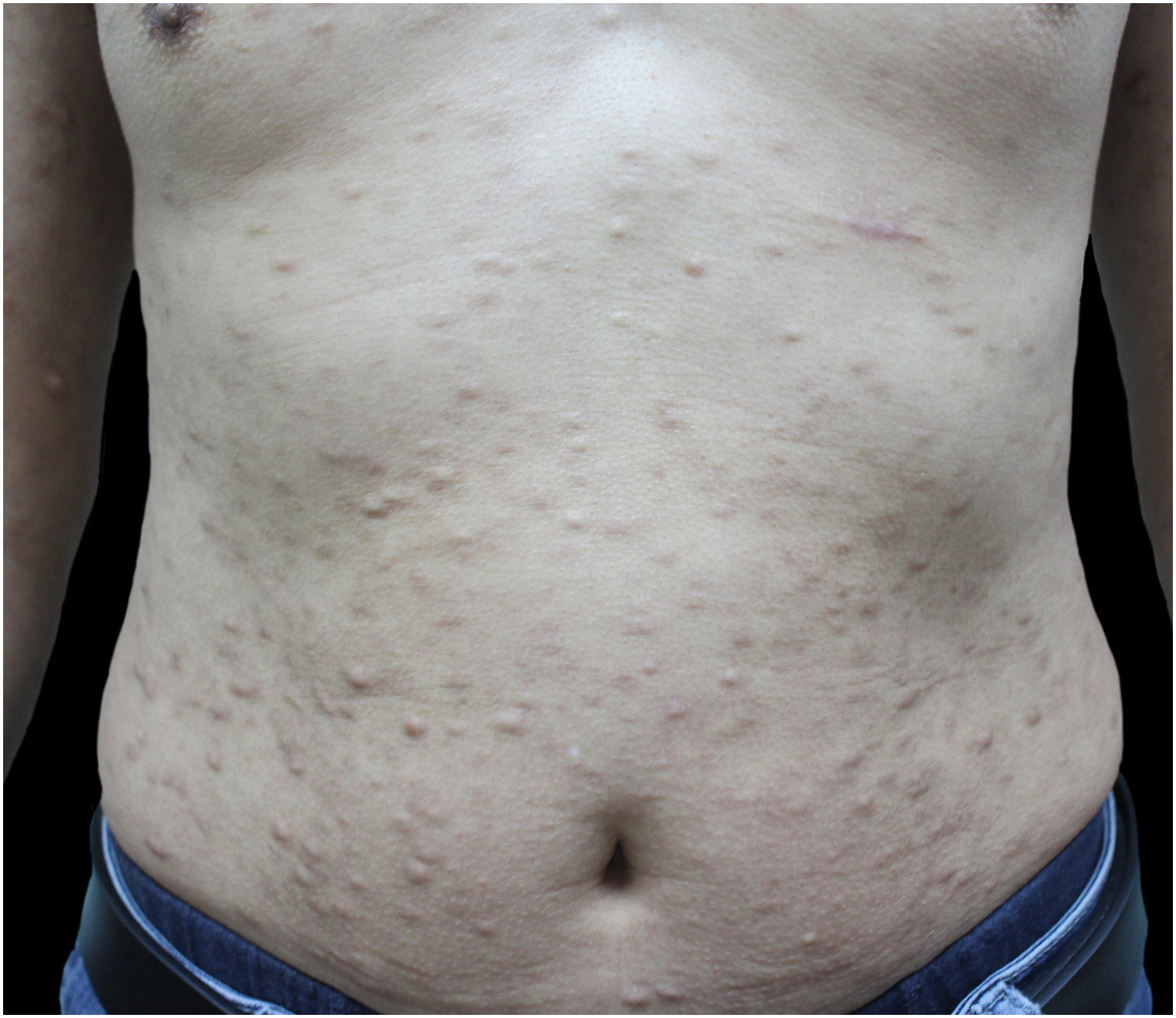
O tratamento inicial com metotrexato na dose de 15mg/semana foi interrompido após três meses, à medida que a doença progredia e novos nódulos surgiam. Subsequentemente, foi iniciado tratamento com micofenolato de mofetil na dosagem de 1g, 2×/dia. Três meses depois, o paciente ainda não apresentava nenhum efeito observável. Assim, o tratamento anterior foi substituído por tofacitinibe. No seguimento ambulatorial, o paciente não desenvolveu novas lesões, enquanto os nódulos preexistentes ficaram menores e menos firmes, com efeitos continuados após oito meses de tratamento com tofacitinibe (fig. 3). O paciente segue monitorado e não apresentou nenhum efeito colateral adverso.
A esclerodermia nodular, também descrita como esclerodermia queloidiana, é variante rara da esclerodermia, relatada pela primeira vez por Addison em 1854.1 Os mecanismos etiológicos subjacentes da esclerodermia nodular ainda estão sendo elucidados. Entretanto, lesões cutâneas são comuns em pacientes com ES progressiva. A via JAK/STAT está envolvida em alguns dos principais mediadores implicados na patogênese da ES: IL‐6, IFN tipos 1 e 2, IL‐4 e IL‐13.2 O inibidor pan‐JAK tofacitinibe tem a capacidade de inibir JAK1, JAK2 e JAK3 e a sinalização downstream de várias citocinas. Evidências anteriores também mostraram que pacientes com ES apresentavam aumento de células B efetoras ativadas por IL‐4 e IL‐13, promovendo fibrose.3
Notavelmente, foi demonstrado que os inibidores de JAK/STAT atenuam a fibrose na pele em diferentes modelos em camundongos.4 O resultado favorável do paciente descrito no presente relato sugere que o tofacitinibe pode ser opção eficaz para o tratamento da esclerodermia nodular. Embora o presente estudo tenha sido consistente com outros, são recomendadas mais investigações para elucidar o papel dos inibidores de JAK na esclerodermia nodular. O tratamento off‐label domina o manejo clínico de doenças raras. No presente artigo, é apresentada a utilização do tofacitinibe na esclerodermia nodular com seguimento em longo prazo.
Suporte financeiroNenhum.
Contribuição dos autoresKai‐Yi Zhou: Obtenção, análise e interpretação dos dados; elaboração e redação do manuscrito; revisão crítica da literatura.
Qian Ye: Obtenção, análise e interpretação dos dados; elaboração e redação do manuscrito; revisão crítica da literatura.
Sheng Fang: Concepção e planejamento do estudo; edição e aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Zhou K‐Y, Ye Q, Fang S. Nodular scleroderma partially controlled with tofacitinib. An Bras Dermatol. 2024;99:989–91.



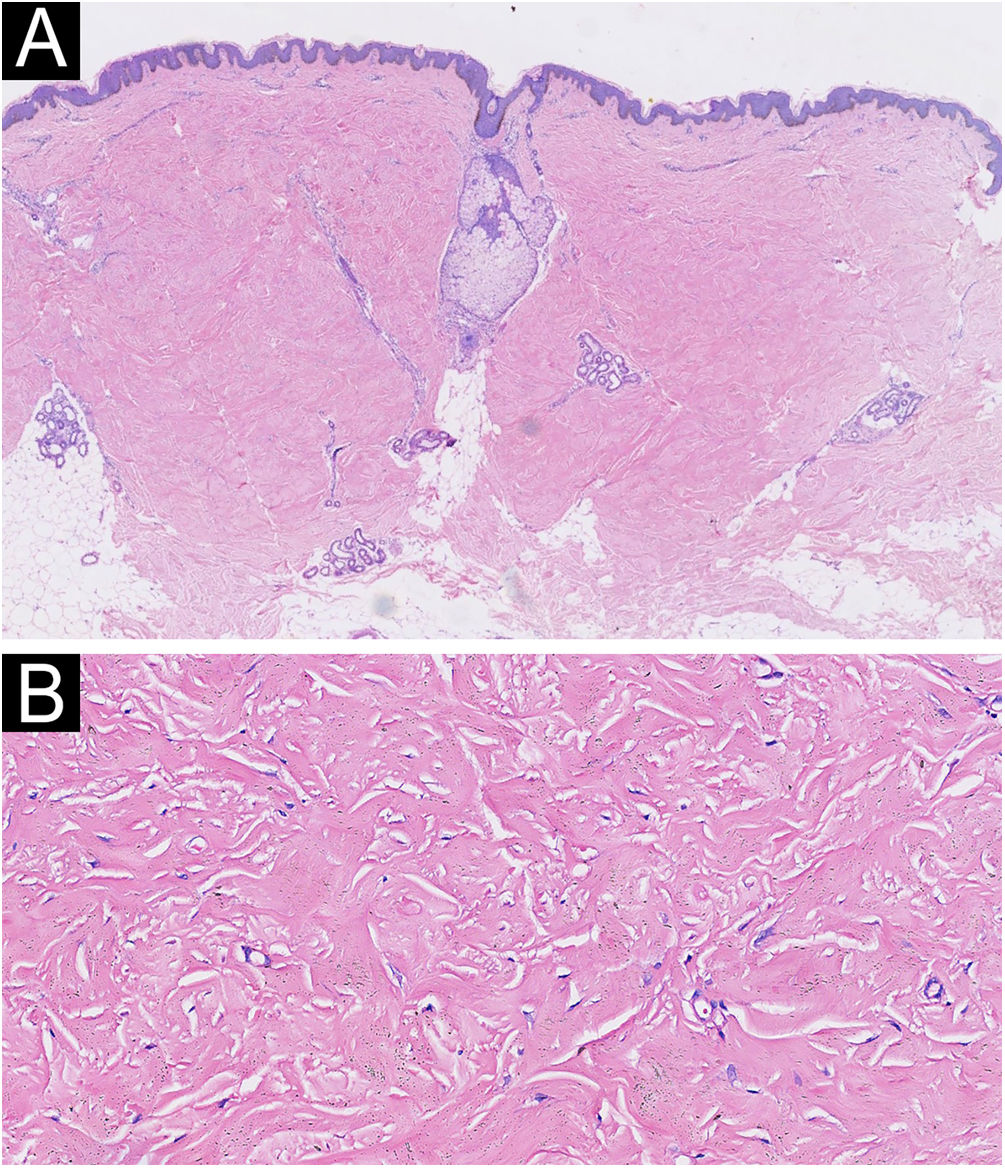

![A histopatologia revelou proliferação de miofibroblastos e feixes de colágeno esclerótico e espessado na derme (Hematoxilina & eosina, 20×[A] e 200×[B]). A histopatologia revelou proliferação de miofibroblastos e feixes de colágeno esclerótico e espessado na derme (Hematoxilina & eosina, 20×[A] e 200×[B]).](https://static.elsevier.es/multimedia/26662752/0000009900000006/v1_202410301154/S2666275224001759/v1_202410301154/pt/main.assets/thumbnail/gr2.jpeg?xkr=ue/ImdikoIMrsJoerZ+w99UWGL/RPJZyNYV9edvxfE4=)

