Os autores apresentam um caso de desenvolvimento de psoríase pustulosa generalizada (PPG) após vacinação contra COVID‐19 em paciente com psoríase vulgar.
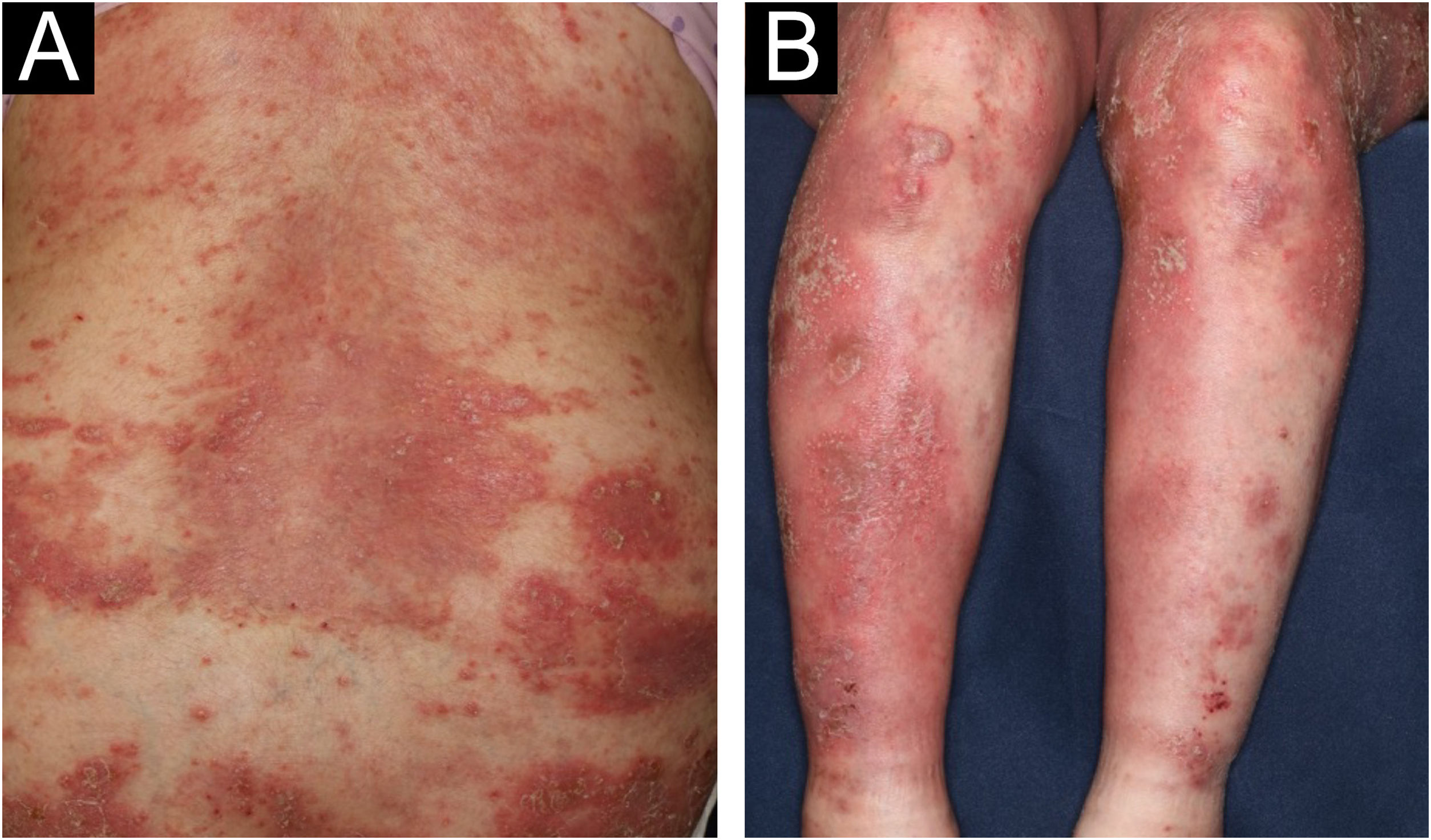
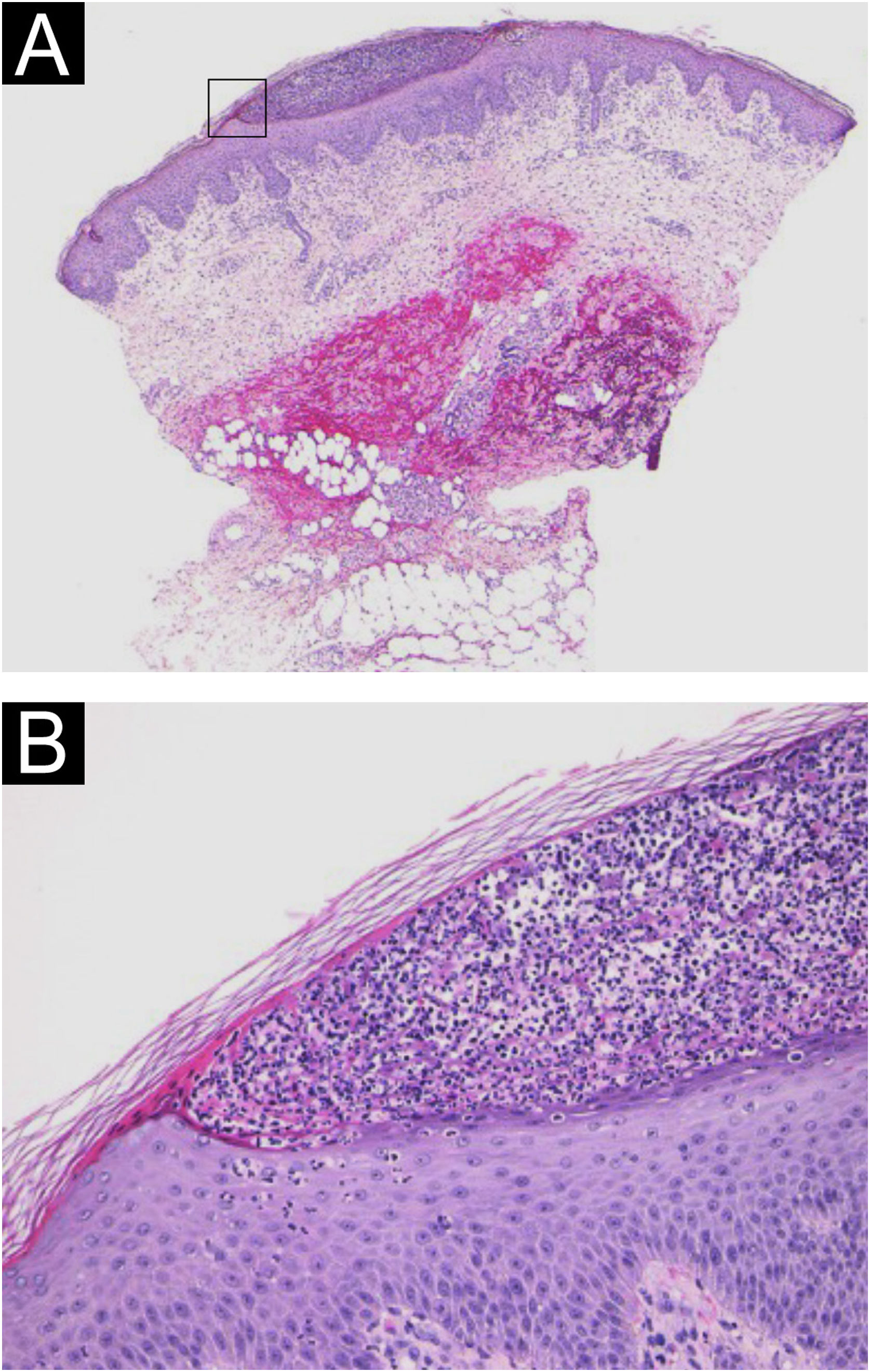
Paciente do sexo feminino, de 64 anos, foi encaminhada ao Departamento de Dermatologia com queixa de febre alta e eritema com pústulas superficiais por todo o corpo sete dias após a terceira dose da vacina de RNA mensageiro Moderna/NIAID contra COVID‐19 (mRNA‐CV). A paciente havia recebido a primeira e a segunda doses da mRNA‐CV da Pfizer/BioNTech. Ela havia desenvolvido psoríase vulgar (PV) cerca de um ano e meio antes, quando foi tratada com apremilaste oral e hidrato de calcipotriol tópico ambulatorialmente com controle da doença. Na consulta inicial, o exame físico revelou múltiplas áreas eritematosas e pequenas pústulas com escamas no tronco e nas extremidades, e edema proeminente na parte inferior das pernas, bilateralmente (fig. 1). Foi realizada biopsia de pele da área de eritema com pústulas na coxa esquerda. A histopatologia mostrou acúmulo subcórneo de neutrófilos e pequenas pústulas multiloculares com espongiose (pústula espongiforme de Kogoj; fig. 2). O exame de sangue mostrou que o nível de proteína‐C reativa estava elevado (7,80mg/dL); os leucócitos estavam normais. Não foram observadas disfunções hepática e renal. A paciente foi tratada com secuquinumabe, resultando em melhora significante da erupção cutânea após dois meses.
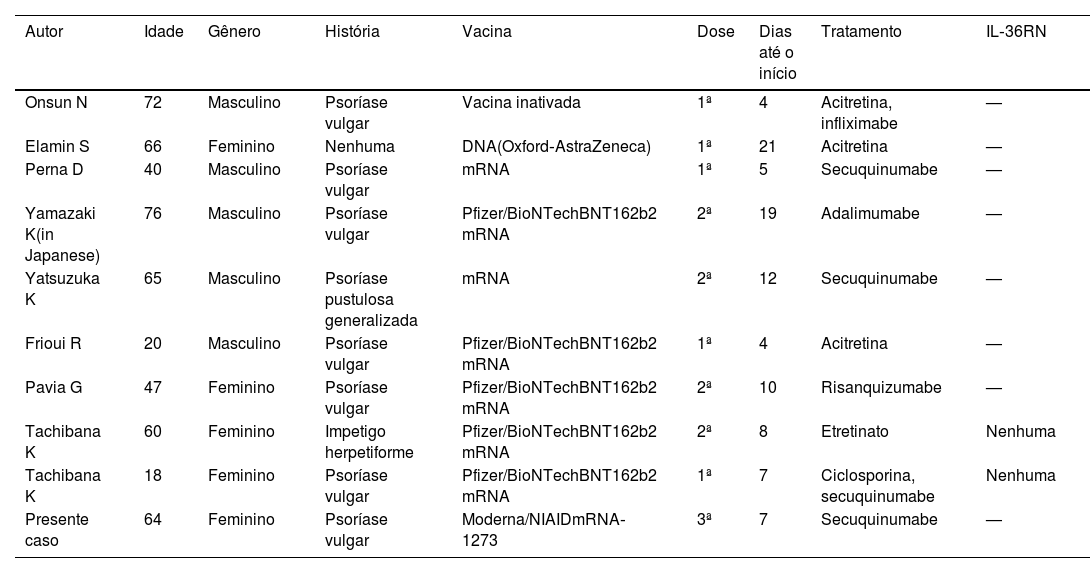
Nos últimos anos, houve vários relatos de PPG após vacinação com mRNA‐CV.1‐8 Que seja de conhecimento dos autores, nove casos foram relatados (tabela 1). A média de idade foi de 52 anos, e a proporção entre homens e mulheres foi de 5:4. Sete dos nove pacientes tinham história de psoríase, enquanto dois pacientes desenvolveram PPG de novo. A duração desde a vacinação até o início dos sintomas variou de quatro a 21 dias. Vacinas de mRNA foram usadas em sete de nove casos (em cinco casos vacinas Pfizer). A maioria dos pacientes desenvolveu lesões pustulosas após a primeira ou segunda dose. Acitretina (n=3), etretinato (n=1), ciclosporina (n=1) e medicamentos biológicos (n=6) foram utilizados no tratamento (com sobreposição). Em relação aos biológicos, foram utilizados secuquinumabe (n=3), infliximabe (n=1), adalimumabe (n=1) e risanquizumabe (n=1). Dois dos nove pacientes realizaram análise de sequenciamento de DNA genômico derivado de sangue periférico, que não revelou mutações genéticas em regiões codificantes inteiras de IL36RN.8 No presente caso, o IL36RN não foi investigado.
Casos de psoríase pustulosa generalizada após aplicação de vacina de mRNA contra o coronavírus
| Autor | Idade | Gênero | História | Vacina | Dose | Dias até o início | Tratamento | IL‐36RN |
|---|---|---|---|---|---|---|---|---|
| Onsun N | 72 | Masculino | Psoríase vulgar | Vacina inativada | 1ª | 4 | Acitretina, infliximabe | — |
| Elamin S | 66 | Feminino | Nenhuma | DNA(Oxford‐AstraZeneca) | 1ª | 21 | Acitretina | — |
| Perna D | 40 | Masculino | Psoríase vulgar | mRNA | 1ª | 5 | Secuquinumabe | — |
| Yamazaki K(in Japanese) | 76 | Masculino | Psoríase vulgar | Pfizer/BioNTechBNT162b2 mRNA | 2ª | 19 | Adalimumabe | — |
| Yatsuzuka K | 65 | Masculino | Psoríase pustulosa generalizada | mRNA | 2ª | 12 | Secuquinumabe | — |
| Frioui R | 20 | Masculino | Psoríase vulgar | Pfizer/BioNTechBNT162b2 mRNA | 1ª | 4 | Acitretina | — |
| Pavia G | 47 | Feminino | Psoríase vulgar | Pfizer/BioNTechBNT162b2 mRNA | 2ª | 10 | Risanquizumabe | — |
| Tachibana K | 60 | Feminino | Impetigo herpetiforme | Pfizer/BioNTechBNT162b2 mRNA | 2ª | 8 | Etretinato | Nenhuma |
| Tachibana K | 18 | Feminino | Psoríase vulgar | Pfizer/BioNTechBNT162b2 mRNA | 1ª | 7 | Ciclosporina, secuquinumabe | Nenhuma |
| Presente caso | 64 | Feminino | Psoríase vulgar | Moderna/NIAIDmRNA‐1273 | 3ª | 7 | Secuquinumabe | — |
Vários mecanismos foram propostos para exacerbação da psoríase pela vacinação contra COVID‐19. Um deles é o mecanismo que envolve a enzima conversora de angiotensina (ECA). Acredita‐se que a atividade da ECA aumente e cause uma tempestade de citocinas inflamatórias pela vacinação contra a COVID‐19.9 Outro mecanismo é a ativação da via do receptor Toll‐like (TLR). Farkas et al.10 descobriram que as vacinas podem ativar células dendríticas mieloides dérmicas que participam da cascata inflamatória da psoríase. As células dendríticas diferenciam as células T em células Th1 e Th17, liberando mediadores inflamatórios e, em seguida, desencadeiam a liberação downstream de citocinas. Acredita‐se que essas citocinas inflamatórias estejam envolvidas na exacerbação da psoríase,1 mas são necessários mais estudos para esclarecer os mecanismos de indução de PPG pela vacinação contra COVID‐19.
Suporte financeiroNenhum.
Contribuição dos autoresMisaki Kusano: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; concepção e planejamento do estudo; manejo dos casos estudados; revisão crítica do manuscrito; elaboração e redação do manuscrito.
Ryuto Mukaiyama: Aprovação da versão final do manuscrito; revisão crítica da literatura; revisão crítica do manuscrito; elaboração e redação do manuscrito.
Toshiyuki Yamamoto: Aprovação da versão final do manuscrito; revisão crítica da literatura; obtenção, análise e interpretação dos dados; concepção e planejamento do estudo; revisão crítica do manuscrito; elaboração e redação do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Kusano M, Mukaiyama R, Yamamoto T. A case of generalized pustular psoriasis following Moderna/NIAID COVID‐19 vaccination successfully treated with secukinumab. An Bras Dermatol. 2024;99:773–5.
Trabalho realizado no Fukushima Medical University, Fukushima, Japão.