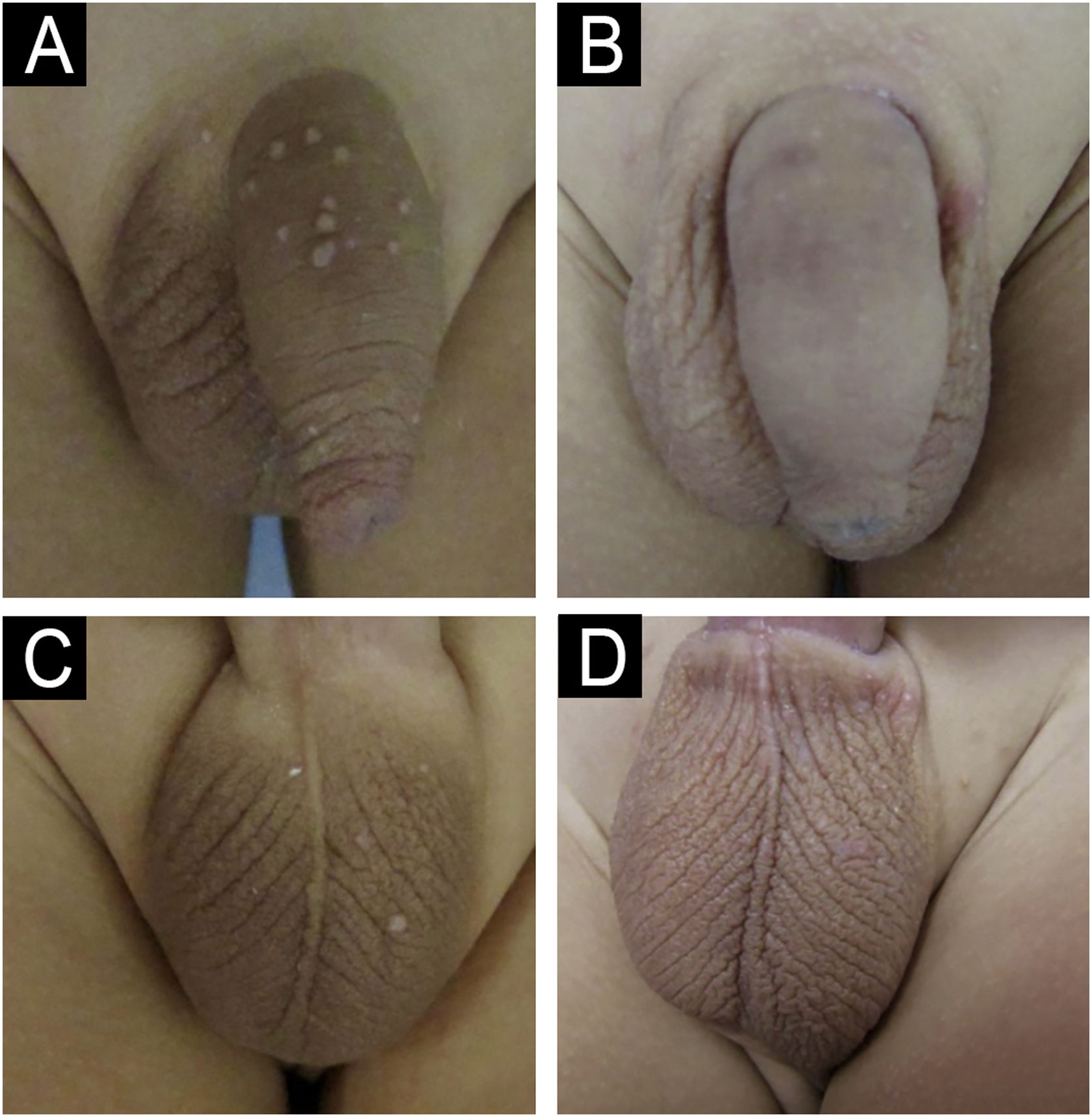
Existem diversas opções terapêuticas para o molusco contagioso (MC), incluindo tratamentos físicos (eletrocauterização, curetagem, crioterapia), químicos (hidróxido de potássio, imiquimode [IMQ]) e até mesmo a espera pela resolução espontânea.1–4 O IMQ é imunomodulador tópico que atua estimulando as vias imunes inatas e adaptativas; inicialmente aprovado para o tratamento de verrugas anogenitais, ceratose actínica e carcinoma basocelular superficial. Existem outras indicações off‐label tanto em doenças dermatológicas benignas quanto malignas em virtude de seus potenciais efeitos antivirais, antitumorais e imunorreguladores.5,6
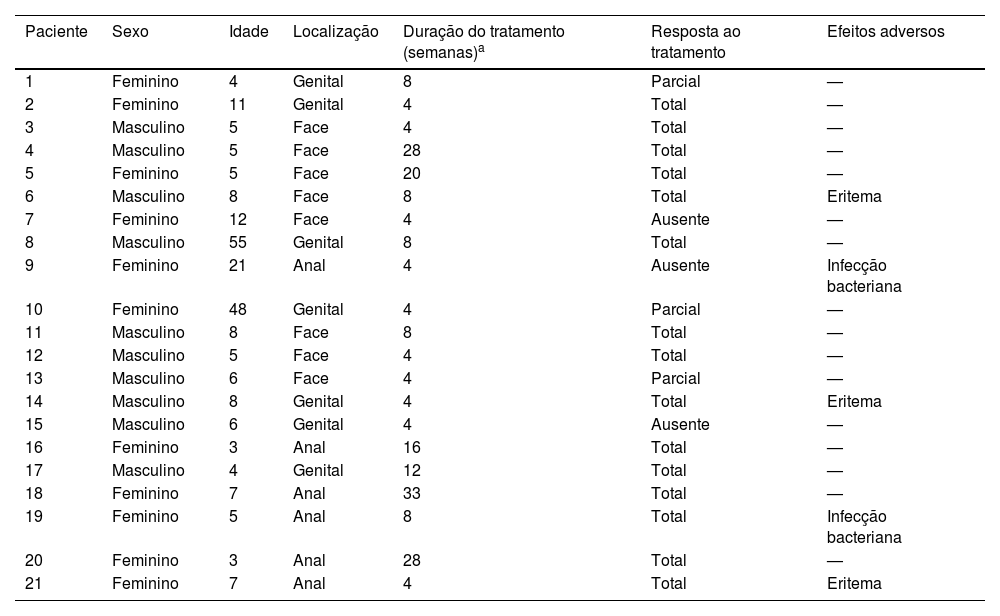
Foi realizado estudo retrospectivo analisando prontuários de pacientes com MC atendidos em uma clínica de dermatologia de hospital terciário público de São Paulo, Brasil, no período de março de 2016 a março de 2024, avaliando: (i) o número de pacientes tratados com IMQ, (ii) resposta terapêutica e (iii) efeitos colaterais apresentados. Dos 1.256 pacientes atendidos em oito anos, o IMQ foi indicado em apenas 21 (tabela 1). A proporção entre os sexos foi semelhante (11 mulheres, 10 homens); apenas três (14,28%) tinham mais de 18 anos. As lesões tratadas localizavam‐se na face (oito; 38,09%) ou na região anogenital (13; 61,91%); todos os pacientes utilizaram dosagem semelhante ao tratamento de verrugas anogenitais (três vezes por semana), por um período de quatro a 33 semanas. Quanto à resposta terapêutica, 15 pacientes apresentaram resolução completa (figs. 1‐3), três apresentaram resposta parcial e outros três não apresentaram resposta. Os pacientes sem resposta usaram o produto por quatro semanas; aqueles com resposta parcial, por quatro a oito semanas; todos os pacientes com resposta completa usaram o produto por oito semanas ou mais.
Características dos 21 pacientes com molusco contagioso tratados com imiquimode
| Paciente | Sexo | Idade | Localização | Duração do tratamento (semanas)a | Resposta ao tratamento | Efeitos adversos |
|---|---|---|---|---|---|---|
| 1 | Feminino | 4 | Genital | 8 | Parcial | — |
| 2 | Feminino | 11 | Genital | 4 | Total | — |
| 3 | Masculino | 5 | Face | 4 | Total | — |
| 4 | Masculino | 5 | Face | 28 | Total | — |
| 5 | Feminino | 5 | Face | 20 | Total | — |
| 6 | Masculino | 8 | Face | 8 | Total | Eritema |
| 7 | Feminino | 12 | Face | 4 | Ausente | — |
| 8 | Masculino | 55 | Genital | 8 | Total | — |
| 9 | Feminino | 21 | Anal | 4 | Ausente | Infecção bacteriana |
| 10 | Feminino | 48 | Genital | 4 | Parcial | — |
| 11 | Masculino | 8 | Face | 8 | Total | — |
| 12 | Masculino | 5 | Face | 4 | Total | — |
| 13 | Masculino | 6 | Face | 4 | Parcial | — |
| 14 | Masculino | 8 | Genital | 4 | Total | Eritema |
| 15 | Masculino | 6 | Genital | 4 | Ausente | — |
| 16 | Feminino | 3 | Anal | 16 | Total | — |
| 17 | Masculino | 4 | Genital | 12 | Total | — |
| 18 | Feminino | 7 | Anal | 33 | Total | — |
| 19 | Feminino | 5 | Anal | 8 | Total | Infecção bacteriana |
| 20 | Feminino | 3 | Anal | 28 | Total | — |
| 21 | Feminino | 7 | Anal | 4 | Total | Eritema |
Dado o número de pacientes atendidos no período analisado, fica claro que o IMQ não é o tratamento de primeira escolha na instituição onde o estudo foi realizado. Um dos motivos é pelo fato de o estudo ter sido realizado em hospital público que não fornece IMQ gratuitamente aos pacientes, e poucos deles têm condições de arcar com o alto custo do medicamento. Outro motivo é pelo medicamento ter sido prescrito apenas para pacientes imunocompetentes e sem comorbidades, característica rara dos atendidos em hospital público terciário. Essa baixa prescrição de IMQ para MC é compatível com dados publicados nos Estados Unidos, onde a taxa de prescrição de IMQ entre 6,4 milhões de consultas para MC foi de apenas 7,0%.7
No entanto, é importante lembrar que a remoção de MC na face ou na região anogenital, baseada em métodos físicos como a curetagem, também é desafiadora. Esses procedimentos podem causar impacto físico e emocional, principalmente em pacientes menores de idade. Assim, uma opção terapêutica tópica domiciliar, como o uso do IMQ, torna‐se valiosa tanto para pacientes quanto para médicos.
O uso do IMQ o tratamento do MC é amplamente discutido na literatura científica, mas ainda sem consenso sobre sua indicação. Estudos prévios apresentam divergências: enquanto alguns autores relatam resultados favoráveis com o uso do IMQ, demonstrando eficácia em casos selecionados,2,3,7 outros questionam a real efetividade do medicamento, afirmando que não existem ensaios clínicos randomizados suficientes para sustentá‐lo como tratamento eficaz para MC, especialmente quando comparado a métodos convencionais, como a curetagem.8–11 Esses estudos contrários argumentam que, em ensaios envolvendo 470 crianças de 2 a 12 anos, a aplicação do IMQ três vezes por semana, por até 16 semanas, não resultou em diferença significante em comparação com os grupos controle, com taxas de resolução completa de 24% (52/217) e 26% (28/106), respectivamente. Observações semelhantes foram feitas em outro estudo, no qual a taxa de resolução foi de 24% (60/253) no grupo tratado, contra 28% (35/126) no grupo controle.4,8–11 No entanto, vale ressaltar que esses estudos não avaliaram a eficácia do IMQ em regiões anatômicas específicas, como a face e a área anogenital, o que pode influenciar as conclusões gerais. No presente estudo, ao focarmos em lesões localizadas em áreas com pele fina, observamos taxa de cura completa de 71,42% (15/21) dos pacientes, com 73,33% (11/15) desses casos alcançando a cura em até 16 semanas.
No entanto, a casuística limitada deve ser levada em consideração, pois o pequeno número de pacientes tratados influencia as taxas de sucesso. Além disso, em quatro casos com resposta positiva após 16 semanas de tratamento é importante considerar a possibilidade de involução espontânea das lesões, um fenômeno observado em MC. Por fim, um dos pacientes necessitou de 28 semanas (sete meses) de tratamento, reforçando a importância do tempo de uso para o sucesso terapêutico.
A escolha criteriosa dos pacientes e das lesões a serem tratadas com IMQ foi fundamental para os resultados positivos observados neste estudo. Foram tratadas apenas lesões localizadas em pequenas áreas da face e região anogenital, onde a pele é mais fina, o que pode ter favorecido a absorção do produto e a ativação do sistema imunológico local, contribuindo para a eficácia do tratamento. Além disso, o perfil dos pacientes selecionados ‐ imunocompetentes e sem comorbidades ‐ também parece ter sido determinante para o sucesso terapêutico, visto que esses pacientes respondem melhor ao estímulo imunológico proporcionado pelo IMQ. Esses fatores podem explicar a taxa de cura completa observada em 71,42% (15/21) dos casos, resultado mais eficaz do que o relatado em estudos anteriores. Farhangian et al.7 também destacam que, embora alguns estudos mostrem eficácia limitada, o uso do IMQ pode ser benéfico em doenças localizadas, especialmente em áreas de pele fina, reforçando os resultados observados no presente estudo. Portanto, a escolha do paciente e da lesão adequada, aliada à aplicação em áreas com características que favorecem a absorção do medicamento, parece ser essencial para o sucesso do tratamento com IMQ no MC.
Em relação à segurança do IMQ, cinco pacientes (23,8%) apresentaram efeitos colaterais leves, como eritema (três casos) e impetigo (dois casos). Todos os efeitos adversos foram rapidamente resolvidos com a suspensão temporária do medicamento e, nos casos de impetiginização, um breve curso de antibioticoterapia tópica foi suficiente para controle. Esses eventos são condizentes com os achados da literatura, que geralmente apontam para perfil de segurança favorável quando utilizado em áreas limitadas e em doses adequadas. Embora raros, eventos adversos mais graves, como leucopenia ou síndrome de Stevens‐Johnson, foram descritos em outros estudos, mas não foram observados neste grupo de pacientes, reforçando a segurança relativa do tratamento em populações selecionadas e bem monitoradas.3,4,12
O tratamento do MC é desafiador. Apesar de ser lesão benigna, é doença infecciosa de fácil transmissão, que causa impacto psicológico nos pacientes e em seus familiares, que buscam uma resolução rápida, eficaz e com poucos efeitos colaterais. Embora o IMQ não seja o tratamento de primeira escolha na prática clínica, é possível que seu uso em pacientes imunocompetentes com MC localizados em regiões onde o epitélio é mais fino traga melhores taxas de cura. É importante ressaltar que, assim como todos os outros tratamentos, o uso do IMQ pode levar a efeitos colaterais, a maioria deles leves e reversíveis.
Suporte financeiroNenhum.
Contribuição dos autoresBruna Cavaleiro de Macedo Souza: Concepção e o desenho do estudo; levantamento dos dados, ou análise e interpretação dos dados; análise estatística; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação final da versão final do manuscrito.
Rebeca Naomi Shida: Concepção e o desenho do estudo; levantamento dos dados, ou análise e interpretação dos dados; análise estatística; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação final da versão final do manuscrito.
John Verrinder Veasey: Concepção e o desenho do estudo; levantamento dos dados, ou análise e interpretação dos dados; análise estatística; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação final da versão final do manuscrito.
Guilherme Camargo Julio Valinoto: Concepção e o desenho do estudo; levantamento dos dados, ou análise e interpretação dos dados; análise estatística; redação do artigo ou revisão crítica do conteúdo intelectual importante; obtenção, análise e interpretação dos dados; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; aprovação final da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Veasey JV, Souza BC, Shida RN, Valinoto GC. Use of imiquimod in 21 patients with molluscum contagiosum: better results in specific areas. An Bras Dermatol. 2025;100:501142.
Trabalho realizado na Clínica de Dermatologia, Hospital da Santa Casa de São Paulo, São Paulo, SP, Brasil.