Micetoma é doença crônica que se inicia com a implantação ou inoculação na pele de microrganismos provenientes do solo e de outras fontes. É dividida em dois tipos, de acordo com a etiologia: eumicetoma, causado por fungos filamentosos, e actinomicetoma, causado por bactérias filamentosas aeróbias.1,2 É considerado doença negligenciada clássica e relacionada à pobreza, por isso a Organização Mundial da Saúde (OMS) incluiu o micetoma no grupo de doenças negligenciadas em 2016.3 O México é o país com mais relatos de micetoma depois do Sudão, embora existam diferenças no perfil micológico.4,5 A simplicidade do diagnóstico da doença contrasta com seu tratamento, especialmente para os eumicetomas, uma vez que os agentes antifúngicos são escassos e caros em uma doença que requer período mínimo de tratamento de um ano. A primeira escolha é o itraconazol oral, com boa resposta em alguns casos, mas as taxas de cura permanecem baixas. A resposta depende de vários fatores, incluindo o tamanho e a extensão do micetoma, o possível envolvimento ósseo e o estado de saúde do paciente.2,3,6 Por isso, novas opções terapêuticas eficazes e com boa relação custo‐benefício devem ser buscadas. Em particular, nos casos que não respondem à terapia com itraconazol, outros tratamentos, como terbinafina isoladamente ou em tratamento combinado, devem ser tentados.7
Todos os casos discutidos no presente relato tiveram diagnóstico confirmado de eumicetoma, com observação de grânulos no exame direto, culturas (ágar Sabouraud‐dextrose), identificação microscópica e molecular por PCR das culturas obtidas e histopatologia de pele, realizados em todos os casos. Foram incluídos no estudo os casos cuja terapia com itraconazol em doses terapêuticas e por períodos prolongados falhou, assim como aqueles que apresentaram efeitos colaterais ou interações com outros medicamentos. As doses de terbinafina variaram de 250 a 750mg diariamente, dependendo da gravidade da doença. Hemograma completo, testes de função hepática, testes de função renal e urinálise foram realizados no início do tratamento e repetidos a cada três meses. O sucesso do tratamento foi avaliado clinicamente e por exame micológico, que incluiu novos exames e culturas para determinar se havia ocorrido cura completa ou melhora parcial.
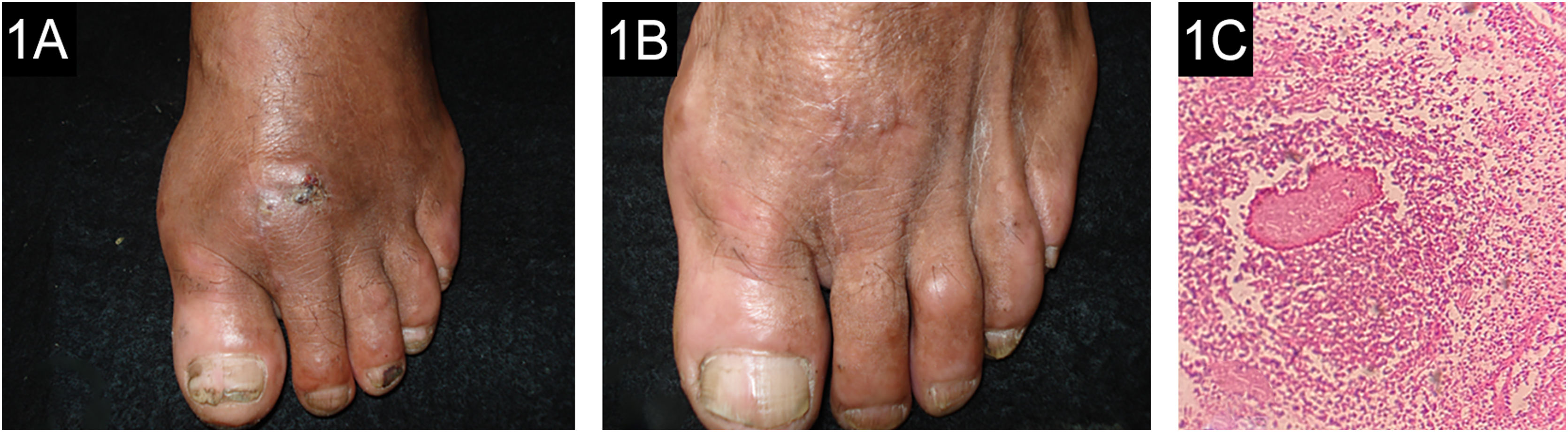
Cinco pacientes foram incluídos no estudo. Os principais dados demográficos, clínicos, micológicos e terapêuticos são apresentados na tabela 1. A cura clínica e micológica sem recidiva foi alcançada em três pacientes (60%) após seguimento de até um ano depois da última dose. Melhora clínica com redução significante do tumor foi observada em dois casos (40%), e ausência de atividade óssea foi notada em um caso (20%; fig. 1).
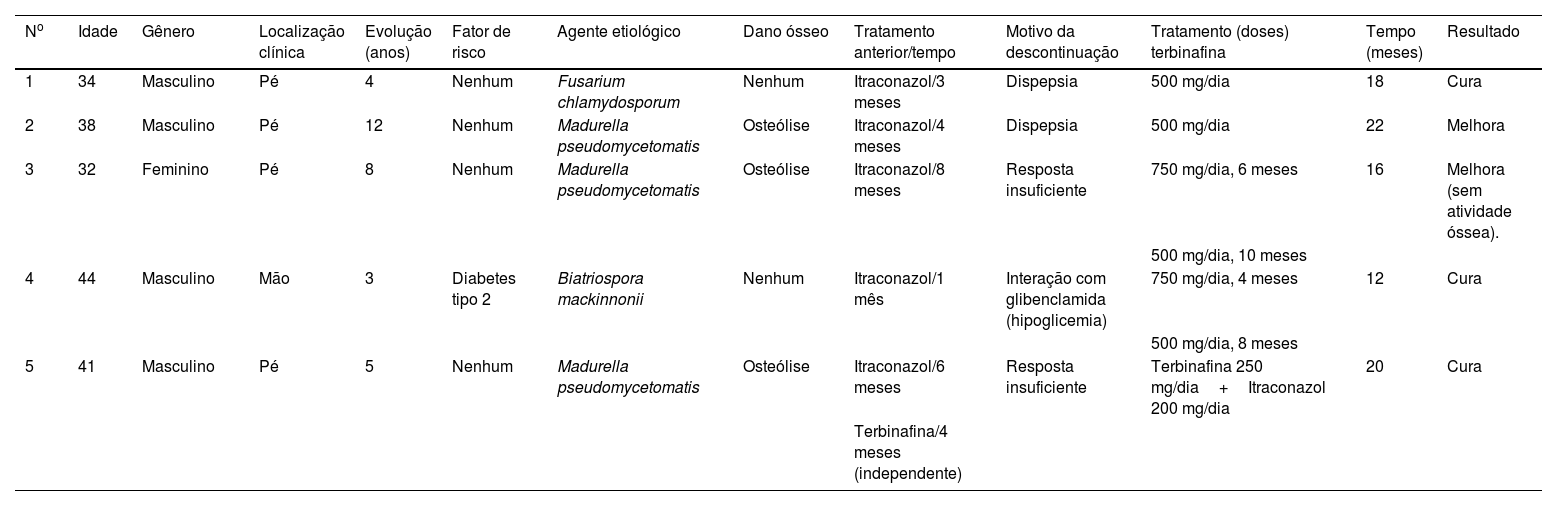
Principais dados demográficos, clínicos, micológicos e terapêuticos dos pacientes com eumicetoma
| No | Idade | Gênero | Localização clínica | Evolução (anos) | Fator de risco | Agente etiológico | Dano ósseo | Tratamento anterior/tempo | Motivo da descontinuação | Tratamento (doses) terbinafina | Tempo (meses) | Resultado |
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 | 34 | Masculino | Pé | 4 | Nenhum | Fusarium chlamydosporum | Nenhum | Itraconazol/3 meses | Dispepsia | 500 mg/dia | 18 | Cura |
| 2 | 38 | Masculino | Pé | 12 | Nenhum | Madurella pseudomycetomatis | Osteólise | Itraconazol/4 meses | Dispepsia | 500 mg/dia | 22 | Melhora |
| 3 | 32 | Feminino | Pé | 8 | Nenhum | Madurella pseudomycetomatis | Osteólise | Itraconazol/8 meses | Resposta insuficiente | 750 mg/dia, 6 meses | 16 | Melhora (sem atividade óssea). |
| 500 mg/dia, 10 meses | ||||||||||||
| 4 | 44 | Masculino | Mão | 3 | Diabetes tipo 2 | Biatriospora mackinnonii | Nenhum | Itraconazol/1 mês | Interação com glibenclamida (hipoglicemia) | 750 mg/dia, 4 meses | 12 | Cura |
| 500 mg/dia, 8 meses | ||||||||||||
| 5 | 41 | Masculino | Pé | 5 | Nenhum | Madurella pseudomycetomatis | Osteólise | Itraconazol/6 meses | Resposta insuficiente | Terbinafina 250 mg/dia+Itraconazol 200 mg/dia | 20 | Cura |
| Terbinafina/4 meses (independente) |
Uma série de cinco casos de eumicetoma tratados com terbinafina foi analisada. Observou‐se resposta favorável, embora a cura clínica e micológica tenha sido alcançada em apenas três casos. Em dois pacientes (40%), o itraconazol foi administrado na dose e no horário corretos mas apresentou resposta insuficiente; decidiu‐se pela mudança de tratamento pela insuficiência da resposta ou por efeitos colaterais e interações medicamentosas (dispepsia e hipoglicemia). É importante ressaltar que a terbinafina não depende do pH para sua absorção e suas interações medicamentosas são mínimas, podendo ser administrada pelo longo tempo necessário para condições crônicas como o micetoma.3,7
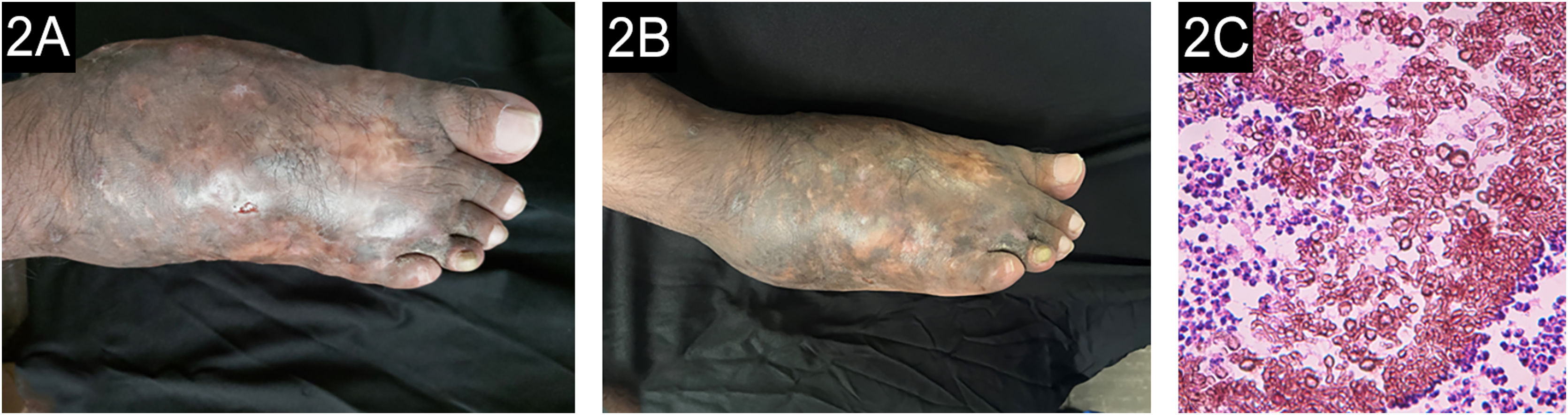
A terbinafina tem atividade moderada contra o micetoma. Nesta série (tabela 1), a cura clínica e micológica foi alcançada em três casos (60%) com o uso de terbinafina, em dois casos como monoterapia (dose de 500mg/dia e no outro caso com 750mg/dia posteriormente reduzida para 500mg/dia), com duração de tratamento de 16 e 18 meses, respectivamente (fig. 2). É importante ressaltar que na presente série três pacientes apresentaram atividade osteolítica e a cura foi alcançada em apenas um deles; anteriormente, foi observada resistência ao tratamento em eumicetoma com envolvimento ósseo.8 N’diaye et al., do Senegal,8 relataram resposta ao tratamento com terbinafina para eumicetoma em 27 pacientes com dose de 1.000mg/dia dividida em duas doses durante 24 a 48 semanas. Outra experiência importante com terbinafina foi relatada no Senegal por Sow et al.,9 que incluíram 68 pacientes com eumicetoma de grânulos pretos também tratados com terbinafina 1.000mg, dividida em duas doses diárias, em combinação com tratamento cirúrgico. Foi alcançada taxa de cura clínica e micológica de 29,4%, melhor que o itraconazol combinado com cirurgia, que foi de 13%. Além dos dois estudos anteriores, outros relatos de casos são esporádicos na literatura.10
O presente estudo constitui uma pequena série de casos que avaliou a eficácia da terbinafina no tratamento do eumicetoma. O tamanho da presente amostra é muito pequeno para que sejam obtidas conclusões, mas indica tratamento alternativo para avaliação em estudos maiores, comparativos e multicêntricos.
Suporte financeiroNenhum
Contribuição dos autoresAlexandro Bonifaz: Contribuiu na elaboração, redação e revisão de todo o manuscrito, foi responsável pela edição do manuscrito, leu e concordou com a versão publicada do manuscrito.
Andrés Tirado‐Sánchez: Contribuiu com a elaboração, redação e revisão de todo o manuscrito, foi responsável pela edição do manuscrito, leu e concordou com a versão publicada do manuscrito.
Denisse Vázquez‐González: Contribuiu com a elaboração, redação e revisão de todo o manuscrito, seguimento e controle clínicos, revisão do manuscrito, leu e concordou com a versão publicada do manuscrito.
Javier Araiza: Contribuiu com a elaboração, redação e revisão de todo o manuscrito, realizou os estudos histopatológicos, leu e concordou com a versão publicada do manuscrito.
Luis Miguel Moreno‐López: Contribuiu com a elaboração, redação e revisão de todo o manuscrito, realizou os estudos micológicos e moleculares e revisão do manuscrito, leu e concordou com a versão publicada do manuscrito.
Gloria González: Realizou os estudos histopatológicos, leu e concordou com a versão publicada do manuscrito.
David Chandler: Contribuiu com a elaboração, redação e revisão de todo o manuscrito, foi responsável pela edição do manuscrito, leu e concordou com a versão publicada do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Bonifaz A, Tirado‐Sánchez A, Vázquez‐González D, Araiza J, Moreno‐López LM, González MG, et al. Treatment of eumycetoma with terbinafine alone and in combination with salvage therapy. An Bras Dermatol. 2024;99:983–6.
Trabalho realizado no Serviço de Dermatologia, Hospital General de México “Dr. Eduardo Liceaga”, Cidade do México, México.