O imatinibe é o tratamento sistêmico padrão de primeira linha para leucemia mieloide crônica e tumor estromal gastrintestinal (GIST, do inglês gastrointestinal stromal tumor), tendo como alvo as tirosina‐quinases BCR‐ABL e c‐KIT, respectivamente. As erupções cutâneas induzidas por imatinibe podem ser variadas, mas os casos de psoríase/erupções psoriasiformes são raros. Relata‐se aqui um desses casos juntamente com a revisão da literatura.
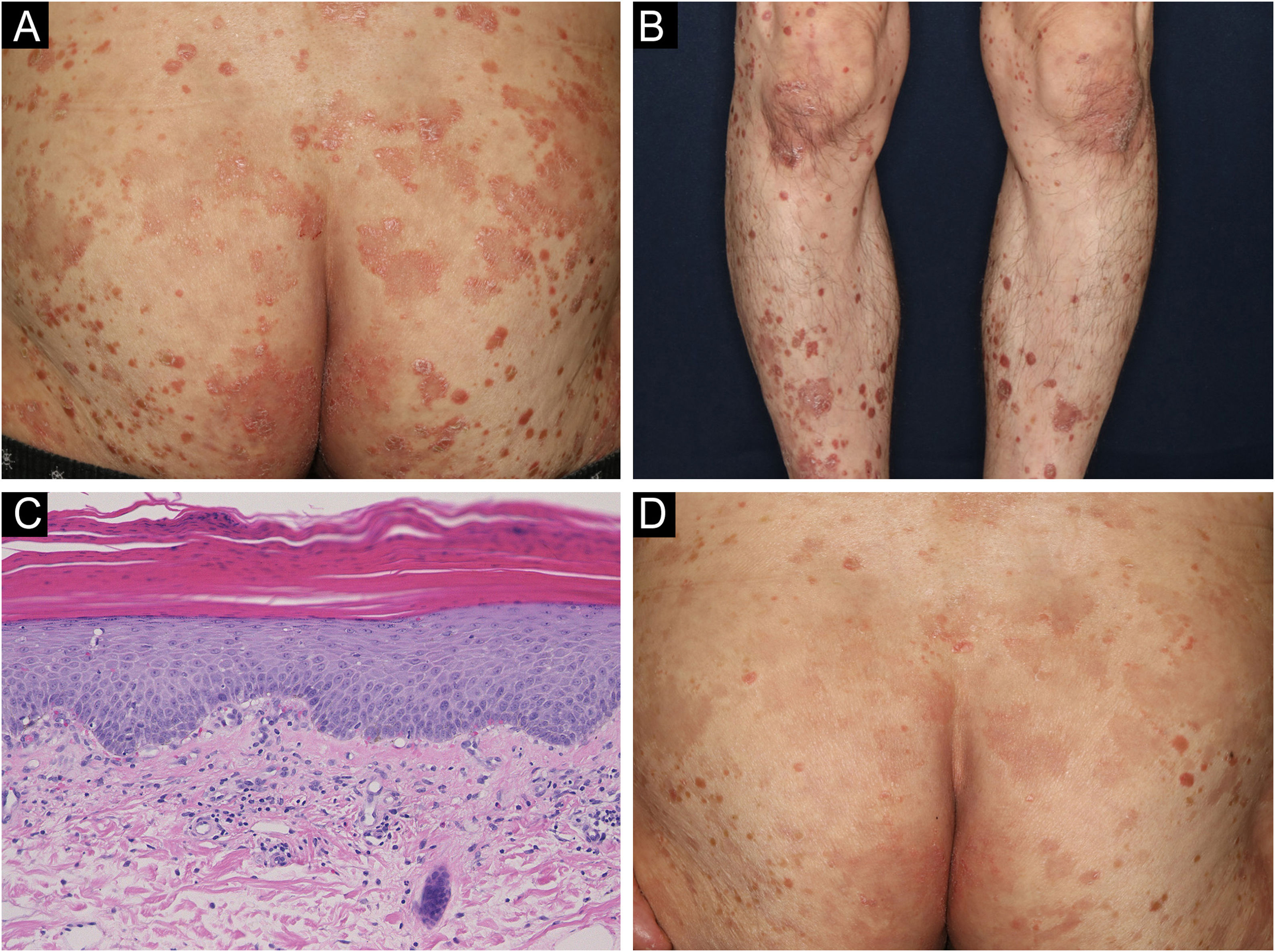
Paciente masculino, de 69 anos, foi encaminhado ao Departamento de Dermatologia com erupção psoriasiforme. Ele havia sido tratado com imatinibe para GIST nos últimos dois anos. Dois meses após o início do tratamento com imatinibe na dose de 400mg/dia, apareceu a erupção cutânea. O exame físico revelou pápulas vermelhas com descamação, medindo de 2 a 4mm no tronco e membros. Além disso, na região glútea havia lesões eritêmato‐descamativas semelhantes à psoríase (fig. 1A). A biopsia de pele foi realizada em lesão eritêmato‐descamativa na perna (fig. 1B). A histopatologia revelou pequena proliferação epidérmica com paraceratose e dilatação de capilares na derme papilar, com infiltrado perivascular de células mononucleares, contendo eosinófilos (fig. 1C). O exame de sangue revelou que os eosinófilos do paciente estavam elevados entre 10% e 15%. Com base na evolução da doença, foi realizado o diagnóstico de erupção medicamentosa causada pelo imatinibe. O tratamento foi iniciado com anti‐histamínico oral e corticosteroides tópicos, e a erupção cutânea melhorou (fig. 1D). Durante o período de tratamento, o imatinibe foi continuado sem redução da dose.
(A) Aspecto clínico do paciente. Lesões psoriasiformes na região glútea. (B) Lesões semelhantes na parte inferior das pernas. (C) Histopatologia com leve paraceratose e epiderme retificada. Infiltração de células inflamatórias perivasculares na derme superficial, acompanhada de extravasamento de hemácias. As células inflamatórias eram eosinófilos, bem como linfócitos e histiócitos (Hematoxilina & eosina, 200×). (D) Resposta parcial ao tratamento.
Reações cutâneas são os efeitos colaterais não hematológicos mais comumente relatados, ocorrendo em 9,5% a 69% dos pacientes.1 Erupções maculopapulares ou eritematosas, edema e edema periorbital são comumente observados. Também foram relatadas erupções medicamentosas graves, como síndrome de Stevens‐Johnson e necrólise epidérmica tóxica. O imatinibe potencialmente afeta diretamente as células do sistema imunológico, e vários casos mostraram melhora da psoríase após a introdução do medicamento.2,3 Por outro lado, raramente foram relatados exacerbação da psoríase ou desenvolvimento de novo de erupção cutânea psoriasiforme. Como mecanismo patogenético, foi relatado que o tratamento com imatinibe reduziu as células T reguladoras (Tregs) CD4+CD25+FoxP3+e diminuiu a função imunossupressora.4 Portanto, a ativação reduzida de Tregs pelo imatinibe pode contribuir para o desenvolvimento de psoríase ou erupções psoriasiformes. Também foi relatado que as erupções psoriasiformes/psoríase são, em geral, menos acentuadas, em virtude da inibição das células T efetoras pelo imatinibe.2
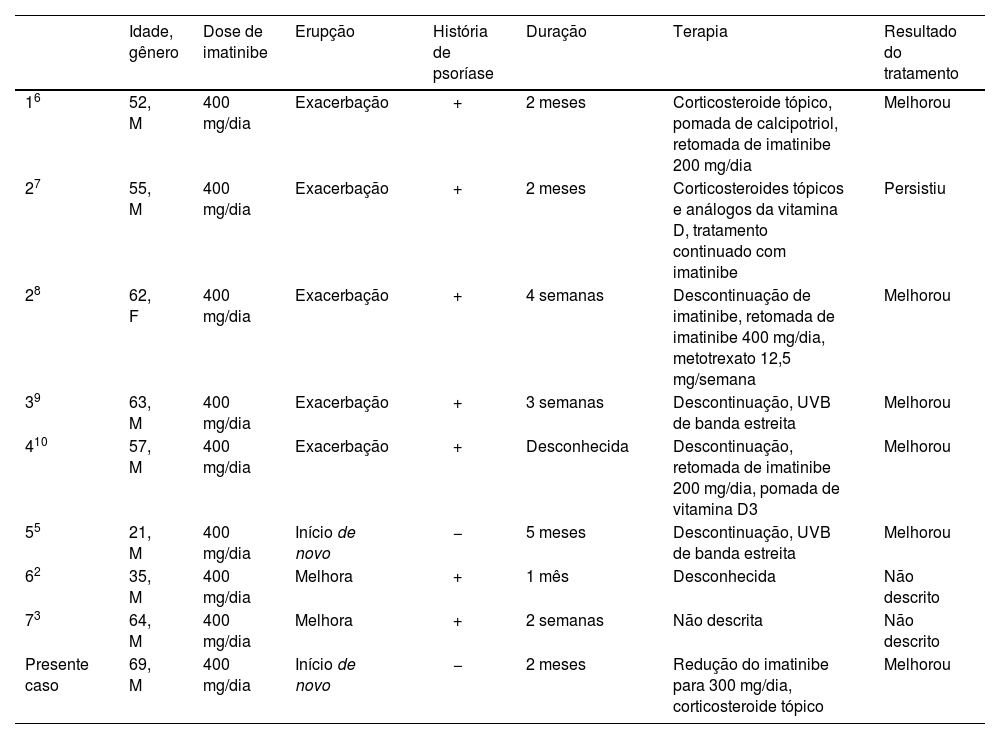
Foi realizada revisão da literatura inglesa no PubMed de 2002 a 2022, utilizando as palavras‐chave “imatinib” e “psoriasis”. Os resultados da pesquisa revelaram oito casos,2,3,5–10 cujos detalhes estão resumidos na tabela 1. O imatinibe causou exacerbação da psoríase, início de novo ou mesmo melhora. A média de idade de ocorrência foi de 51,1 anos, com predomínio do gênero masculino (proporção de 6:2 homens para mulheres). O início da apresentação variou de algumas semanas a vários meses. Havia sete pacientes com psoríase preexistente, e o paciente remanescente apresentava sintomas de psoríase de início recente. Como o presente caso também foi uma erupção psoriasiforme de início recente, o caso anterior do mesmo tipo foi enfocado. Houve diferenças nos achados histopatológicos e no curso da doença. As características histopatológicas no caso anterior incluíram formação de crostas contendo neutrófilos e ausência de camada granulosa.5 Por outro lado, as características histopatológicas no presente caso foram atípicas para psoríase, com pequena paraceratose, sem proliferação epidérmica evidente e ausência de microabscessos neutrofílicos subcórneos. No tratamento do paciente do caso anterior, o medicamento foi substituído,5 mas o paciente do presente caso conseguiu continuar o tratamento com o imatinibe.
Casos de psoríase associados a imatinibe
| Idade, gênero | Dose de imatinibe | Erupção | História de psoríase | Duração | Terapia | Resultado do tratamento | |
|---|---|---|---|---|---|---|---|
| 16 | 52, M | 400 mg/dia | Exacerbação | + | 2 meses | Corticosteroide tópico, pomada de calcipotriol, retomada de imatinibe 200 mg/dia | Melhorou |
| 27 | 55, M | 400 mg/dia | Exacerbação | + | 2 meses | Corticosteroides tópicos e análogos da vitamina D, tratamento continuado com imatinibe | Persistiu |
| 28 | 62, F | 400 mg/dia | Exacerbação | + | 4 semanas | Descontinuação de imatinibe, retomada de imatinibe 400 mg/dia, metotrexato 12,5 mg/semana | Melhorou |
| 39 | 63, M | 400 mg/dia | Exacerbação | + | 3 semanas | Descontinuação, UVB de banda estreita | Melhorou |
| 410 | 57, M | 400 mg/dia | Exacerbação | + | Desconhecida | Descontinuação, retomada de imatinibe 200 mg/dia, pomada de vitamina D3 | Melhorou |
| 55 | 21, M | 400 mg/dia | Início de novo | − | 5 meses | Descontinuação, UVB de banda estreita | Melhorou |
| 62 | 35, M | 400 mg/dia | Melhora | + | 1 mês | Desconhecida | Não descrito |
| 73 | 64, M | 400 mg/dia | Melhora | + | 2 semanas | Não descrita | Não descrito |
| Presente caso | 69, M | 400 mg/dia | Início de novo | − | 2 meses | Redução do imatinibe para 300 mg/dia, corticosteroide tópico | Melhorou |
O presente relato descreveu caso raro de desenvolvimento de novo de erupção psoriasiforme durante tratamento com imatinibe. A erupção psoriasiforme/ psoríase induzida por imatinibe leva vários meses para se desenvolver e parece ser dependente da dose. Consequentemente, acredita‐se que esteja relacionada a efeitos farmacológicos e não com mecanismo alérgico. No presente caso, foram necessários dois meses para que a erupção se desenvolvesse. Entretanto, a erupção cutânea melhorou sem redução da dose de imatinibe. Além disso, os níveis de eosinófilos do paciente estavam elevados após o início do tratamento com imatinibe, mas melhoraram após o término do medicamento, e a infiltração de eosinófilos foi acentuada na histopatologia. Assim, sugere‐se que mecanismo alérgico ou outros efeitos farmacológicos possam estar envolvidos.
Suporte financeiroNenhum.
Contribuição dos autoresYukina Watanabe: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito.
Tomoko Hiraiwa: Aprovação da versão final do manuscrito; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados.
Mikio Ohtsuka: Aprovação da versão final do manuscrito; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados.
Toshiyuki Ymamoto: Revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Conflito de interessesNenhum.