A terapia biológica é tratamento eficaz para psoríase. Entretanto, seu uso a longo prazo traz o risco de efeitos adversos graves e altos custos para o sistema de saúde, o que é particularmente relevante em países latino‐americanos com recursos limitados. Portanto, há interesse científico em explorar a viabilidade da redução gradual da terapia quando a psoríase em baixa atividade ou em remissão clínica.
ObjetivoFornecer recomendações com base em consenso de especialistas para orientar a redução gradual personalizada e eficiente de agentes biológicos em pacientes adultos com psoríase cutânea.
MétodosApós revisão sistemática exaustiva da literatura, o consenso foi desenvolvido usando a metodologia Delphi modificada por um grupo de dermatologistas clínicos latino‐americanos, e metodologia independente. Os tópicos abordados incluiram metas de tratamento, objetivos e estratégias de redução gradual, regimes, monitoramento e falha de redução gradual e considerações de implementação de terapias biológicas em pacientes com psoríase.
ResultadosO painel de especialistas chegou ao consenso sobre cinco princípios gerais e 13 recomendações para redução gradual da terapia biológica na psoríase. Essas recomendações fornecem suporte científico para dermatologistas e profissionais de saúde em relação aos critérios de redução gradual, estratégias e regimes, monitoramento, manejo de falhas e considerações para implementação.
ConclusãoA redução gradual de biológicos parece ser eficaz e segura em pacientes com psoríase com baixa atividade estável ou remissão clínica. Este consenso latino‐americano foi desenvolvido em reconhecimento à necessidade do uso racional e ideal de biológicos, ao mesmo tempo em que individualiza os casos para aplicar as melhores práticas clínicas.
Psoríase é doença inflamatória crônica da pele com forte predisposição genética e características patogênicas autoimunes.1 Estima‐se que afete entre 2% e 3% da população mundial, com maior incidência nos países nórdicos e menor incidência nos países equatoriais.1 Na América Latina e no Caribe, a incidência da psoríase foi estimada em 120 por 100.000 pacientes‐ano entre aqueles que compareceram à consulta dermatológica,2 representando alta carga para o sistema de saúde. A terapia a longo prazo é frequentemente necessária para seu manejo. A escolha do tratamento é determinada pela gravidade da doença, comorbidades e acesso a cuidados médicos.1
Quando os tratamentos de primeira linha, como metotrexato ou ciclosporina, não controlam a doença ou são contraindicados,3 a terapia biológica provou ser eficaz na redução de lesões cutâneas, envolvimento articular, carga inflamatória e comorbidades emergentes.4 Apesar de sua eficácia, o uso prolongado de agentes biológicos está associado a eventos adversos graves e ao alto custo de tratamento. Consequentemente, é de interesse científico analisar se a redução gradual da dose pode diminuir as desvantagens do uso prolongado dessa terapia, uma vez que o estado estável de baixa atividade da doença ou remissão clínica seja alcançado.4
As evidências permanecem inconsistentes em relação à redução gradual da dose de agentes biológicos uma vez que o objetivo terapêutico é alcançado. A redução gradual da dose demonstrou oferecer benefícios potenciais ao reduzir os efeitos colaterais, a carga de injeções repetidas e o custo da terapia biológica.4 Entretanto, faltam diretrizes clínicas para redução gradual da dose de agentes biológicos em pacientes com psoríase, especialmente em países de baixa renda, onde o custo anual desse tipo de terapia pode ser o dobro do dos países europeus.5,6
O objetivo desta iniciativa latino‐americana é fornecer recomendações baseadas em consenso de especialistas para orientar o manejo personalizado e eficiente da redução da dose de agentes biológicos em pacientes adultos com psoríase cutânea, bem como fornecer critérios de elegibilidade, estratégias de redução e resultados a serem avaliados ao decidir realizar essa estratégia, garantindo a eficácia e a segurança do tratamento.
Este documento é destinado a dermatologistas, especialmente aqueles que usam terapia biológica em sua prática clínica, e outros profissionais de saúde e administrativos interessados no assunto no contexto do uso racional dos recursos de saúde. As recomendações devem ser analisadas e implementadas no contexto de cuidados individualizados, adaptados às circunstâncias clínicas individuais e às realidades dos países latino‐americanos.
MetodologiaParticipantesO grupo de consenso foi composto por dermatologistas clínicos que discutiram, definiram e votaram nas recomendações finais. Eles foram selecionados de diferentes países da América Latina (Argentina, Brasil, Chile, Colômbia, Costa Rica, Equador, Guatemala, México, Paraguai, Peru) com base em sua experiência específica com psoríase e disposição para participar de atividades relacionadas. Uma equipe de metodologia independente orientou todo o processo. Todos os participantes preencheram a declaração de interesse, que foi analisada para identificar potenciais conflitos. As informações sobre os participantes e suas declarações de interesse são descritas no Apêndice Suplementar 1.
Escopo e busca de evidênciasA população‐alvo são pessoas com 18 anos ou mais diagnosticadas com psoríase cutânea, excluindo artropatia, que estão sendo tratadas com agentes biológicos e para as quais a redução gradual foi decidida. Para este documento, redução gradual refere‐se à redução na dose ou frequência da quantidade de medicamento biológico administrado ao paciente uma vez que as metas terapêuticas tenham sido alcançadas. Os tópicos abordados incluem metas de tratamento, estratégias de redução gradual, regimes, monitoramento, falha de redução gradual e considerações de implementação.
Revisão sistemática exaustiva da literatura foi realizada para informar as recomendações para redução gradual da terapia biológica em pacientes com psoríase. As buscas foram conduzidas em bancos de dados eletrônicos, incluindo Medline (PubMed), Embase e Ovid, bem como bancos de dados de agências compiladoras e desenvolvedores de diretrizes de prática clínica. As estratégias de busca foram adaptadas para cada banco de dados usando os seguintes termos: “psoriasis” AND “tapering” OR “dose‐adjustment” OR “optimization” AND “biologic”. As buscas iniciais foram conduzidas em maio de 2022 e atualizadas em abril de 2023.
Os critérios de inclusão abrangeram ensaios clínicos, estudos observacionais e revisões sistemáticas da literatura que avaliaram a redução ou suspensão da terapia biológica. Fontes secundárias, como diretrizes de prática clínica, documentos de recomendação baseados em evidências e estudos econômicos, também foram consideradas com base nas necessidades de informação. Documentos produzidos nos últimos sete anos disponíveis como publicações completas, resumos (desde que contivessem informações relevantes), no prelo ou literatura cinzenta foram incluídos. Não houve restrições de idioma. Além disso, as buscas foram conduzidas nos sites de sociedades científicas internacionais relevantes.
Para a seleção das referências identificadas, dois revisores avaliaram os documentos de maneira independente com base nos critérios de elegibilidade. A triagem inicial foi realizada por meio da revisão de títulos e resumos, seguida por uma revisão do texto completo. Desacordos sobre inclusões foram resolvidos por discussão. Para a avaliação da qualidade dos estudos selecionados, a ferramenta de risco de viés Cochrane7 foi usada para ensaios clínicos randomizados (ECRs),7 a escala Newcastle‐Ottawa8 para estudos observacionais e a lista de verificação do Joanna Briggs Institute9 para estudos transversais analíticos. Especificações detalhadas dos processos de busca, seleção e avaliação de qualidade são fornecidas no Material Suplementar 1.
Processo DelphiConsenso formal foi alcançado usando a metodologia Delphi modificada. Com base nas evidências selecionadas, uma lista de declarações foi preparada de acordo com matriz temática. O painel de especialistas revisou o questionário para determinar a necessidade de ajustes, exclusões ou adições. A versão final do questionário incluiu 64 itens organizados em blocos temáticos: critérios para redução gradual (metas e objetivos), estratégias e regimes, seguimento, definição de falha ou recidiva durante a redução gradual, re‐tratamento e outras considerações.
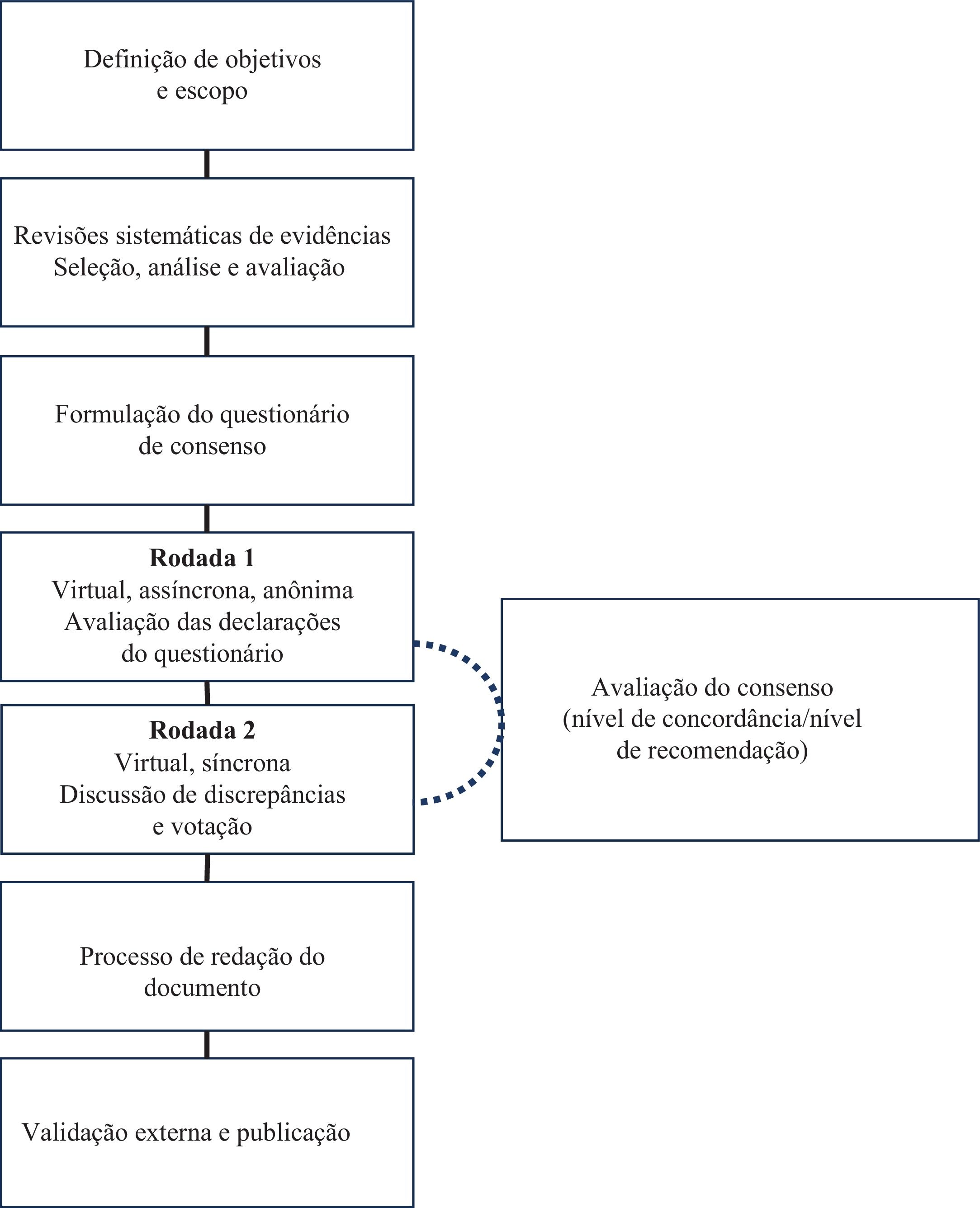
Na primeira rodada, todos os membros do painel preencheram o questionário Delphi de maneira assíncrona e anônima online. O grau de concordância com as declarações foi registrado usando escala Likert de 5 pontos.10 Os julgamentos dos especialistas foram tabulados e apresentados em uma segunda rodada, mantendo a confidencialidade das opiniões de cada membro. Itens sem consenso claro e aspectos controversos foram abordados por meio de deliberações exaustivas e votos síncronos anônimos para chegar ao consenso final. Especificações detalhadas do processo Delphi e resultados são fornecidos no Material Suplementar 2 e ilustrados na figura 1.
Apresentação e interpretação das declarações de consensoNa seção a seguir, as declarações são organizadas por assunto. Quando uma declaração indica que uma ação “deve ser realizada”, isso significa que há evidências sólidas de qualidade moderada ou alta apoiando a eficácia e os benefícios da ação recomendada. Além disso, há consenso entre os participantes do painel de que essa ação deva ser realizada em quase todos os casos. Por outro lado, quando é mencionado que uma ação “poderia ser realizada” ou “poderia ser considerada”, isso implica que a intervenção é apoiada por evidências limitadas ou de baixa qualidade ou carece de aplicabilidade em cenários latino‐americanos. O acordo geral entre o painel é que tais ações podem ser implementadas em circunstâncias selecionadas, considerando as características particulares do paciente e o contexto do tratamento.
Resultados e discussãoO processo de consenso resultou em 13 recomendações para redução gradual da terapia biológica em pacientes com psoríase. O uso de estratégias para reduzir a dose ou estender o intervalo de administração de agentes biológicos em pacientes com psoríase deve ser planejado de acordo com os princípios gerais descritos na tabela 1.
Princípios gerais para redução gradual da terapia biológica na psoríase
| Princípios gerais |
|---|
| A decisão de reduzir gradualmente os agentes biológicos na psoríase deve pesar os benefícios e riscos por meio de uma avaliação individualizada de cada paciente. |
| Cada avaliação do paciente deve ser baseada na gravidade da doença, presença de comorbidades, qualidade de vida e valores e preferências do paciente. |
| As declarações geradas a partir deste consenso servem como recomendações práticas sugeridas sem constituir diretriz de tratamento restritiva para pacientes com psoríase. |
| Particularmente no contexto latino‐americano, é importante considerar as realidades do cenário clínico específico e a disponibilidade de recursos ao implementar as recomendações. |
As características dos estudos selecionados são descritas em detalhes no Apêndice Suplementar 3. Essas evidências incluem oito ensaios clínicos (10 publicações) que avaliaram a eficácia da redução da dose ou prolongamento do intervalo de agentes biológicos.11–20 Esses estudos incluíram entre 111 e 2.546 pacientes que foram tratados por ≥ 12 ou 24 semanas com agentes como adalimumabe, etanercepte, ustequinumabe, brodalumabe, secuquinumabe e guselcumabe. Sete ensaios clínicos (oito publicações)13,16,19–24 avaliaram a descontinuação completa de terapias biológicas como etanercepte, adalimumabe, tildraquizumabe e risanquizumabe (n=3.298 pacientes), com duração do tratamento variando de quatro meses a quase cinco anos antes da descontinuação. Além disso, 22 estudos observacionais investigaram a redução gradual de biológicos em pacientes com psoríase.11,25–45 Esses estudos incluíram tamanhos de amostra variando de 2 a 223 pacientes com tratamentos como adalimumabe, etanercepte, ustequinumabe, infliximabe, guselcumabe, ixequizumabe e secuquinumabe, com durações de tratamento biológico de pelo menos seis meses. Informações de seis fontes secundárias também foram incluídas: documentos de consenso,46–48 diretrizes de prática clínica,49,50 e documentos de recomendação.51
As evidências para cada tópico são descritas abaixo.
Critérios para redução gradualA tabela 2 descreve as declarações de consenso sobre os critérios para redução gradual da terapia com biológicos na psoríase.
Declarações de consenso sobre critérios para redução gradual da terapia biológica na psoríase
| Declarações | Nível de concordância |
|---|---|
| A redução gradual da terapia biológica pode ser considerada em pacientes com psoríase que atingem e mantêm a meta terapêutica de PASI100, PASI/BSA/PGA 0 sustentado, por pelo menos um ano. | 100% |
| A redução gradual da terapia biológica pode ser considerada em pacientes com psoríase que atingem e mantêm PASI absoluto <3 por pelo menos um ano, de acordo com as características clínicas individuais e em consulta com o paciente. | 67%a |
| A redução gradual da terapia biológica pode ser considerada em pacientes com psoríase envolvendo áreas específicas com melhora completa ou quase completa (PGA 0–1) por pelo menos um ano. | 87% |
| A redução gradual da terapia biológica pode ser considerada em pacientes com psoríase leve, boa saúde geral, escore PASI inicial baixo, boa resposta ao tratamento biológico e curto tempo para remissão clínica. | 88% |
| Ao considerar a redução gradual da terapia biológica, a qualidade de vida relacionada à saúde deve ser levada em consideração, pois ela pode se deteriorar significantemente durante a interrupção do tratamento. | 94% |
PASI, Psoriasis Area Severity Index; PGA, avaliação global do médico; ASC, área de superfície corporal.
Estudos publicados mostraram ampla heterogeneidade em escalas e pontos de corte para definir as metas do tratamento e o momento apropriado para reduzir gradualmente a terapia com biológicos. Avanços recentes no desenvolvimento de biológicos motivaram o estabelecimento de alvos terapêuticos mais rigorosos. As evidências consistentemente sugerem estratégias para redução gradual em pacientes com psoríase com resposta completa ou quase completa, medida por PGA 0–1, PASI90 ou PASI ≤ 2.11,14,15,17,18,52–56
O início da redução gradual com metas terapêuticas menos exigentes do que a depuração completa tem sido controverso; entretanto, há evidências de resultados aceitáveis nesses cenários. Nos Estados Unidos, a redução gradual do adalimumabe em pacientes com escore PASI ≥ 50 resultou na manutenção da resposta em 24 semanas.17,55 Estudos observacionais na Espanha e na Europa34,35,37 mostraram respostas clínicas sustentadas na maioria dos pacientes em 6 e 12 meses após a redução gradual da terapia com biológicos, principalmente para adalimumabe e etanercepte, quando eles alcançaram respostas de ≥ PASI50, ≥ PASI75 ou PASI <3 mantidas ao longo do tempo.
As evidências da região incluem um estudo de coorte na Colômbia (n=467) que avaliou a redução gradual de vários biológicos em pacientes com psoríase que alcançaram resposta sustentada, incluindo PASI absoluto <3, e relatou que 88% dos pacientes mantiveram resposta clínica após oito meses de seguimento.43 O painel de consenso discutiu extensivamente a adequação de PASI absoluto <3 como critério para considerar estratégias de redução gradual. No entanto, o acordo unânime não foi possível em virtude da variabilidade dos casos, particularmente na psoríase de localizações especiais. O uso de limiares diferentes da depuração completa em pacientes com psoríase é decisão que deve ser considerada individualmente, de acordo com as manifestações clínicas e em consulta com o paciente.
Em uma pesquisa com dermatologistas em todo o mundo (n=57), quase metade dos médicos usou PASI ≤ 1 ou ≤ 2, ASC ≤ 1 ou ≤ 2 ou PGA ≤ 1 como critérios para iniciar a redução gradual da terapia com biológicos, enquanto 25% indicaram que considerariam a redução da dose apenas em pacientes sem psoríase (PASI/PGA0). Em geral, 64,9% dos pacientes foram submetidos à redução gradual após pelo menos um ano de tratamento.51 Esse achado é consistente com estudos que mostram que a redução gradual da terapia com biológicos geralmente ocorre após a manutenção de metas de tratamento individualizadas por pelo menos 12 meses.
Embora o DLQI raramente seja usado para definir o início da redução gradual da terapia com biológicos,11 fatores associados à melhora da qualidade de vida, como redução dos sintomas relacionados à psoríase e satisfação com o tratamento, são frequentemente considerados. O uso do DLQI é importante como resultado relatado pelo paciente (PROM, do inglês Patient‐Reported Outcome Measures) na avaliação abrangente da psoríase, mas requer orientação para uso ideal e fácil compreensão pelos pacientes. De acordo com o painel, essas limitações impedem que o DLQI seja estabelecido como critério necessário para determinar a redução gradual de biológicos em pacientes com psoríase. Entretanto, a importância da perspectiva do paciente na redução gradual foi documentada na prática clínica dermatológica em todo o mundo.51 Portanto, os médicos são instados a incluir avaliação abrangente dos pacientes e suas circunstâncias como parte da tomada de decisão compartilhada e informada.
Com base nos resultados de vários estudos clínicos anteriores, a descontinuação da terapia com biológicos deve ser considerada se a condição do paciente puder ser mantida em quase remissão por 40 a 52 semanas.50 Nenhuma evidência de longo prazo além de um ano foi apresentada para qualquer produto biológico usando essa estratégia.47,50
Os estudos que incluíram a descontinuação de biológicos como estratégia avaliaram a obtenção de metas usando escores PASI ≥ 50 ou ≥ 75, escores PGA ≤ 2 ou escores sPGA 0–1, mostrando ampla variabilidade.13,16,19–24 Entretanto, os resultados desses estudos apoiam a continuação da terapia com biológicos para manter a eficácia ao longo do tempo, dadas as altas taxas de recidiva e a deterioração da qualidade de vida relacionada à saúde associada à descontinuação da terapia.50
Estratégias e regimes de redução gradualA tabela 3 descreve as declarações de consenso sobre estratégias e regimes de redução gradual para terapia com biológicos na psoríase.
Declarações de consenso sobre estratégias e regimes de redução gradual para terapia biológica na psoríase
| Declarações | Nível de concordância |
|---|---|
| Em pacientes com psoríase que alcançaram e mantiveram resposta terapêutica, a redução gradual da terapia biológica visa manter a meta estabelecida, utilizando a menor dose eficaz possível. | 92% |
| As estratégias de redução gradual incluem aumentar gradualmente os intervalos entre as administrações e reduzir a dose dos medicamentos que permitem isso. | 92% |
| O regime de dosagem biológica deve permitir modificação flexível da dose (aumentando o intervalo ou reduzindo a dose). | 82% |
| O regime de redução deve ser baseado nas indicações de cada medicamento biológico, seus intervalos de dosagem e opções de ajuste de dose (ver tabela 4). | 100% |
As evidências apoiam a possibilidade de redução gradual da terapia biológica em pacientes com psoríase que alcançam e mantêm resposta terapêutica. As estratégias para redução gradual incluem estender os intervalos entre as doses, reduzir a dose mantendo o tratamento contínuo e usar a menor dose eficaz para terapia de manutenção.47 Para algumas moléculas, estudos demonstraram a segurança de reduzir a dose inicial em até 50%, mantendo a eficácia.3 Estender os intervalos de dosagem é a estratégia mais comumente usada em estudos observacionais, com 60% a 100% dos pacientes mantendo respostas clínicas de ≥ PASI75, ≥ PASI90 ou mesmo PASI100 em vários períodos de seguimento, normalmente até um ano.0,1125–70,30,31,33,36,40–42,45
Os diferentes regimes de redução gradual para cada biológico são mostrados na tabela 4.
Regimes de redução gradual para tratamento biológico da psoríase
| Biológico | Dose padrão | Regime inicial de redução gradual | Regime de redução gradual estendidoa |
|---|---|---|---|
| Adalimumabe | 40mg a cada duas semanas | 40mg a cada quatro semanas | Posteriormente, a cada seis semanas |
| Etanercepte | 50mg a cada semana | 50mg a cada 14 dias | Intervalo de até 21 dias |
| Infliximabe | 3 ou 5 mg/kg a cada oito semanas | Não diminua gradualmente em virtude de riscos associados; prefira mudar | |
| Ustequinumabeb | 45mg (≤ 100 kg) a cada 12 semanas | 45mg a cada 16 semanas | Intervalo de até 24 semanas |
| 90mg (> 100 kg) a cada 12 semanas | 90mg a cada 16 semanas | Intervalo de até 24 semanas | |
| 45mg a cada 12 semanas | 45mg a cada 16 semanas | ||
| Secuquinumabec | 300mg a cada quatro semanas | 300mg a cada seis semanas | Intervalo de até oito semanas |
| 150mg a cada quatro semanas | Intervalo de até seis semanas | ||
| Guselcumabe | 100mg a cada oito semanas | 100mg a cada 12 semanas | Intervalo de até 16 semanas |
| Risanquizumabe | 150mg a cada 12 semanas | 150mg a cada 16 semanas | Intervalo de até 24 semanas |
| Certolizumabe pegol | 200mg a cada duas semanas | 200mg a cada quatro semanas | 200mg a cada seis semanas |
| Ixequizumabe | 80mg a cada quatro semanas | 80mg a cada seis semanas | 80mg a cada oito semanas |
Em geral, os intervalos de administração são prolongados dentro de um cronograma fixo, com a possibilidade de ajustes adicionais para aumentar o tempo entre as doses se a estabilidade da doença for mantida após seis meses de terapia. Essas estratégias podem ser adaptadas a diferentes grupos de pacientes. Por exemplo, um estudo que avaliou o impacto de intervalos de tratamento prolongados e intervenção precoce (≤ 2 anos do início dos sintomas) com guselcumabe demonstrou a possibilidade de redução gradual em superrespondedores (PASI0 nas semanas 20 e 28), mantendo medidas favoráveis de PASI e DLQI ao longo do tempo.52
Terapia intermitente foi considerada em pacientes com boa resposta e naqueles com histórico de exacerbações curtas (com duração inferior a seis meses por ano).47 Evidências de estudos clínicos randomizados com períodos de retirada e re‐tratamento descreveram para guselcumabe mediana de tempo para perda de resposta PASI90 de 15,2 semanas (23 semanas após a última dose de guselcumabe)57 e, para ixequizumabe, mediana de tempo para perda de resposta (PASI ≤50) de 20,4 semanas (143 dias).58
Uma revisão sistemática da literatura59 revelou evidências da eficácia e segurança da terapia intermitente com inibidores do fator de necrose tumoral (adalimumabe,16 certolizumabe pegol,60 etanercepte,23,37,56,61,62 infliximabe),24,63 anti‐IL 12/23 (ustequinumabe),64,65 anti‐IL 23 (guselcumabe)57 e anti‐IL 17 (brodalumabe,54,58,66 ixequizumabe58 e secuquinumabe12). Estudos demonstraram que 60% ou mais dos pacientes em terapia intermitente alcançam o controle da doença (como definido em cada estudo) após o re‐tratamento, com os perfis de segurança dos biológicos durante o re‐tratamento sendo os esperados. A exceção a esses achados gerais foi o infliximabe, que teve a menor taxa de obtenção do resultado de eficácia (25% e 38% nos dois grupos de dosagem avaliados) e maior incidência de reações adversas. O painel de consenso considera que a redução gradual do infliximabe pode impor riscos imunológicos aos pacientes; portanto, é preferível mudar para um agente biológico diferente.
Outra estratégia abordada nesses estudos é a interrupção completa do tratamento. Ensaios clínicos com adalimumabe, etanercepte e risanquizumabe relataram tempos mais curtos de manutenção da resposta clínica, com subsequente piora dos escores PASI e da qualidade de vida relacionada à saúde.13,16,19–24
Por fim, a decisão sobre a estratégia de redução gradual e o regime de agentes biológicos no tratamento da psoríase deve ser baseada em avaliação individualizada da situação clínica, considerando a duração do tratamento, obtenção das metas propostas, as características específicas do agente biológico, a satisfação do paciente com o tratamento e os recursos disponíveis para cumprir as recomendações.
Monitoramento e falha durante o redução gradualA tabela 5 descreve as declarações de consenso sobre monitoramento e manejo de falhas durante a redução gradual da terapia com biológicos na psoríase.
Declarações de consenso sobre seguimento e falha da redução gradual da terapia com biológicos na psoríase
| Declarações | Nível de concordância |
|---|---|
| Pacientes submetidos à redução gradual da terapia com biológicos devem ser seguidos a cada três meses, ou antes, se houver piora dos sintomas (de pele ou articulação) ou qualquer outra situação que o justifique. | 100% |
| A identificação de qualquer um dos seguintes critérios em qualquer momento durante o seguimento é considerada falha da estratégia de redução gradual: | |
| PASI absoluto> 3 | 100% |
| PGA/ASC> 1 | 93% |
| Aumento inaceitável da atividade da doença, conforme julgado pelo paciente | 100% |
| Alteração na morfologia (p. ex., psoríase com pústulas) | 93% |
| Reativação ou aparecimento de lesões em áreas específicas | 100% |
| Início de sintomas articulares | 100% |
| No caso de recidiva com PASI ≥ 10 em paciente com psoríase submetido à redução gradual da terapia biológica, a dose de indução do biológico deve ser reiniciada. | 100% |
| No caso de recidiva com PASI <10 em paciente com psoríase submetido à redução gradual da terapia biológica, a dose efetiva imediatamente anterior da terapia biológica deve ser restabelecida. | 100% |
PASI, Psoriasis Area Severity Index; PGA, avaliação global do médico; ASC, área de superfície corporal.
Os tempos de seguimento em ensaios que reduziram a dose ou estenderam o intervalo entre as doses do agente biológico variaram amplamente. Em ensaios clínicos, os pacientes são geralmente avaliados a cada quatro a 12 semanas,14,15,17,18,52–56,67 incluindo aqueles que interromperam o biológico.13,16,19–24 Em estudos observacionais, estratégias de redução gradual foram monitoradas, geralmente a cada 12 a 16 semanas ou em intervalos cada vez maiores, dependendo do tempo de interrupção do biológico.11,25–43 O Spanish Psoriasis Group da Spanish Academy of Dermatology and Venereology (AEDV) recomenda o monitoramento a cada oito a 12 semanas durante a fase de manutenção para a maioria dos agentes biológicos; a fase de manutenção foi definida como o período de tratamento iniciado após a fase de indução, independentemente de sua duração, com base nas necessidades do paciente e pode durar de várias semanas a anos, ou mesmo a vida toda, dependendo das necessidades do paciente.47
O painel de especialistas deste consenso considera que o seguimento a cada três meses é indicado para o contexto latino‐americano, considerando as circunstâncias clínicas e os diferentes cenários de convênios e sistemas de saúde na região.
Que seja de conhecimento dos autores, não há consenso sobre a definição de falha de redução gradual de biológicos. Em geral, a diminuição no escore PASI (< 50 ou <75 ou a diminuição ≥ 50% da melhora alcançada antes da descontinuação), escore PGA ≥ 3 ou perda do status de resposta, ou escore DLQI >5 indicaram falha na redução gradual em pacientes com psoríase em ensaios clínicos.14,15,17,18,52–56,67 Em estudos observacionais, a falha na redução gradual foi definida como perda de resposta, definida e medida individualmente pelo PASI ou DLQI, entre 3 e 24 meses após o início da estratégia.11,25–43 Em ensaios em que o tratamento com biológicos foi completamente interrompido, a falha foi definida como diminuição no escore PASI> 50% da melhora inicial ou escore PGA ≥ 3.13,16,19–24 O consenso espanhol sobre a avaliação e tratamento da psoríase moderada a grave definiu a recidiva após a descontinuação de medicamento eficaz como a perda de ≥ 50% da melhora alcançada ou escore PGA> 2 se PGA 0–1 foi alcançada em qualquer momento.47
Na opinião deste painel de especialistas, a heterogeneidade nas definições de falha de redução biológica em pacientes com psoríase é consequência da variabilidade na definição dos objetivos da estratégia. Neste contexto, qualquer evidência de regressão na obtenção dos objetivos de tratamento definidos para redução gradual indica falha. Da mesma maneira, circunstâncias clínicas específicas, como alterações na morfologia da psoríase (p. ex., psoríase eritrodérmica ou pustulosa generalizada), reativação ou aparecimento de lesões em áreas específicas e eventos negativos relatados pelo paciente, como o aparecimento de sintomas articulares ou aumento inaceitável na atividade da doença, também devem ser considerados como falhas da redução gradual e requerem avaliação rápida para determinar o curso de ação apropriado.
Nos ensaios que relataram recidiva, menos de 18% dos pacientes submetidos à redução gradual apresentaram recidiva dentro de seis meses a 40 semanas.13,17,19,55 Os tempos para recidiva variaram e nenhuma diferença significante nas taxas de recidiva foi relatada de acordo com o tipo de agente biológico.43 Uma vez que a perda de resposta foi estabelecida, as opções terapêuticas incluem reiniciar a terapia com biológicos na última dose eficaz, re‐tratamento com doses padrão, terapia de resgate ou troca de agentes biológicos.11,25–43 De acordo com o painel de consenso, a decisão terapêutica nesses pacientes deve ser baseada na gravidade da recidiva. Nos estudos que relataram esse achado, a maioria dos pacientes atingiu o PASI alvo dentro de quatro56 a 12 semanas17,55 do reinício do tratamento. A recuperação dessas respostas após o re‐tratamento também foi relatada em estudos de coorte de seguimento não controlados.31,36,45 Esses achados reforçam ainda mais a eficácia e a segurança da redução gradual da terapia com biológicos em pacientes com psoríase.
Considerações para implementaçãoAs estratégias de redução gradual visam minimizar a imunomodulação crônica, que está associada a infecções oportunistas e outras complicações. Além disso, a redução gradual reduz a ocorrência de efeitos colaterais e a ansiedade associada à medicação vitalícia. A redução gradual está de acordo com a preferência do paciente em reduzir a frequência das doses e o tempo gasto no tratamento. As estratégias para reduzir a terapia com biológicos em pacientes com psoríase também apoiam a racionalização técnico‐científica dentro dos sistemas regionais de saúde e abordam as limitações gerais de recursos na América Latina. Grupos de dermatologia relataram economia de custos como um dos principais resultados da redução da dose de agentes biológicos.51 Estudos de custo mostraram que a redução da dose ou o prolongamento do intervalo de administração, bem como regimes de terapia intermitente, são alternativas viáveis para otimizar o tratamento biológico e reduzir os custos da terapia.28,46
Este documento é baseado nas melhores evidências disponíveis no momento de sua produção. No entanto, reconhece‐se que os resultados de estudos em andamento ou pesquisas futuras podem exigir a modificação de algumas das recomendações descritas aqui ou a geração de novas recomendações. Os biológicos abordados no consenso estão disponíveis atualmente ou podem estar disponíveis em breve em países da América Latina. Algumas moléculas para as quais há evidências que apoiam a redução gradual, como o brodalumabe,54,58,66 não foram incluídas em recomendações específicas porque não estão disponíveis em países da América Latina. Atualmente, há muito poucos relatos sobre moléculas de redução gradual, como o risanquizumabe; portanto, diretrizes específicas para elas devem ser desenvolvidas em futuras atualizações deste consenso.
A orientação fornecida neste consenso tem como objetivo apoiar o desenvolvimento de estratégias de redução gradual eficientes e seguras para biológicos, mas não é uma diretriz rígida. Como já enfatizado, a flexibilidade nos regimes de redução gradual de biológicos deve ser mantida por meio de avaliações clínicas detalhadas e individualizadas, considerando os valores, preferências e circunstâncias dos pacientes no contexto da tomada de decisão compartilhada. Nesse contexto, espera‐se que as estratégias prescritas pelo médico para redução gradual ou reinício da terapia com biológicos para psoríase sejam facilitadas administrativamente para promover a adesão, garantir o seguimento oportuno e melhorar as chances de manter a doença estável com requisitos farmacológicos reduzidos.
ConclusõesA redução gradual de terapias com biológicos parece ser eficaz e segura em pacientes com psoríase com baixa atividade estável ou remissão clínica. Este consenso latino‐americano foi desenvolvido em reconhecimento à necessidade de uso racional e ideal de tais terapias, incluindo sua administração e descontinuação, para manter os melhores resultados de saúde para os pacientes. Este consenso visa facilitar a tomada de decisões incorporando as melhores e mais recentes evidências disponíveis, especialmente em populações heterogêneas com recursos de saúde limitados. Incentivar a pesquisa local é essencial para avançar o conhecimento sobre questões relacionadas à suspensão de biológicos e para informar futuras atualizações de redução gradual.
Suporte financeiroEste consenso é endossado pela Sociedade Latino‐Americana de Psoríase (SOLAPSO) e pelo Colombian Group of Psoriasis and Immunodermatology (COLPSOR), afiliado à Sociedade Colombiana de Dermatologia (ASOCOLDERMA). Foi desenvolvido de maneira completa e independente, com transparência e imparcialidade. Os financiadores não participaram do desenvolvimento do consenso, das decisões do painel ou do manuscrito final.
Contribuição dos autoresAngela María Londoño García: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Juan Raúl Castro‐Ayarza: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Manuel Darío Franco: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Cesar Fernando González Ardila: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Gabriel Magariños: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Enrique Salvador Rivas Zaldívar: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Susan Martínez: Revisão crítica da literatura, elaboração e redação da versão inicial do manuscrito, revisão editorial do manuscrito final, concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Linda Ibatá: Revisão crítica da literatura, elaboração e redação da versão inicial do manuscrito, revisão editorial do manuscrito final, concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Julieth Carolina Castillo: Revisão crítica da literatura, elaboração e redação da versão inicial do manuscrito, revisão editorial do manuscrito final, concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Paola Jimena Cárdenas Rojas: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Evelyn Giuliana Castro Vargas: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Claudia Romina Contreras: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Claudia de la Cruz Fernández: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Andrés Chavarriaga Restrepo: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Cristina Mariela Echeverria: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
André Vicente Esteves de Carvalho: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Benjamín Hidalgo‐Matlock: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Enrique Fabian Loaiza Sánchez: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Matías Rafael Maskin: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Ricardo Romiti: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Fernando Valenzuela: Concepção e planejamento do estudo, análise e interpretação dos dados, revisão crítica do conteúdo e aprovação final do manuscrito.
Conflito de interessesGrupo de desenvolvimentoÁngela María Londoño García: Dermatologista. Mestre em Epidemiologia, Mestre em Autoimunidade. Coordenadora de Pós‐Graduação em Dermatologia, CES University, Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante para: Abbvie, Boehringer Ingerhaim, Bristol, Eli Lilly, Jannsen, Novartis, Pfizer.
Juan Raúl Castro Ayarza: Dermatologista. Mestre em Dermatologia Oncológica. Candidato ao Mestrado em Epidemiologia. Professor na National University of Colombia, Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante para AbbVie, Amgen, Eli Lilly, Janssen, Novartis, Pfizer.
Manuel Darío Franco Franco: Dermatologista. Membro fundador do Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR, Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante para AbbVie, Amgen, Eli Lilly, Janssen, Novartis, Pharmalab e Sanofi.
César Fernando González Ardila: Dermatologista. Consultório particular, Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR.
Gabriel Magariños: Dermatologista. Psoriahue, Argentina. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante para: AbbVie, Boehringer Ingelheim, Eli Lilly, Jannsen e Novartis.
Enrique Salvador Rivas Zaldívar: Dermatologista. Fellowship em Cirurgia Dermatológica. Doutor em Medicina, Guatemala. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante da AbbVie e da Novartis.
Painel de especialistasPaola Jimena Cárdenas Rojas. Dermatologista. Mestre em Dermatologia Oncológica. Mestre em Saúde Pública. Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante da AbbVie, Amgen, Elli Lilly e Janssen.
Evelyn Giuliana Castro Vargas. Dermatologista. Tutor residente de dermatologia da Universidade de San Martin de Porres, Peru. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante da AbbVie, Janssen e Tecnofarma.
Cláudia Romina Contreras. Dermatologista. Mestre em Doenças Autoimunes. Paraguai. Sociedade Latino‐Americana de Psoríase – SOLAPSO.
Cláudia de la Cruz Fernández. Dermatologista. Chile. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante ou pesquisadora da AbbVie, Boehringer Ingelheim, Bristol Myers Squibb, Eli Lilly, Janssen, Novartis, Pfizer, Sandoz, UCB Pharma.
Andrés Chavarriaga Restrepo. Médico internista e reumatologista. Colômbia. Sociedade Latino‐Americana de Psoríase – SOLAPSO, Grupo Colombiano de Psoríase e Imunodermatologia – COLPSOR. Foi palestrante da Amgen, Eli Lilly, Jansen, Novartis, Pfizer, Pharmalab.
Cristina Mariela Echeverria. Dermatologista. Argentina. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante da AbbVie, Boehringer Ingelheim, Bristol Myers Squibb, Eli Lilly, Jannsen, L’Oreal, Novartis, Pfizer, Sandoz, UCB Pharma.
Andrés Vicente Esteves de Carvalho. Dermatologista. Brasil. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante da AbbVie, Boehringer, Eli Lilly, Jansen e Novartis.
Benjamín Hidalgo Matlock. Dermatologista. Costa Rica. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi pesquisador da Cutera e da Novartis.
Enrique Fabian Loaiza Sánchez. Dermatologista. Dermatopatologista. Mestre em Pesquisa Clínica e Epidemiológica. Professor da Universidade Católica. Equador. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante da Janssen, Medicament e Novartis.
Matías Rafael Maskin. Internista. Dermatologista. Argentina. Sociedade Latino‐Americana de Psoríase ‐ SOLAPSO.
Ricardo Romiti. Dermatologista. Brasil. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante para AbbVie, Boehringer, Eli Lilly, Janssen, LEO Pharma, Novartis, Teva e UCB.
Fernando Valenzuela. Dermatologista. Professor na Universidade do Chile. Chile. Sociedade Latino‐Americana de Psoríase – SOLAPSO. Foi palestrante para AbbVie, Boehringer Ingelheim, Eli Lilly, Jannsen, LEO e Novartis.
Equipe MetodológicaSusan Martínez R. Médica, especialista em Epidemiologia, Mestre em Saúde Pública. Epithink Health Consulting.
Linda Ibatá. Médica, especialista em Epidemiologia, Mestre em Saúde Pública. Epithink Health Consulting.
Julieth Carolina Castillo. Enfermeira, Especialista em Epidemiologia, Mestre em Saúde Pública. Epithink Health Consulting.
Como citar este artigo: García AML, Castro‐Ayarza JR, Franco MD, Ardila CFG, Magariños G, Zaldívar ESR, et al. Latin American consensus on tapering of biological therapy in psoriasis. An Bras Dermatol. 2025;100:501134.
Trabalho realizado no Latin American Psoriasis Society (SOLAPSO), Bogotá, Colômbia.