O albinismo oculocutâneo é doença autossômica recessiva causada pela completa ausência ou diminuição da biossíntese de melanina nos melanócitos. Devido à redução ou ausência de melanina, os albinos são altamente suscetíveis aos efeitos nocivos da radiação ultravioleta e estão em maior risco de dano actínico e câncer da pele. No Brasil, assim como em outras partes do mundo, o albinismo ainda é um distúrbio pouco conhecido, tanto em relação aos dados epidemiológicos quanto à variabilidade fenotípica e genotípica. Em várias regiões do país, os indivíduos com albinismo não têm acesso a recursos e atendimento médico especializado, e muitas vezes são negligenciados e privados de inclusão social. Por ser um país tropical, com alta incidência de radiação solar ao longo do ano e em todo o território, o dano actínico e o câncer da pele ocorrem precocemente e em alta incidência nessa população, levando muitas vezes à morte prematura. O monitoramento cutâneo desses pacientes e as intervenções terapêuticas imediatas, seguramente, têm impacto positivo na redução da morbimortalidade associada à condição. É evidente a importância da educação em saúde, a fim de informar adequadamente os albinos e suas famílias, a população geral, os educadores, os profissionais da área médica e os órgãos públicos quanto às particularidades dessa condição genética. O presente artigo tem por objetivo apresentar uma revisão acerca das características epidemiológicas, clínicas, genéticas e psicossociais do albinismo, com enfoque nas alterações cutâneas que envolvem essa rara desordem da pigmentação.
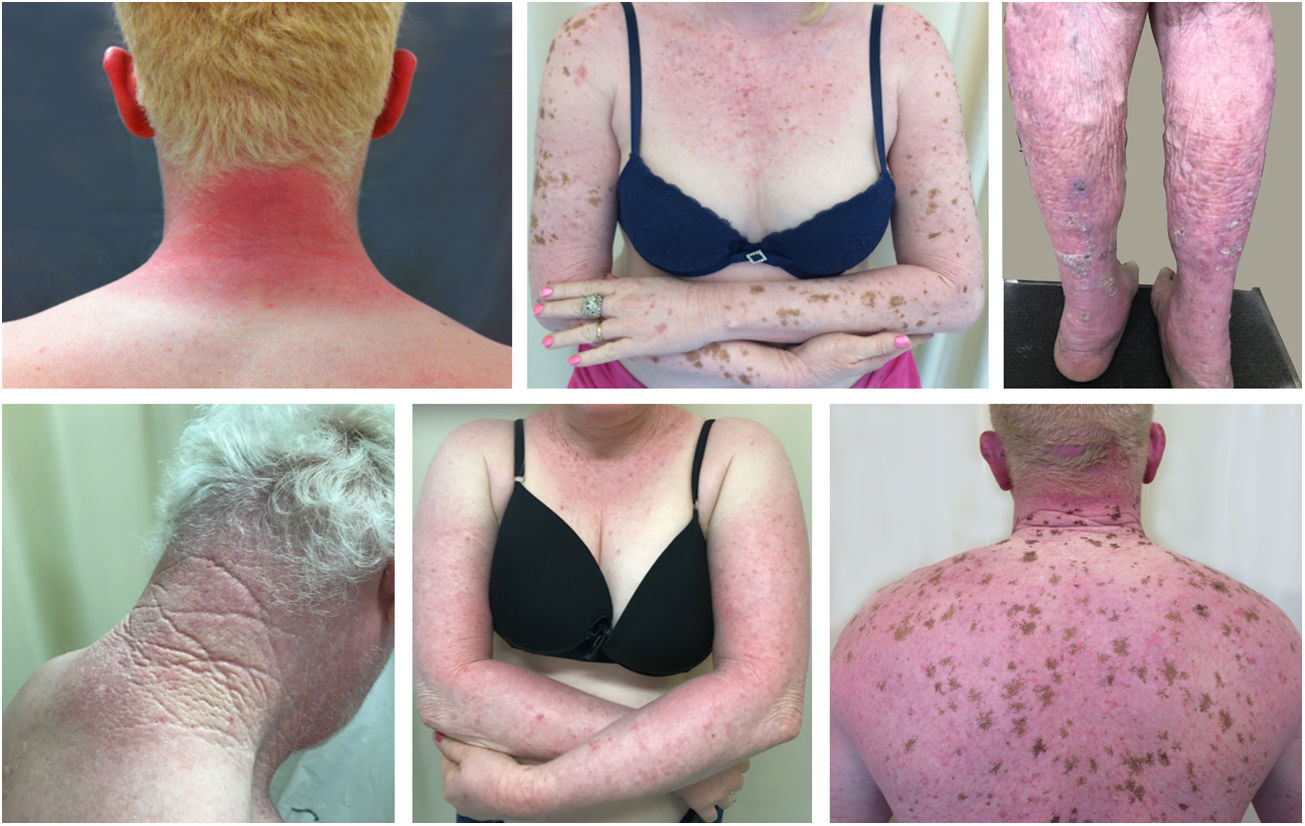
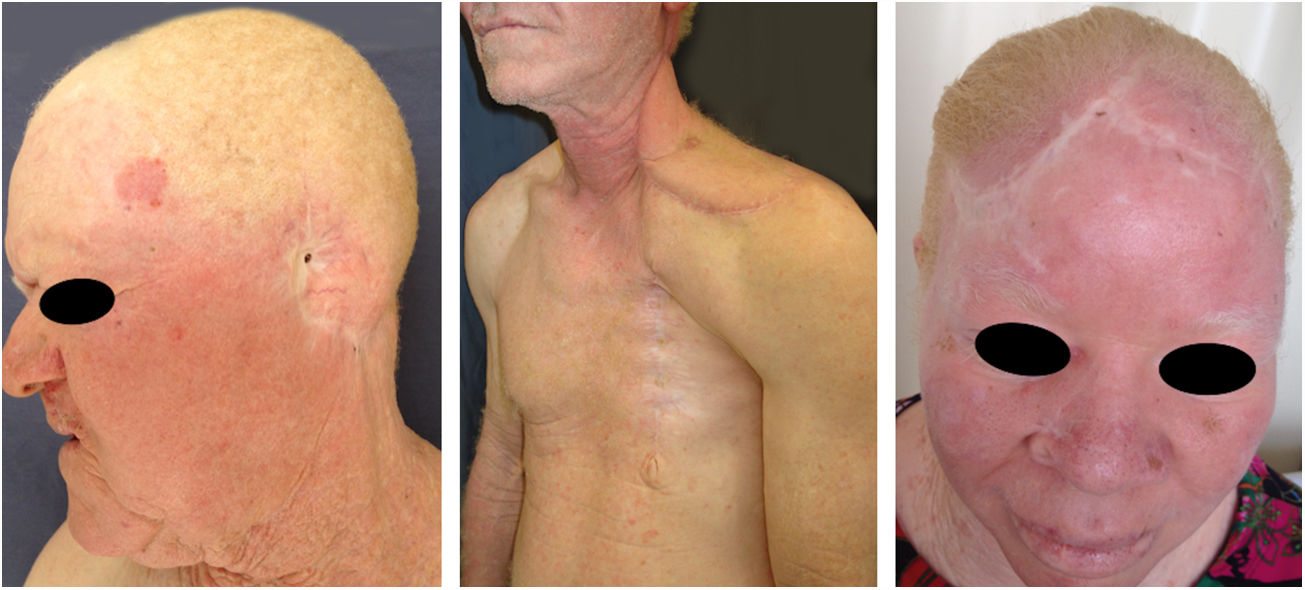
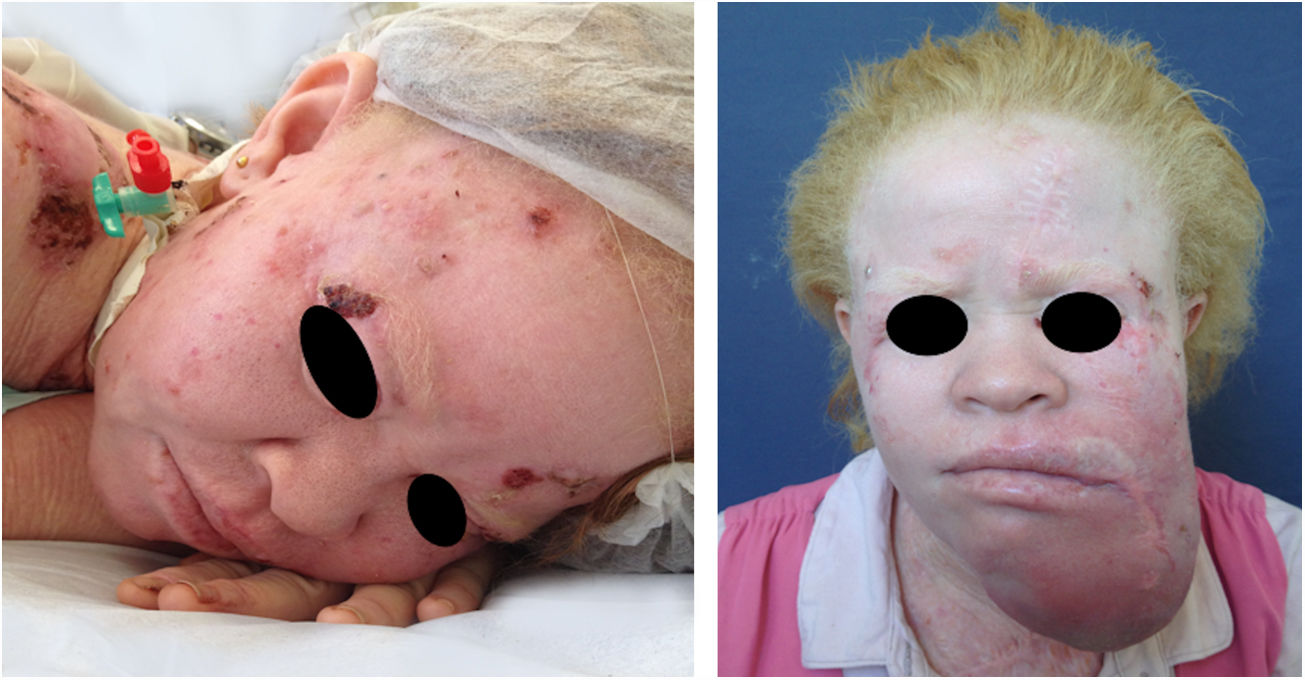
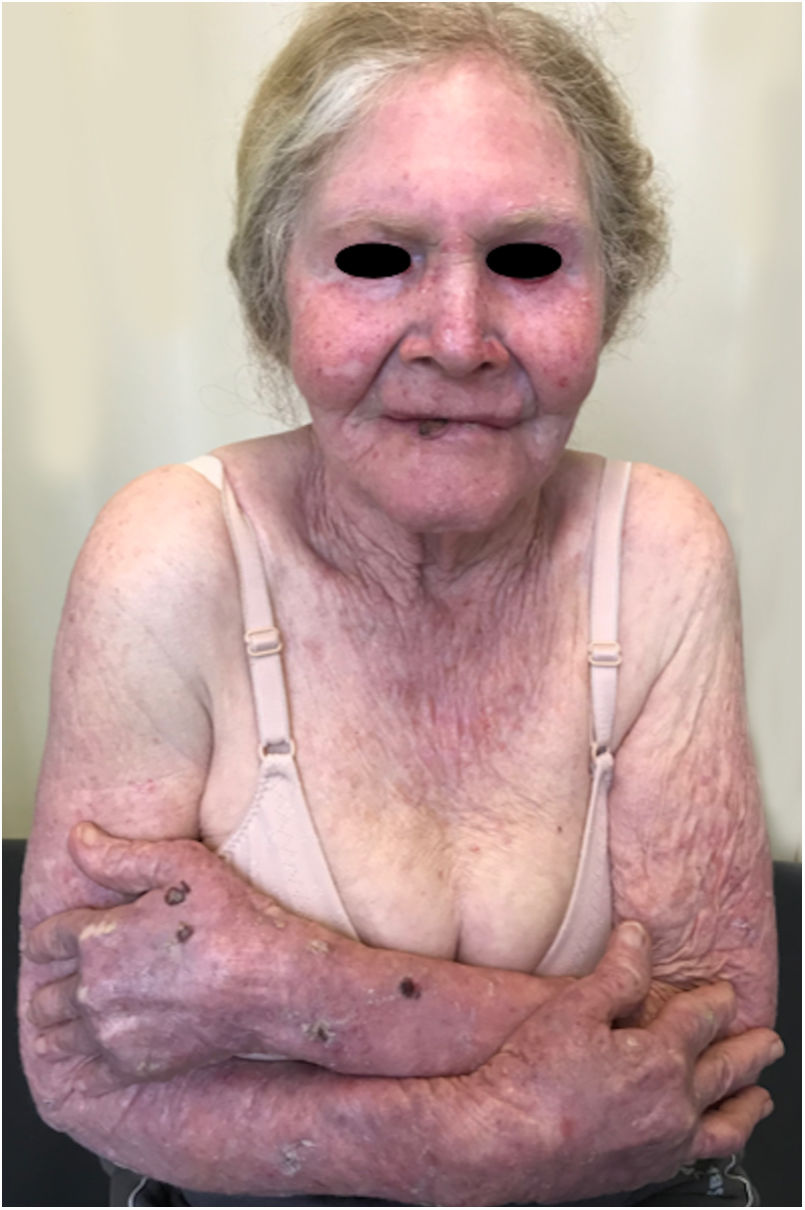
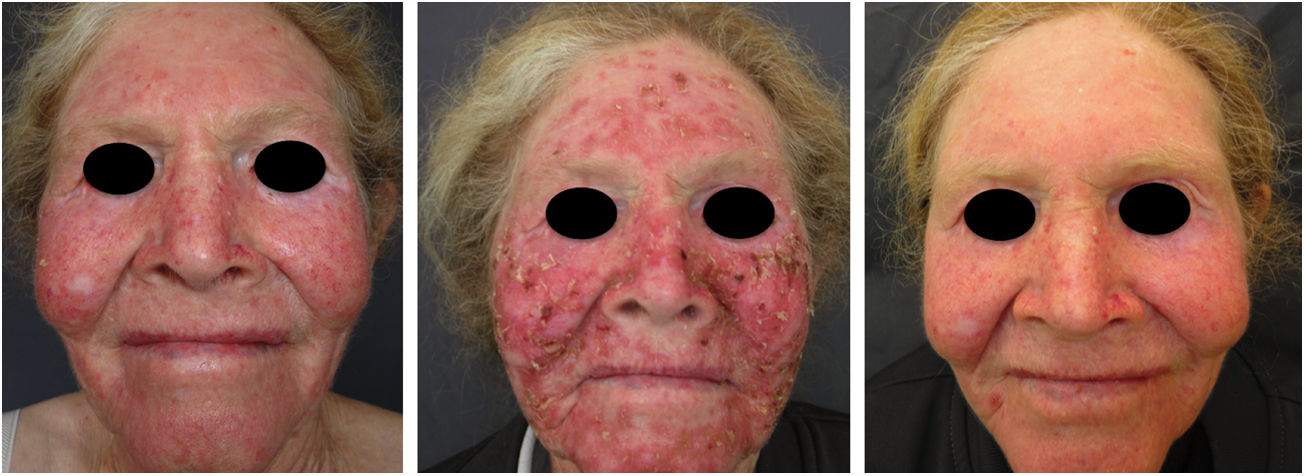
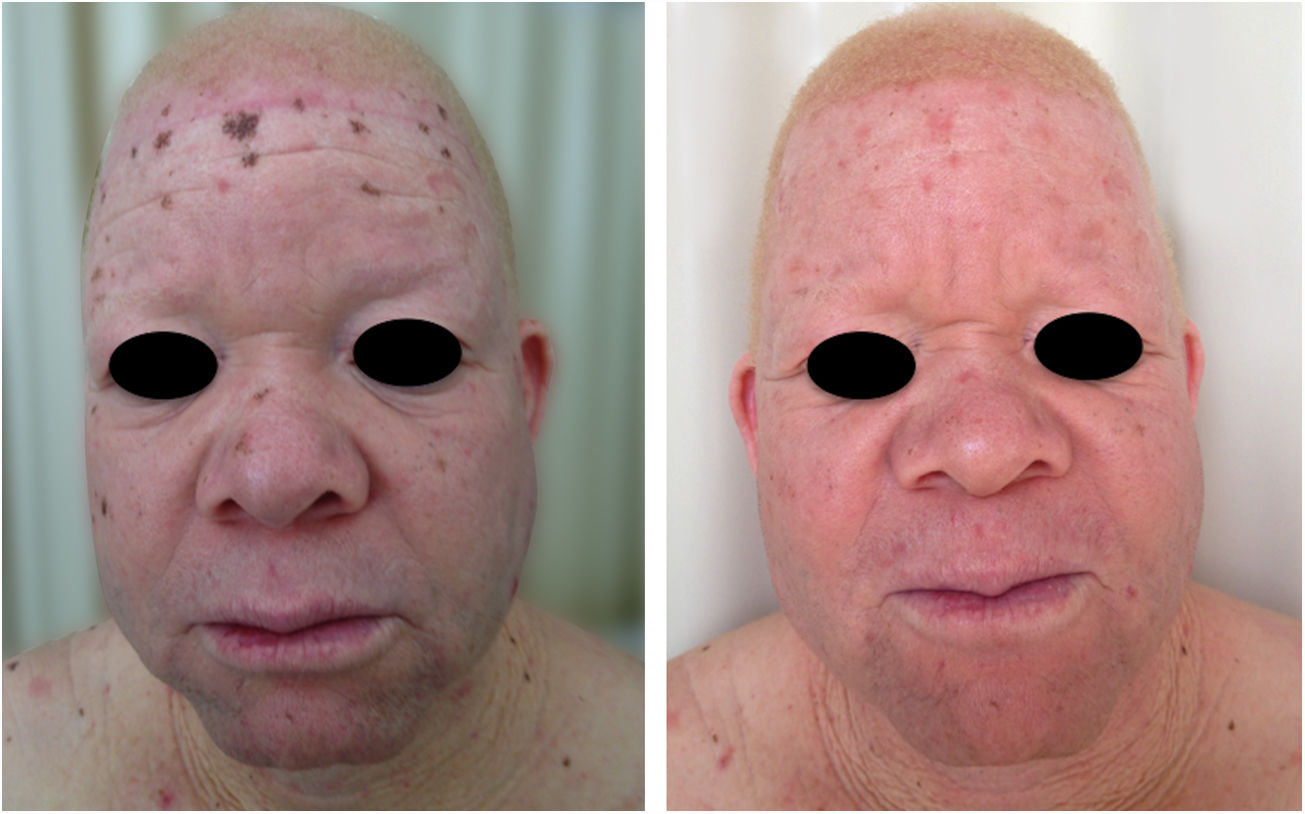
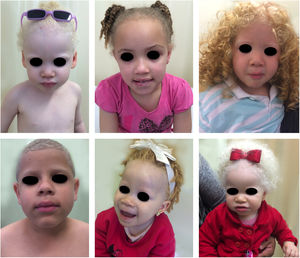
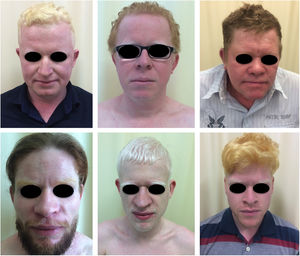
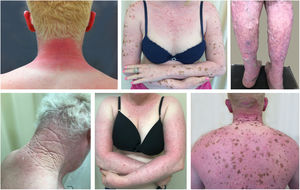
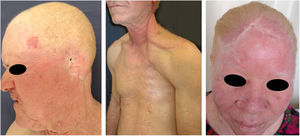
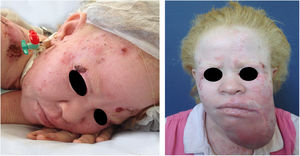
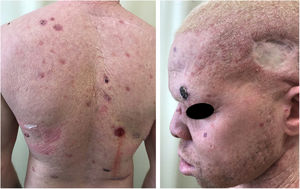
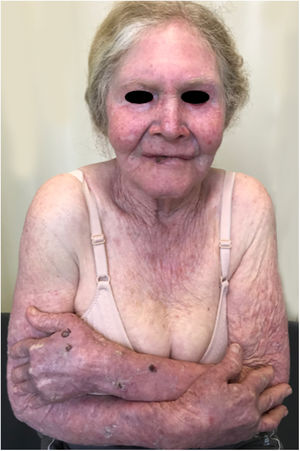
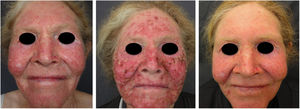
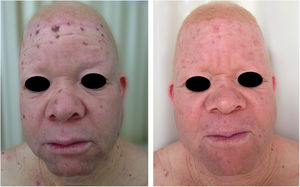
Albinismo oculocutâneo (AOC) é uma desordem autossômica recessiva causada por ausência completa ou redução da biossíntese de melanina nos melanócitos. Os pacientes com albinismo têm número normal de melanócitos na epiderme e nos folículos, mas o pigmento melanina é total ou parcialmente ausente.1–4 Os portadores de albinismo oculocutâneo não conseguem oxidar a tirosina em dopa por meio da tirosinase. Essa incapacidade de formar pigmento tem como consequência a pele muito clara, os cabelos brancos ou claros e olhos vermelhos, pois a luz reflete os vasos sanguíneos da retina, ou, ainda, azul‐esverdeados ou castanho claros, se houver formação de algum pigmento na íris. De fato, a variabilidade fenotípica no albinismo é vasta, oscilando de ausência completa de pigmentação no cabelo, pele e olhos à presença relativa de pigmento (figs. 1, 2 e 3).5–7
Devido à redução ou ausência de melanina, os albinos são altamente suscetíveis aos efeitos nocivos da radiação ultravioleta (RUV) e estão sob maior risco de danos actínicos – por exemplo, queimaduras solares, lentigos, elastose solar, queratoses actínicas, carcinoma basocelular e carcinoma espinocelular.5,8,9 Portanto, faz parte da conduta clínica educar os albinos e os membros da família sobre a importância da prevenção da exposição solar e sobre os métodos para proteção contra a RUV.
Muitos albinos desenvolvem queratoses actínicas ou cânceres da pele antes dos 30 anos de idade.5,8–12 As sequelas do câncer da pele são uma das principais causas de morte prematura nos pacientes com albinismo.11,12 O câncer da pele, para os pacientes que não foram protegidos do sol e que tiveram uma vida relativamente exposta, ocorre já na fase de adulto jovem e, na maioria das vezes, é múltiplo e de comportamento biológico agressivo, embora o melanoma seja raro nos pacientes com albinismo.5,8,9 Na maioria das vezes, a localização é na cabeça e no pescoço, áreas mais expostas à radiação. Devido à extrema sensibilidade à luz UV, albinos precisam de proteção absoluta ao sol e exame da pele realizado pelo menos a cada seis meses ou em intervalos menores.5,8,9
Nos albinos, é também comum a diminuição da acuidade visual, erros de refração, íris translúcida, nistagmo, hipoplasia da fóvea, hipopigmentação do fundo do olho e desvio das fibras do nervo óptico no quiasma. Esse desvio é caracterizado por excessivo cruzamento de fibras no quiasma óptico, o que pode resultar em estrabismo e redução da visão estereoscópica. Ademais, a fotofobia pode ser relevante. Os albinos, também do ponto de vista ocular, são mais suscetíveis aos efeitos prejudiciais da RUV.5–7 Indivíduos com albinismo, em sua maioria, sofrem com baixa visão em graus variados.
Tipos de albinismo e epidemiologiaO albinismo pode ocorrer nas formas sindrômica e não sindrômica. Nas formas sindrômicas de albinismo, das quais as principais são Hermansky‐Pudlak e Chediak‐Higashi, a hipopigmentação e as alterações visuais coexistem com alterações patológicas mais graves. A síndrome de Hermansky‐Pudlak pode cursar com alterações imunológicas, fibrose pulmonar intersticial, colite granulomatosa e diátese hemorrágica decorrente de alterações plaquetárias. Na síndrome de Chediak‐Higashi, além da hipopigmantação, podem estar presentes alterações hematológicas, alta suscetibilidade a infecções, sangramento e alterações neurológicas.13–17 O albinismo pode ainda se apresentar na forma exclusivamente ocular (AO1 e síndrome FHONDA).5,18,19
Existem atualmente 19 genes relacionados às diferentes apresentações clínicas do albinismo, incluindo sete para o AOC. Inicialmente, eram quatro os tipos principais de albinismo não sindrômico descritos: de AOC tipo 1 (A e B) até AOC4. O tipo AOC1A é o mais grave, com total ausência de produção de melanina ao longo da vida, enquanto as outras formas, AOC1B, AOC2, AOC3 e AOC4, mostram algum acúmulo de pigmentos ao longo do tempo. As mutações nos genes TYR, AOC2, TYRP1 e SLC45A2 são as principais responsáveis por causar AOC.2,5,10 Recentemente, mais dois novos genes, SLC24A5 e C10orf11,20 foram identificados como responsáveis por causar AOC6 e AOC7, respectivamente, totalizando sete tipos diferentes de albinismo. Também um lócus foi mapeado na região do cromossoma humano 4q24, que é responsável pela causa genética do AOC5.21
No entanto, ainda existe substancial número de casos de albinismo sem identificação molecular, sugerindo que genes adicionais podem estar associados com o albinismo. Além disso, o desconhecimento sobre os mecanismos subjacentes pelos quais uma mutação genética tem efeito funcional deletério sobre o produto do gene faz com que a doença não seja completamente compreendida até o presente.21
No Brasil, o diagnóstico clínico do albinismo é realizado com base na presença de alterações cutâneas típicas e de achados oculares. A distinção entre os subtipos de albinismo a partir das características clínicas, além de sua ampla heterogeneidade fenotípica, tornam difícil estabelecer correlações fenotipogenéticas, e há grande sobreposição de diferentes formas da doença. Por isso, é hoje necessária pesquisa molecular para definição exata do tipo de mutação. No entanto, esse exame não está disponível no sistema público de saúde brasileiro.2–4
O albinismo é um distúrbio genético que ocorre em indivíduos de qualquer classe social e em todos os países do mundo, mas com prevalências variadas. A incidência mundial do albinismo é de 1:20.000 habitantes – os Estados Unidos apresentam um índice menor (1:37.000),1,7,22 enquanto a maior incidência reportada na literatura até o momento deu‐se entre os índios Cuna (no Panamá e na Colômbia): estima‐se que ocorra em 6,3:1.000 habitantes.23 Altas incidências foram reportadas também na África.22,23 Na Tanzânia, Luande et al.24 estimaram que havia 700 albinos que viviam em Dar es Salaam, uma prevalência de cerca de 1:1.500 habitantes. Na África Subsaariana, 1:5.000 a 1:15.000 pessoas é portadora de albinismo.25 Um estudo de revisão publicado em 2006 revelou que sete publicações continham dados epidemiológicos sobre a prevalência do albinismo na África do Sul, Zimbabwe, Tanzânia e Nigéria.26 A prevalência de albinismo desses estudos variou de 1:15.000 no estado leste‐central da Nigéri27a até 1:1.000 na tribo de Tonga do Zimbábue, uma comunidade rural isolada.28 O albinismo é considerado uma condição hereditária relativamente comum entre as populações da África Austral. Além da limitada mobilidade geográfica, a consanguinidade, juntamente com outras práticas tradicionais de casamento, também podem ser fatores a serem considerados na avaliação das tendências de prevalência atuais e futuras do albinismo.22,27–29
A prevalência dos diferentes tipos de AOC varia de acordo com a população. AOC1 é o subtipo mais comum encontrado em caucasianos e é responsável por cerca de 50% dos casos em todo o mundo.30,31 O AOC2, ou AOC marrom, é responsável por 30% dos casos em todo o mundo e é mais comum na África, onde se estima que afete 1:10.000 pessoas e mais de 1:1.000 em determinadas populações.27,32 Isso se deve principalmente a uma deleção do AOC2 de alta frequência encontrada na população africana.32–35 O AOC3, ou AOC ruivo, é praticamente inexistente em caucasianos, mas afeta aproximadamente 1:8.500 indivíduos da África do Sul ou 3% dos casos em todo o mundo.31 O AOC4 também é raro entre os caucasianos, assim como entre os africanos, mas em todo o mundo é responsável por 17% dos casos, e no Japão é diagnosticado em 1:4 pessoas afetadas pelo AOC. No Japão e na China, as formas predominantes são o AOC1 e o AOC4, respectivamente em primeiro e segundo lugares.31,36 Novos genes e mutações vêm sendo descobertos ao redor do mundo, como o responsável pelo AOC5 que foi identificado no Paquistão,37 pelo AOC6, identificado inicialmente na China, mas já descrito em outras populações,38,39 e pelo AOC7, identificado em uma família das ilhas Faroé e na Dinamarca.20 A forma sindrômica Hermansky‐Pudlak apresenta alta incidência na população porto‐riquenha40,41 e mostrou‐se relativamente prevalente em algumas populações – como exemplo, um recente estudo europeu avaliou de forma prospectiva as características clínicas e genéticas em um grupo de pacientes (33 crianças e 31 adultos) atendidos em um hospital‐dia especializado e revelou prevalência de 7,8%.42 A síndrome de Chediak‐Higashi é universalmente rara, descrita em algumas regiões europeias e da Ásia.16,17
No Brasil, não existe mapeamento epidemiológico do albinismo. Estudos epidemiológicos são escassos e não há nenhum tipo de informação nas bases de dados do governo (seja pelo Censo do Instituto Brasileiro de Geografia e Estatística, IBGE, seja pelo DATASUS) sobre a incidência da desordem genética no país. Pressupõe‐se que a incidência seja maior nas regiões com maior prevalência da população negra, como é o caso do Nordeste. A Bahia, terceiro estado mais populoso do Brasil, tem a maioria da população negra ou parda e, supostamente, devido à alta presença de ancestralidade negra, uma vez que a região foi porta de entrada para escravos africanos durante o período de colonização, apresenta também a maior incidência de albinos do país.43,44 Em estudo sobre o perfil do albinismo na Bahia, verificou‐se que 70% dos albinos declararam ascendência negra ou parda.44 Outro estudo realizado na cidade de Salvador revelou o registro de moradores com albinismo em 44% dos 163 bairros e localidades da capital – 17% com frequência maior que 1:10.000 e 8,5% com frequência maior que 2:10.000. Entre os bairros com maiores taxas de albinismo, foi observada frequência elevada da raça negra. Em uma das regiões investigadas, chamada Ilha de Maré, em que vive população remanescente de quilombo, foi encontrada proporção de albinos acima de 1:1.000 habitantes.43
Outra localidade brasileira estudada pela alta incidência de albinismo é o município de Lençóis, no norte do Maranhão. Por ter população pequena e acesso remoto, a consanguinidade é alta e a frequência hipotética registrada de albinismo nas décadas de 1970 a 1980 chegou a ser considerada uma das maiores do mundo. Atualmente, essa região apresenta número reduzido de albinos, pois muitos migraram para outras regiões e/ou morreram precocemente por câncer da pele, segundo relatos não publicados. Há também relatos isolados de albinismo em diversas comunidades indígenas no país (Pará, Acre, Paraná, São Paulo, Mato Grosso), informações não publicadas em periódico científico.45–47
Os poucos estudos e relatos disponíveis na literatura científica favorecem a hipótese de provável apresentação do albinismo no Brasil, em números, semelhante ao da África. No entanto, fica a dúvida se esses números refletem a realidade de todo o país e a certeza da necessidade de mobilização do governo para o registro do albinismo nas bases oficiais ou o desenvolvimento de estudos populacionais que revelem esses índices de maneira fidedigna. Portanto, há grande escassez de estudos que desenhem a epidemiologia do albinismo no Brasil. Mais estudos são necessários para melhor compreensão sobre o modo como essa desordem genética incide no país e o consequente estabelecimento de estratégias mais objetivas e assertivas para a condição.
A ocorrência do albinismo está associada a dificuldades e desvantagens, consequências do distúrbio genético e da segregação social. O albinismo é um distúrbio estigmatizante, que afeta os portadores e suas famílias. Relatos de estudos realizados no estado da Bahia, dados da Associação de Pessoas com Albinismo no Estado da Bahia* [APALBA] (http://apalba‐albinosdabahia.blogspot.com), referências informais globais e a experiência prática dos autores revelam que os albinos no Brasil, mesmo nos grandes centros, sofrem com preconceito e exclusão social, além de padecerem de acesso restrito à assistência médica especializada e recursos. Esses fatores contribuem para o aumento da morbimortalidade associada à condição, o que inclui, por exemplo, os danos actínicos e o câncer da pele.44–48
Fisiopatologia – albinismo, danos actínicos e câncer da peleFisiopatologia da biossíntese da melanina e albinismo oculocutâneoA pigmentação da pele varia entre os indivíduos e é determinada por múltiplos fatores, incluindo o número e a atividade metabólica dos melanócitos na camada basal da epiderme, a atividade melanogênica dos melanossomas dentro desses melanócitos e variações em número, tamanho e distribuição dos melanossomas. Diferenças nos tipos de melaninas, no grau de arborização dos prolongamentos dendríticos dos melanócitos e na transferência de melanossomas a partir desses prolongamentos para os queratinócitos também afetam a pigmentação da pele.49,50
Os melanócitos têm origem ectodérmica, na crista neural, evoluindo com migração cutânea (cabelo, pele) ou extracutânea (olhos, cóclea, leptomeninge). Alguns genes controlam a proliferação e a diferenciação das células da crista neural e regulam a migração dos melanócitos precursores para suas posições finais. O fator de transcrição de microftalmia (MITF) é o principal regulador do desenvolvimento, da função e da sobrevivência dos melanócitos51 e é responsável por modular a expressão de algumas proteínas específicas nessas células.52 Após a diferenciação dos melanócitos, o MITF regula a expressão de genes durante a exposição à RUV, auxiliando no bronzeamento da pele.53
A melanina é um pigmento polimérico produzido nos melanócitos. Sua síntese ocorre por reações enzimáticas que convertem a tirosina em melanina por meio da enzima tirosinase. A biossíntese da melanina é regulada por vários fatores, particularmente pelo receptor da melanocortina‐1 (MC1R) nos melanócitos e seu ligante, o hormônio estimulante α‐melanócito (α MSH). Citocinas e fatores de crescimento do meio ambiente e o grau de atividade basal da tirosinase, da proteína 1 relacionada à tirosinase (TRP1) e das proteínas associadas à membrana de transporte são fatores adicionais que regulam essa biossíntese.50–54
Uma das importantes funções da melanina é proteger a pele e os olhos dos efeitos nocivos da RUV. A melanina produzida mediante essa modulação é transferida para os queratinócitos circunvizinhos, onde ocorre então a formação de uma capa ao redor do núcleo, protegendo o DNA do dano induzido pela RUV.50,55 O grau de pigmentação da pele é inversamente correlacionado com o risco de câncer da pele induzido pelo sol.53
Mutações genéticas envolvidas no albinismoGeneticamente, o albinismo é classificado de acordo com o tipo de mutação genética presente. Existem sete tipos de AOC não sindrômico atualmente identificados; desses, o AOC1 e o AOC2 são os mais frequentes. O AOC1 é considerado o tipo globalmente mais prevalente,56 afeta diferentes grupos étnicos/raciais e é caracterizado por perda da função da enzima tirosinase, como resultado de uma mutação no gene TYR. A tirosina é a enzima crítica na biossíntese da eumelanina marrom‐preta e da feomelanina amarela. Indivíduos com AOC1A têm TYR não funcional, com ausência total da produção de melanina, enquanto em indivíduos com AOC1B existe alguma função da atividade da tirosinase com produção limitada de melanina.57 O AOC2 é a forma mais prevalente de albinismo na África.5,35,53 Afeta os negros mais comumente do que os brancos e caracteriza‐se por mutações no gene AOC2 (anteriormente conhecido como gene P) que codifica a proteína P.5,57 Suas funções precisas não são totalmente compreendidas, mas a proteína P parece estar envolvida com as proteínas de transporte para o melanossoma, estabilizando o complexo proteico melanossomal e a regulação do pH do melanossoma e/ou metabolismo da glutationa, todos os quais com significativa importância para a produção de melanina.5,34,57–59 Albinos com um fenótipo AOC2 não têm eumelanina, mas têm algum grau de feomelanina, que pode aumentar progressivamente com a idade.57,60
Os fenótipos AOC3 e AOC4 do albinismo são causados por mutações em genes que codificam a proteína 1 relacionada à tirosinase (TYRP1) e a proteína de transporte associada à membrana (MATP), respectivamente.60 A TYPR1 é a enzima que estabiliza a tirosinase. Mutações na TYPR1 estão associadas à degradação precoce da tirosinase e maturação tardia dos melanossomas.7 A MATP funciona como um transportador de membrana melanossomal de proteínas necessárias para a biossíntese de melanina. Mutações no gene MATP, consequentemente, causam hipopigmentação e o fenótipo AOC4 do albinismo.7 O fenótipo AOC5 está ligado a um gene específico ainda não identificado, mapeado para a região do cromossoma 4q24, e foi descoberto nos membros de uma família paquistanesa consanguínea.37,61
No início de 2013, uma equipe chinesa de pesquisadores relatou a utilização de abordagem de sequenciamento abrangente para revelar a base molecular do albinismo em uma família afetada. Descobriram que mutações em SLC24A5, gene que codifica a proteína transportadora de soluto, estavam associadas a uma nova forma de AOC, nomeada como AOC6. Mutações de SLC24A5 foram detectadas em pacientes de diversas origens étnicas, indicando assim que o AOC6 não está restrito à população chinesa. Resultados recentes indicam atuação importante do SLC24A5 na maturação dos melanossomas, na arquitetura melanossomal e na adequada biosíntese da melanina. Estudos em animais revelaram que a mutação desse gene leva à diminuição do número, do tamanho e da densidade dos melanossomas.38,39 Também em 2013 foi descoberto um novo gene associado ao albinismo entre indivíduos com AOC das Ilhas Faroé (Dinamarca). O gene C10orf11 foi identificado pelo mapeamento genético de uma família consanguínea. Além disso, uma mutação no mesmo gene C10orf11 foi encontrada em um albino originário da Lituânia. Dados sugerem fortemente um papel desse novo gene na diferenciação dos melanócitos.5,21
Ao nascer, pessoas com diferentes formas fenotípicas de AOC apresentam, no geral, cabelos brancos e pele muito pálida ou rosa‐esbranquiçada. Indivíduos com AOC1B, AOC2, AOC3, AOC4, AOC5, AOC6 ou AOC7 irão adquirir alguma pigmentação durante a vida, mas aqueles com AOC1A permanecerão completamente despigmentados.37,60,61
Melanina e câncer da peleA melanina cutânea, particularmente a eumelanina (marrom/preta), fornece proteção contra a radiação solar e contra o dano oxidativo ao DNA induzido por estresse, de modo que indivíduos de pele escura têm uma frequência menor de cânceres da pele do que indivíduos de pele clara. No entanto, a fotoproteção proporcionada pela melanina não está completa mesmo em pessoas de pele escura, que também podem apresentar danos ao DNA induzidos pela radiação solar porém, esses danos geralmente ocorrem em grau passível de reversão pelos mecanismos de reparo ao DNA celular, reduzindo assim o risco de transformação maligna. Por outro lado, em indivíduos de pele clara, que não têm melanina suficiente para fornecer proteção eficaz contra a radiação solar, a extensão do dano ao DNA pode exceder a capacidade desses mecanismos de reparo, com maior risco de transformação maligna.62,63 Albinos que têm pouca ou nenhuma melanina na pele são, portanto, muito suscetíveis aos carcinomas induzidos pela radiação solar.
A melanina presente no AOC é principalmente a feomelanina (amarela/vermelha), com produção mínima de eumelanina.64 A eumelanina tem um importante papel fotoprotetor. Embora a feomelanina ofereça alguma fotoproteção contra a radiação solar, durante sua biossíntese, espécies reativas de oxigênio (ROS) carcinogênicas são geradas. Portanto, em albinos, tanto a redução na fotoproteção pela pequena quantidade de eumelanina presente quanto o aumento de ROS derivadas da feomelanina estão implicados nos carcinomas de queratinócitos.60
A biossíntese de ambos os tipos de melanina, eumelanina marrom/preta e feomelanina amarela/vermelha, é controlada em grande parte pelo MC1R nos melanócitos. Albinos com o fenótipo AOC2 que apresentam variantes genéticas polimórficas de MC1R, em contraste com a maioria dos outros albinos, podem ter cabelos avermelhados e um tom de pele amarelado.65 A atividade de algumas variantes do MC1R pode neutralizar a apoptose e reduzir a capacidade de reparo ao DNA nos melanócitos. Também pode, indiretamente, reduzir a proteção de queratinócitos contra o dano ao DNA induzido pela radiação solar, devido à produção reduzida de eumelanina, aumentando assim o risco de câncer da pele. As variantes do gene MC1R estão associadas não apenas com produção desregulada de melanina e capacidade de bronzeamento reduzido, mas também com a modulação de respostas imunoinflamatórias que são importantes na vigilância imunológica e na destruição de queratinócitos transformados pela radiação solar.49,64,66 Desse modo, polimorfismos genéticos de outros genes codificadores envolvidos na biossíntese da melanina (TYR e TYRP1), além de determinar a pigmentação da pele, são realmente fatores que contribuem para o risco de desenvolver câncer da pele.49 Tem sido sugerido que a tirosinase funcionalmente ativa tem a capacidade de proteger contra os danos oxidativos ao DNA.67 A falta de melanina e a exposição à intensa RUV aumenta o risco de desenvolvimento de câncer cutâneo.68–70
Diferenças na sensibilidade à carcinogênese da pele podem ser esperadas dependendo da mutação no AOC. Não há, até o momento, evidências convincentes para as diferenças de risco entre os vários tipos de albinismo. A suposição de que a presença de baixos níveis de pigmento oferece alguma fotoproteção, reduzindo o risco de desenvolvimento de câncer da pele em albinos, pode ser questionada.60 Relatos na literatura sugerem que pacientes com AOC1A têm risco menor de desenvolver câncer da pele em comparação com os outros tipos de AOC. Isso é apoiado pelo fato de que o polímero de melanina feomelanina é produzido principalmente quando a melanogênese permanece em nível basal, como em AOC1B, 2, 3, 4, 5, 6 e 7. A feomelanina promove a produção de ROS. O efeito prejudicial das ROS sobre o DNA é bem conhecido.71 Como os pacientes com AOC1A não sintetizam feomelanina, o risco de produzir ROS induzidas pela RUV é menor. Outro argumento que sugere que os pacientes AOC1A podem ser menos vulneráveis aos carcinomas da pele vem da comparação com o vitiligo. Em pacientes cujas manchas brancas não têm melanina, foi relatada uma correlação negativa entre vitiligo e câncer da pele.72 Uma explicação para isso pode ser que os níveis aumentados de glutationa peroxidase e superóxido dismutase (SOD) inativam as ROS, proporcionando proteção contra o dano oxidativo e, com isso, reduzindo o risco de câncer da pele.73 É de interesse investigar a pele branca de pacientes com AOC1A para distinguir entre as suscetibilidades ao câncer da pele induzidos por RUV. As várias mutações que causam AOC devem ser consideradas em conjunto com estudos sobre polimorfismos de nucleotídeo único (SNPs), buscando associação significativa com o risco de câncer da pele.74 Em conclusão, a ausência de feomelaninas e a possível inativação de ROS por enzimas antioxidantes faz com que o risco de câncer da pele induzido por RUV em pacientes com AOC1A possivelmente seja menor do que nos demais tipos de AOC. Para obter uma comparação válida do risco de câncer da pele entre o AOC1A e os outros tipos de albinismo, pesquisas relacionadas às diferenças na concentração de ROS devem ser realizadas. Além disso, as informações obtidas dos SNPs devem ser levadas em consideração, fornecendo dados adicionais sobre os mecanismos moleculares do câncer da pele no albinismo.60
Transformação maligna induzida pela radiação solar no albinismoO AOC predispõe aos carcinomas de queratinócitos da pele, ou seja, ao carcinoma basocelular (CBC) e ao carcinoma espinocelular (CEC), particularmente nas áreas mais expostas ao sol.11,75 Como os indivíduos com AOC são, na maioria, muito propensos à queimadura solar,5 os queratinócitos progenitores das células basais da pele de albinos exposta ao sol correm grande risco de sofrer transformação maligna induzida pela RUV. CECs em albinos podem surgir de novo ou de lesões actínicas pré‐malignas, como queratoses actínicas, em que os queratinócitos já sofreram transformação inicial induzida pela radiação solar. Os queratinócitos apresentam danos no DNA de diferentes graus de gravidade, de acordo com a intensidade e a duração da exposição à luz solar. Normalmente, o gene supressor de tumores p53 interrompe o ciclo celular, permitindo o reparo do DNA danificado, ou promovendo a apoptose se os danos ao DNA são irreparáveis. No entanto, se a radiação solar induzir mutações no próprio p53, tornando‐o disfuncional, haverá propagação do DNA danificado por divisão celular, resultando em campo epitelial pré‐cancerizado composto por clone de queratinócitos inicialmente transformados, com instabilidade genômica. Essa instabilidade genômica predispõe à transformação inicial dos queratinócitos a alterações genéticas adicionais e pode conduzir aos processos de divergência clonal, com consequente expansão de queratinócitos com vantagem de crescimento seletivo, em última análise, dando origem a um CEC franco.50,62,76,77
O risco de câncer da pele é proporcional ao quantum acumulado de RUV absorvida pelos queratinócitos.78 O potencial de alteração maligna é determinado pelo número de insultos genéticos. Assim, frequências numerosas de menores exposições à luz solar são mais prováveis de serem carcinogênicas do que exposições maiores, mas pouco frequentes,78 pois cada evento de exposição tem o potencial de causar uma mudança. Quanto mais alterações genéticas ocorrem, maior será a chance de transformação maligna.
Como os albinos são fotossensíveis e tendem a sofrer queimadura facilmente, a inflamação local induzida pela radiação solar na pele pode ser um fator adicional em causar um aumento na proliferação e longevidade dos queratinócitos, favorecendo a transformação maligna. Após a queimadura solar, as ROS derivadas das células inflamatórias locais podem causar danos diretamente ao DNA, e/ou desregular os mecanismos, não apenas de reparo ao DNA e controle do ciclo celular, mas também da apoptose, promovendo evolução para carcinoma cutâneo.79
Em nível molecular, o dano ao DNA induzido pela RUV é caracterizado pela substituição de nucleotídeos específicos, particularmente transições C > T e CC > TT encontradas no gene p53, que codifica a proteína p53, a qual normalmente regula o ciclo celular, a apoptose e o reparo ao DNA. A radiação solar regularmente provoca essas alterações genéticas, que são referidas como “assinaturas” associadas à RUV; essas mutações “assinadas” conduzem a transformação maligna da radiação solar induzindo câncer da pele.78,80
Os queratinócitos inicialmente transformados são imunogênicos e geram respostas imunes que podem modular ou controlar a tumorigênese. No entanto, a imunossupressão induzida pela radiação solar pode interferir criticamente com esse mecanismo de proteção.81 Assim, a exposição aos raios UV é altamente prejudicial para a pele hipopigmentada dos albinos. A falta de melanina predispõe essa população a danos cutâneos graves. A maioria dessas lesões está nas partes do corpo mais expostas ao sol, como face, orelhas, pescoço e ombros. As lesões cutâneas incluem queimaduras solares, bolhas, elastose/queratose solar, efélides, lentiginose e câncer da pele.24,68,82,83
Fatores climáticos e câncer da pele no albinismoFatores climáticos no BrasilO Brasil é cortado ao norte pela Linha do Equador e ao sul pelo Trópico de Capricórnio, estando 92% do seu território em Zona Tropical, o que faz com que a disponibilidade de radiação solar seja bastante elevada. Apesar de haver variações de latitude, altitude e características atmosféricas nas diferentes regiões, estudos meteorológicos mostram que os índices de RUV costumam ser muito altos em todo o país, mesmo no inverno e mesmo fora dos horários considerados críticos para exposição solar, habitualmente atingindo as escalas mais elevadas do índice ultravioleta (IUV) referido pela Organização Mundial de Saúde (OMS)‐isto é, de dano muito alto (IUV entre 8 e 10) a extremo (IUV superior a 11). As doses diárias de radiação são, em média, mais elevadas nas regiões Norte e Nordeste, atingindo 20 vezes as doses recomendadas pela OMS mesmo no inverno, mas níveis críticos, acima de 15, são também registrados na região Sudeste, no verão.84,85 Sabemos que altas doses de RUV acumulada estão associadas com o desenvolvimento de carcinomas cutâneos. Estudos revelam que a incidência de CEC dobra para cada diminuição de 8 a 10 graus na latitude, sendo máxima no Equador.86 A dose UV por unidade de tempo no Equador é de cerca de 200% da dose na Europa ou norte dos Estados Unidos.87 Esse acúmulo de RUV ocorre facilmente na pele albina devido à deficiência de melanina e faz, portanto, com que o Brasil seja um país bastante desfavorável para essa população altamente vulnerável.
Radiação solar, danos actínicos e câncer da peleA prevalência de queratose actínica depende do tipo de pele, da localização geográfica e da duração da exposição à luz solar; sem tratamento, essas lesões podem evoluir para CEC.88,89 Conforme referido, o Brasil recebe alto índice de RUV, favorecendo o surgimento de câncer da pele em sua população com fototipos mais baixos.90 Estudo na Austrália realizado por Green e Batistutta91 mostrou que a pele clara é o fator de risco mais importante para o desenvolvimento de carcinomas. Maia et al.92 classificaram o tipo de pele de 259 pacientes com CBC de acordo com os critérios de Fitzpatrick.93 As formas de pele clara I e II apresentaram maior chance de desenvolver o carcinoma. Esses estudos apontam a relação direta entre pele clara e maior ocorrência de câncer da pele, e nesse grupo podem‐se incluir os portadores de albinismo.
Danos actínicos e câncer da pele são geralmente encontrados em indivíduos de meia‐idade e idosos de pele clara que vivem em áreas ensolaradas, como Austrália e África do Sul.94 Estima‐se que 80% dos carcinomas cutâneos são diagnosticado em pessoas acima de 55 anos.95 Estudo recentemente realizado no setor de Oncologia Cutânea da Clínica de Dermatologia da Santa Casa de Misericórdia de São Paulo (ainda não publicado) revelou que, dentre 945 pacientes que apresentaram câncer da pele não melanoma (CPNM) pela primeira vez, a média de idade foi de 68 anos – 1,7% apresentavam idade inferior a 40 anos e 90,3% apresentavam idade superior a 50 anos. Em contrapartida, estudo semelhante realizado com pacientes do Programa Assistencial Pró‐Albino do mesmo serviço (não publicado), incluindo 146 pacientes, revelou que a média de idade dos pacientes albinos com câncer da pele foi de 47 anos. Como esperado, a falta de uso de proteção solar e a queimadura se associaram significativamente com a ocorrência do câncer. Chamou também a atenção na população estudada a alta prevalência dos danos actínicos (fig. 4): queimadura solar (72%), queratose actínica (45%), elastose (57%), lentigos (25%) e câncer da pele (26%). Infelizmente, esses danos estiveram presentes de maneira significativa, com números muito parecidos com alguns estudos africanos.27 Essas lesões expõem os albinos a múltiplos tratamentos, cirurgias e mutilações que poderiam ser evitadas com prevenção ou intervenção precoces (fig. 5). As idades mínimas de ocorrência desses danos também se mostraram prematuras, assim como referido na África,83 com idade mínima de 21 anos para queratoses actínicas, 6 anos para elastose solar e 23 anos para câncer da pele.
Na população negra com albinismo da África, os danos actínicos ocorrem em crianças pequenas. CPNM, incluindo CBC e CEC, são comuns entre o grupo suscetível com albinismo. Esses cânceres aumentam a morbimortalidade, particularmente nas regiões equatoriais, são desfigurantes e dispendiosos de tratar. Estudos no oeste, leste e sul da África revelam a extensão da vulnerabilidade dos afetados pelo albinismo.27,96 Diversos estudos documentaram alta frequência de queratoses actínicas e cânceres da pele nesses pacientes,24,27,68,82,97 particularmente em comparação com a baixa prevalência de câncer da pele na população negra normalmente pigmentada da África, em quem carcinomas cutâneos são raros.98–103 As condições de clima quente e as atividades agrícolas nessa comunidade limitam o uso de roupas de proteção solar de qualidade, e esse fato em si pode aumentar a taxa de câncer da pele.87,88 Como já foi enfatizado em relatos prévios,24,27,98 essa relação parece ser confirmada por estudos de populações albinas em que a frequência de alterações cutâneas malignas é muito maior naqueles que vivem em regiões equatoriais do que naqueles que vivem a certa distância do Equador.
Estudo realizado por Lookingbill et al., que envolveu 164 albinos da zona rural da África equatorial (norte da Tânzania), revelou que, com exceção de quatro bebês, todos os pacientes tinham pele queimada pelo sol. Foi observada alta frequência de queratoses actínicas e câncer da pele nos adultos, mas também danos actínicos na pele de crianças pequenas. Rugas no dorso das mãos e elastose solar na região cervical posterior foram quase universais em pacientes com mais de 10 anos de idade. Queilite actínica também estava presente em muitas crianças e em 93% dos pacientes com mais de 10 anos de idade. O paciente mais novo com queratoses actínicas tinha 8 anos de idade. Em pacientes com mais de 20 anos de idade, 91% apresentavam queratoses actínicas, enquanto em pacientes com mais de 30 anos, 100% foram afetados.83
Recente estudo realizado no Quênia (localizado ao longo do Equador) envolvendo 151 albinos revelou a presença de lesões cutâneas graves em 80% dos pacientes. A faixa etária mais frequente foi de 21‐30 anos. Frequência de lesões cutâneas pré‐malignas e malignas: queilite actínica (18%), elastose solar (12%), queratose actínica (37%), câncer da pele (13%).104 Por outro lado, avaliação prospectiva de 64 pacientes albinos franceses revelou história médica pregressa de carcinoma cutâneo em três indivíduos adultos (4,6%). Queratose actínica foi encontrada em 9% dos pacientes.42 Poucos pacientes desse estudo europeu declararam queimaduras solares, o que confirma nível satisfatório de proteção solar. De modo semelhante, a caracterização dermatológica em albinos italianos envolvendo 200 pacientes revelou a presença de queratoses actínicas em três pacientes (1,5%) e câncer da pele (melanoma) em um.105 Isso pode ser devido à menor exposição ao sol nas latitudes europeias.
Câncer da pele em albinosO câncer da pele é a malignidade mais comum entre os caucasianos. Representa aproximadamente 20%‐30% de todas as neoplasias em caucasianos e 1%‐2% naqueles com pele pigmentada.101 O câncer da pele é uma das principais causas de morbidade e mortalidade em albinos que desenvolvem lesões pré‐malignas e malignas em uma idade mais jovem e sofrem de câncer da pele avançado na terceira a quarta décadas de vida.24,27 Estudos anteriores da Nigéria97 e da Tanzânia102 relataram que apenas alguns albinos sobreviveram além dos 30 anos. Por volta da terceira década de vida, muitos albinos negros na África terão desenvolvido CECs potencialmente fatais,7,69 mas, se diagnosticado em estágio inicial, o CEC é curável por excisão cirúrgica.
Estudos mostram que o risco de CECs em albinos negros é 1.000 vezes maior do que na população geral, e a cabeça e o pescoço são as regiões mais frequentemente afetadas.63,69,75 O CEC é mais frequente, apresenta um curso mais agressivo e tende a ter maior taxa de recorrência em albinos negros do que em pessoas normalmente pigmentadas.7,8,103
Estudo realizado na Nigéria revelou que os albinos representavam 67% dos doentes tratados para cânceres da pele primários em um Hospital Universitário, e que 61% tinham menos de 40 anos.12 A presença de câncer da pele foi investigada em 111 albinos pertencentes à população negra de Johanesburgo, na África do Sul. A taxa global foi de 23%, com aumento do risco com a idade.68 Em sua revisão de 1.000 albinos nigerianos, Okoro não encontrou nenhum paciente com mais de 20 anos de idade livre de lesões de pele pré‐malignas ou malignas induzidas pela radiação solar.27 Achado semelhante também foi relatado por Luande et al. em sua revisão de 350 albinos em Dar es Salaam. Nesse estudo, a idade de pico dos pacientes com câncer da pele avançado foi a 4ª década de vida.24 Estudo realizado na Tanzânia, que envolveu revisão histológica de 134 biópsias de 86 pacientes albinos com diagnóstico de câncer da pele atendidos em centro dermatológico na Tanzânia, revelou que o paciente mais jovem tinha 18 anos e o mais velho, 68 anos, com média de idade de 35 anos.88
No Brasil, temos pouquíssimos estudos que fazem referência aos danos clínicos do albinismo – os únicos dois disponíveis foram realizados na Bahia. Um foi publicado em 2007 e envolveu 40 albinos vinculados à Associação dos Portadores de Albinismo da Bahia. Esse estudo mostrou que 42% dos albinos apresentavam lesões de pele e 47% não usavam protetor solar com regularidade. Proporção significante dos albinos que desenvolveram lesões de pele não usava protetores solares, ou usava irregularmente.44 O outro estudo foi publicado em 2013, retrospectivo, com dados coletados de 22 albinos e 30 não albinos (24‐89 anos) com lesões cancerígenas e 24 albinos sem lesões na pele. A média de idade dos indivíduos albinos com neoplasias foi de 34 anos, contra 65 anos para indivíduos não albinos. Demonstrou‐se relação significativa entre o uso de protetor solar e a ausência de desenvolvimento de tumores cutâneos. Entre os albinos que usavam protetor solar desde a infância, apenas dois (11%) desenvolveram câncer da pele.48
A prevalência de câncer da pele nos pacientes estudados do Programa Pró‐Albino (n = 146) (26%) foi semelhante à encontrada entre albinos por pesquisadores na Tanzânia (25%),83 África do Sul (23%)68 e muito mais alta do que a encontrada na Europa, que foi de 6% na França e de 0,5% na Itália.42,105 Portanto, ao compararmos nossos resultados com os dados da literatura, observamos grande similaridade com os relatos dos estudos na África e expressiva discrepância em relação aos achados dos grupos europeus. Isso demonstra a significativa influência dos fatores ambientais e das condições socioeconômicas e culturais na morbimortalidade associada ao albinismo. Enfoques e abordagens diferentes podem ser necessárias quando levamos em consideração, em especial, as medidas preventivas. Fica evidente a importância fundamental das orientações e atitudes efetivas de proteção solar nas regiões com maior incidência de radiação solar.
Tipos de câncer da pele no albinismoO CPNM corresponde a 90% de todos os cânceres da pele. Os tumores da pele mais frequentem no Brasil e no mundo são o CBC (70%‐80% dos diagnósticos) e o CEC (20%‐25% dos casos). O CBC é de três a quatro vezes mais comum que o CEC na população caucasiana. Ambos apresentam altos percentuais de cura se detectados precocemente, e apenas uma pequena proporção se torna letal. Assim, entre os tumores da pele, são os cânceres de maior incidência e mais baixa letalidade.89,106–109
Estudo retrospectivo envolvendo revisão dos registros de pacientes, em geral, com CPNM primários, realizado na Santa Casa de São Paulo, revelou que, do total de 945 pacientes, 82% apresentaram diagnóstico de CBC e 18% de CEC. Os locais do corpo mais acometidos foram: cabeça e pescoço, com 81% dos casos, tronco, com 11% dos casos, acompanhados pelos membros, com 8% (dados não publicados). Em contraste, estudos africanos revelam o CEC como a malignidade cutânea mais comumente observada em albinos.11,12,27,68,69,97,110 Estudo com albinos africanos revelou prevalência de CECs em relação à CBCs, numa relaçãode 1,2:1. Cabeça e pescoço foram os locais mais comumente acometidos pelo câncer da pele (56%).88 Estudos anteriores também relataram predominância de CECs em albinos, com CECs ocorrendo três a seis vezes mais que CBCs.11,12,68,97,111 Estudo de revisão de 775 africanos normalmente pigmentados e 18 albinos africanos com tumores malignos de pele mostrou que o CEC foi o tipo de tumor mais comum, com localização preferencial na região da cabeça e pescoço.97 Na África do Sul, em um estudo com 111 albinos de etnia negra, a cabeça foi o local mais comumente afetado e o CEC foi muito mais comum que o CBC. Nenhum melanoma foi detectado.68
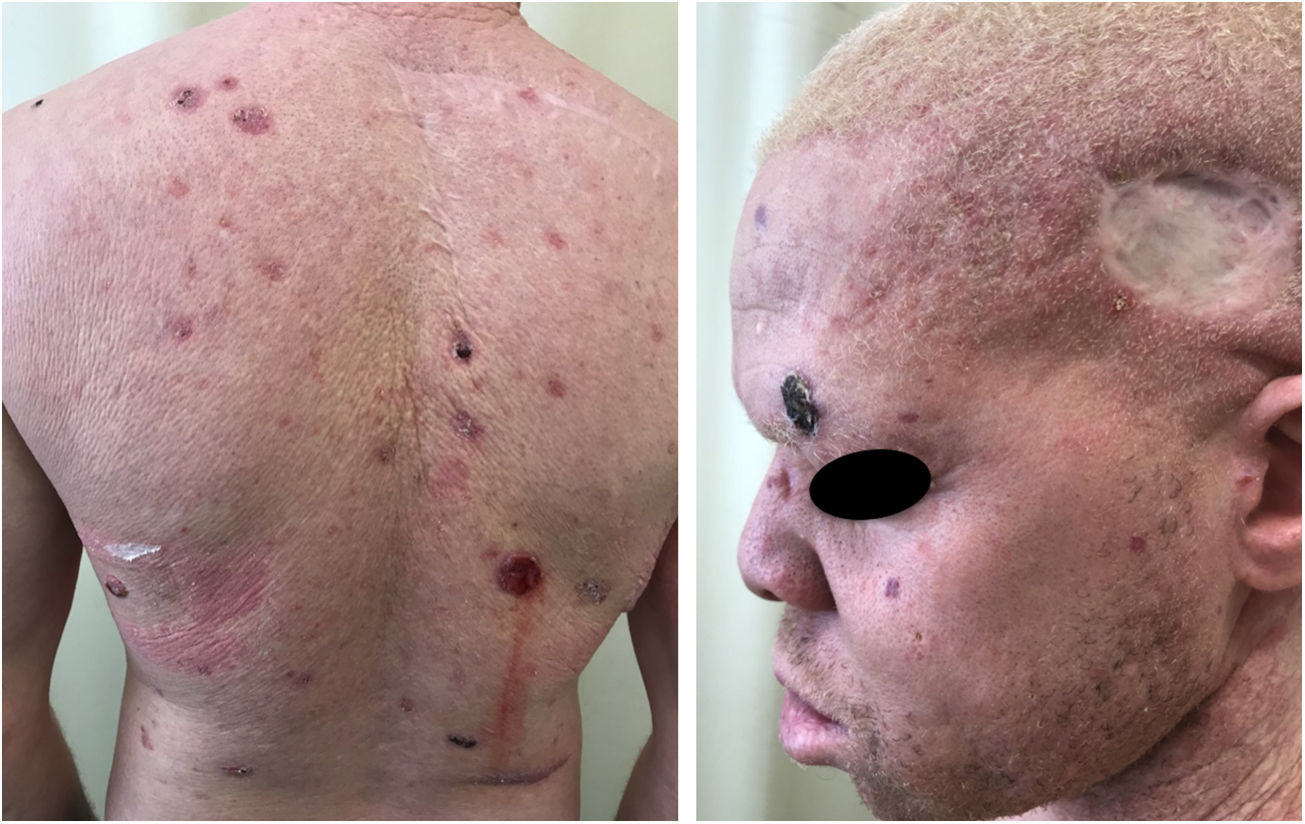
No estudo referido com os pacientes do Programa Pró‐Albino, dos 37 (26% da amostra; n = 146) pacientes com história prévia ou atual de câncer da pele, foi possível a identificação do tipo histológico em 29 deles: 62% CBC, 51% CEC e 7% melanoma, em uma proporção CBC/CEC de 1,2:1. Essa proporção é um pouco diferente da descrita para a população não albina, porém com predomínio mantido de CBC em detrimento do CEC. Desses pacientes, 14% apresentaram os dois tipos de carcinoma (CBC e CEC). Alguns pacientes apresentavam múltiplos tumores ulcerados (figs. 6, 7 e 8). A localização dos tumores foi preferencialmente na cabeça e pescoço (43%), seguida do tronco (37%) e membros (20%), reafirmando a tendência de maior prevalência nas áreas mais expostas ao sol.11,12,24,68,83,96,97,104,110 De maneira semelhante aos nossos resultados, outro estudo realizado no Brasil, na Bahia, revelou que, dos albinos com câncer da pele (n = 22), 56% apresentaram CBC.48
O predomínio relativamente alto de CECs sobre CBCs nos estudos africanos pode ter sido devido ao pequeno tamanho amostral (quatro estudos tinham menos de 20 pacientes). A maioria desses estudos também foi baseada em biópsias excisionais de tumores avançados. O pequeno CBC de crescimento lento pode ter sido perdido em estudos anteriores. Biópsias foram obtidas de pacientes submetidos a exames dermatológicos de rotina em apenas um dos estudos, que revelou prevalência basicamente proporcional entre CEC e CBC (1,2:1),88 assim como visto em nosso estudo, em que a proporção de CEC e CBC foi invertida (1:1,2), mas muito semelhante do ponto de vista quantitativo. Com base nessas informações, sugere‐se que CPNM são predominantes nos albinos e que a proporção de CECs e CBCs parece ser quase idêntica.
Na África, os albinos negros estão frequentemente sujeitos à discriminação por causa das crenças supersticiosas e do estigma associado à condição.62 Os albinos são muitas vezes rechaçados por suas comunidades, com consequente atraso em procurar e obter tratamento médico, até o curso tardio de quaisquer lesões actínicas pré‐malignas ou malignas. Assim, no momento do diagnóstico, o CEC em albinos africanos é muitas vezes avançado.12,62 Tem sido relatado que, em média, os albinos negros na África buscam tratamento 14‐26 meses após o início de qualquer lesão actínica.12,69,88,97,111 Infelizmente, cerca de 40% desses albinos com câncer da pele não completam o tratamento em razão de problemas financeiros11 ou, devido à distância das instalações médicas, têm seu seguimento perdido. Essas podem ser as razões pelas quais os CECs são mais frequentes e tendem a ter maior taxa de recorrência em albinos negros na África do que em pessoas normalmente pigmentadas.7,8,103
Estudo recente realizado no Quênia revelou que o CBC foi mais comum que o CEC em albinos.104 As menores taxas de CEC foram atribuídas ao tratamento precoce das queratoses actínicas, impedindo a transformação maligna para CEC. Sabidamente, não há correlação entre queratoses actínicas e CBC. Os achados enfatizam, portanto, a importância do diagnóstico e do tratamento precoces das lesões pré‐malignas, o que pode ser facilmente atingido por meio dos programas assistenciais direcionados a essa população. Os tratamentos preferencialmente instituídos em nosso programa para as lesões pré‐malignas (queratoses actínicas) são a crioterapia e a quimioterapia tópica com 5‐fluorouracil (figs. 9 e 10), intervenções relativamente simples, efetivas e de baixo custo.
Os objetivos do manejo do câncer da pele no campo da saúde pública são redução da incidência, detecção precoce e tratamento imediato da doença quando esta ocorre. Precauções universais contra a exposição solar devem ser introduzidas no início da infância e continuar ao longo da vida, devendo‐se incorporar a redução de atividades ao ar livre durante os horários de pico da luz solar (10‐16h), o uso de roupas de proteção para cobrir tanto a pele quanto possível, chapéus de abas largas, óculos e uso de filtro solar para a pele exposta e lábios.62,76,112 Com base nessas considerações, o papel do dermatologista é evidente no manejo dessa condição e, particularmente, na triagem destinada a detectar cânceres da pele precoces.
Estudos na África revelam que poderia ser possível reduzir a prevalência de carcinomas cutâneos em albinos12 se a equipe de saúde pública fosse disponibilizada regularmente para visitar aldeias remotas a fim de fazer o rastreamento de lesões malignas e pré‐malignas na população albina e educá‐la sobre os efeitos nocivos da exposição à radiação solar. Isso precisaria ser complementado por centros médicos, onde o tratamento precoce do câncer pudesse ser feito26 e pelo estabelecimento de grupos de apoio educacional. Outros estudos que avaliam o impacto dos programas assistenciais aos albinos na África revelam aumento na expectativa de vida, devido a uma melhor conscientização e ao tratamento precoce do câncer da pele.83,113
A utilização sustentada e em quantidade suficiente de protetor solar e demais medidas fotoprotetoras é fundamental no manejo preventivo dos danos actínicos e do câncer da pele nos albinos.76,112 O uso do protetor desde a infância reduz em até aproximadamente 78% a chance de desenvolver câncer da pele na população geral,114 e essa redução provavelmente é ainda mais significativa nos albinos. Observamos na prática uma grande dificuldade dessa população na aquisição de produtos relativos à fotoproteção, por total falta de acesso a recursos. Seria de fundamental importância que o SUS fornecesse gratuitamente esses insumos à população albina, o que inclusive reduziria gastos secundários com o tratamento do câncer cutâneo, custos relacionados ao afastamento do trabalho e a morbimortalidade associados.
A comunicação em saúde também tem se mostrado efetiva na redução da morbimortalidade associada ao albinismo.26,102,113 Informações relevantes sobre as medidas preventivas devem ser feitas em cada consulta, e também é producente a organização de encontros com os pacientes, nos quais essas questões e demais problemas relacionados ao albinismo possam ser expostos e discutidos amplamente. Fica clara a importância da comunicação nas escolas e as orientações específicas em relação às atividades profissionais, visando minimizar a exposição solar. Defendemos uma abordagem de aprendizagem social e interativa para programas de extensão, grupos de apoio e workshops focados na gestão do albinismo.
A prevalência estimada de albinismo sugere a existência de número significativo de pessoas vivendo com albinismo no Brasil. As evidências demonstram que uma grande proporção desses indivíduos vive em precárias condições socioeconômicas e com demanda de serviços sociais e de saúde, deixando clara a falta de assistência aos afetados. Esses fatos reiteram a necessidade de maior conscientização e intervenções de saúde pública para o albinismo.
Questões psicológicas e sociais: estigma, preconceito e discriminaçãoAlém das preocupações com a saúde física, os portadores de albinismo também precisam lidar com desafios psicológicos e sociais. Na Nigéria, um estudo coletou relatos de pessoas com albinismo. Esses indivíduos afirmaram afastar‐se de situações sociais a fim de evitar serem notados. Eram mais instáveis emocionalmente e tinham personalidades menos assertivas do que pessoas sem albinismo. Além disso, consideravam a sociedade indelicada e sentiam‐se rejeitados, mesmo que tivessem amigos próximos.112 Grande parte da discriminação social na África parece derivar da falta de educação das comunidades sobre a etiologia do albinismo. Há uma consciência limitada de sua herança genética e, portanto, mitos e superstições tradicionais são numerosos.22 Por exemplo, algumas dessas crenças ligam o albinismo à concepção (culturalmente inaceitável) durante a menstruação ou consideram o albinismo uma punição dos deuses pelos erros cometidos por um ancestral.27 Devido a essa discriminação socialmente enraizada, a qualidade de vida das pessoas com albinismo pode estar comprometida. Por exemplo, é mais provável que abandonem a escola e enfrentem mais dificuldades no emprego e no casamento em comparação com a população geral. Além disso, seus familiares também podem sofrer discriminação da comunidade. À luz dos mitos tradicionais sobre a etiologia do albinismo, as mães de crianças afetadas podem estar sujeitas a grande estigma e sofrimento psicológico.22,26,28,102,115,116 No Brasil, por total desconhecimento, esse sofrimento envolve, por exemplo, questionamentos sobre a paternidade no momento do nascimento de uma criança albina em família de ascendência negra ou parda, o que faz com que a mãe e a criança padeçam de preconceitos dentro da própria família e na comunidade em geral.
Os indivíduos com albinismo também enfrentam discriminação social como resultado de sua diferença na aparência. Estudos revelam que a maioria dos países relata falta de conhecimento entre o público em geral. Mostram também que muitas pessoas com albinismo não entendem completamente sua própria condição. Essa discriminação social é vista como obstáculo para construir relacionamentos e encontrar/manter uma ocupação. Assim, a maioria das pessoas com albinismo geralmente apresenta menor status econômico em sua sociedade. À luz dessas dificuldades, não é surpreendente que muitas pesquisas tenham relatado abusos e problemas psicológicos nessa população.26 Não temos estudos específicos em relação a esses fatores no Brasil; no entanto, a experiência adquirida no Programa Pró‐Albino e o contato com histórias diversas revelam que os albinos brasileiros enfrentem problemas semelhantes. Está entre os objetivos do Programa trabalhar essas questões, a fim de minimizar o estigma e o preconceito e promover a inclusão social.
O albinismo é um distúrbio que afeta os indivíduos e suas famílias do ponto de vista médico, social e psicológico. Para alguns, esses últimos problemas podem ser um fardo maior do que as queixas médicas. Embora baixo em comparação com outras grandes questões de saúde, o número de indivíduos afetados e o número ainda maior de pessoas afetadas indiretamente qualificam o albinismo como um problema de saúde pública que merece maior atenção, principalmente para aumentar a conscientização e a informação sobre essa condição.
DiagnósticoO diagnóstico do albinismo resulta de observações clínicas e análise genética molecular, a partir dos seguintes fatores:
- •
Exame físico completo, que inclui a verificação da pigmentação de pele, cabelo e olhos;4,5
- •
Exame ocular meticuloso, que inclui a avaliação de possível nistagmo, estrabismo, déficts de refração, fotofobia e transiluminação da íris. Realiza‐se também a inspeção visual da retina a fim de determinar se há sinais de desenvolvimento anormal;117
- •
Comparação da pigmentação do paciente albino com a de outros membros da família;
- •
Revisão do histórico familiar e pessoal, incluindo a existência de sangramento contínuo, hematomas excessivos, alterações intestinais, pulmonares e neurológicas ou infecções de repetição.
Com base nos achados capilares e cutâneos (hipopigmentação):
- •
Síndromes AOC;
- •
Síndrome de Hermansky‐Pudlak;
- •
Síndrome de Chediak‐Higashi;
- •
Síndrome de Angelman e síndrome de Prader‐Willi;
- •
Síndrome Vici: transtorno autossômico recessivo que cursa com ausência de corpo caloso; hipopigmentação dos cabelos e da pele, microcefalia, imunodeficiência, anormalidades cardíacas, déficit de crescimento, catarata, fissura labiopalatina e anormalidades neurológicas;
- •
Síndrome de Waardenburg tipo II: mutação do gene autossômico dominante MITF, cursando com hipopigmentação heterogênea da pele, mechas brancas ou cabelos grisalhos prematuramente, heterocromia da íris e perda auditiva neurossensorial;
- •
Síndrome da albino‐surdez de Tietz: mutação do gene autossômico dominante MITF, cursando com sobrancelhas e cílios brancos, hipopigmentação da íris, acuidade visual normal e perda auditiva neurossensorial;
- •
Síndrome de Griscelli: defeitos autossômicos recessivos na miosina, bem como em seus receptores e ligantes; os melanócitos não transferem os melanossomas para os dendritos e queratinócitos periféricos, levando à atenuação da cor da pele e do cabelo; apresenta‐se com hipopigmentação, cabelos grisalhos prateados, imunodeficiência, diminuição da acuidade visual com movimentos oculares móveis, pancitopenia, síndrome hemofagocítica e desmielinização cerebral.118
Por meio do diagnóstico genético molecular, o tipo de albinismo e a herança genética podem ser determinados. A análise genética torna possível, ainda, o adequado aconselhamento genético e o diagnóstico precoce das formas sindrômicas (Hermansky‐Pudlak e Chediak‐Higashi), que podem apresentar‐se inicialmente como as formas não sindrômicas e desenvolver complicações graves em idades mais tardias – complicações essas que podem ser prevenidas com orientações e intervenções terapêuticas precoces.4,5,119,120
A consulta genética antes dos anos férteis é benéfica para os pais de crianças albinas que consideram futuros filhos, para o paciente com albinismo e seus irmãos. O albinismo é uma condição homozigótica obrigatória com 100% de chance de transmitir seu gene defeituoso. O teste genético coordenado do parceiro não afetado é possível se a variante patogênica for conhecida. Isso confirmará que os descendentes têm o potencial de herdar a condição, se o parceiro for portador da mesma variante patogênica, ou apenas portadores obrigatórios se o parceiro tiver apenas genes do tipo selvagem. Um casal que já teve um filho albino tem 25% de chance de ter outro filho com albinismo, 50% de chance de gerar filhos portadores do gene e 25% de ter filhos não portadores. Assim, é suposto que se um dos pais não for albino, a chance de uma segunda prole albina é de 50% após uma descendência albina confirmada. É importante saber que os irmãos não albinos têm 67% de chance de serem portadores antes que eles considerem ter filhos. É digno de nota que, se dois pais carregam genes para diferentes tipos de albinismo, nenhuma criança nascerá com albinismo, mas as crianças correm o risco de serem heterozigotas para ambos os alelos mutantes.118
Em resumo, o diagnóstico genético é de fundamental importância na abordagem dos pacientes albinos. Por meio da pesquisa molecular, poderemos realizar a classificação dos subtipos, o que não é possível unicamente pela avaliação clínica fenotípica, diagnosticar os casos não evidentes clinicamente, promover aconselhamento genético adequado e identificar as formas sindrômicas.
TratamentoPor ser um distúrbio genético, o albinismo não tem cura. O tratamento se concentra na realização de cuidados oftalmológicos adequados e no acompanhamento cutâneo em busca de sinais de anormalidades e prevenção do dano solar. O tratamento geralmente inclui:
Cuidados oculares: avaliação oftalmológica nos primeiros meses de vida, exame oftalmológico periódico, lentes corretivas, fisioterapia ocular, intervenções cirúrgicas quando necessárias, orientações para aprendizagem‐auxílios de ensino e considerações especiais na sala de aula (material de leitura de alto contraste, textos e planilhas impressas, configurações de ampliação em computadores, entre outros). Essa abordagem ajudar a superar os atrasos educacionais associados aos déficits visuais;117,118,121
Cuidados cutâneos e prevenção do câncer da pele: orientações quanto à prevenção dos danos actínicos e avaliação clínica e dermatoscópica cutânea periódica para detecção de câncer da pele ou lesões precursoras. Intervenções, como aplicação de nitrogênio líquido, quimioterapia tópica, curetagem, eletrocauterização e cirurgia, são realizadas quando necessário.
Não há substituto para a proteção solar ao longo da vida no albinismo, e sua importância não pode ser superestimada. Os indivíduos devem ser informados sobre evitar a exposição prolongada à luz UV, a exposição direta em horários críticos de incidência de radiação (10‐15h) e a evitar medicamentos que aumentem a fotossensibilidade. Qualquer atividade ao ar livre, por mais breve que seja, deve ser precedida da aplicação de protetor solar (FPS 30+) com reaplicação liberal e frequente (a cada 2 horas) quando sob o sol. Proteção adicional deve ser realizada com o uso de roupas de proteção, chapéus e óculos. Autoexame e autoeducação sobre os critérios para câncer da pele e encaminhamento imediato ao dermatologista para quaisquer lesões suspeitas devem ser realizados. O acompanhamento com o dermatologista deve ser precoce (infância) para esclarecer o benefício e as opções de proteção solar.11,104,118
Formas sindrômicas: pacientes com as síndromes de Hermansky‐Pudlak ou Chediak Higashi geralmente requerem cuidados periódicos especializados para atender às necessidades médicas e prevenir complicações.5,21,118
Modalidades terapêuticas diretas (em vias de estudo e comprovação): a nitisinona desencadeia o acúmulo de tirosina em modelos sanguíneos e de ratos, sugerindo que poderia melhorar a pigmentação em indivíduos AOC1B, mas um ensaio clínico ainda está em andamento. Aminoglicosídeos são uma terapia potencial e não confirmada. Apesar dos relatos, a L‐DOPA não resultou em nenhuma melhora na acuidade visual em um estudo com 45 pacientes. Vírus adeno‐associados (AAV) vetores são uma potencial terapia gênica introduzindo uma cópia funcional do gene da tirosinase em pacientes AOC1 e OA1.122,123
PrognósticoA expectativa de vida da população com AOC não sindrômica é comparável à população geral. Há um aumento do risco de mortalidade devido ao câncer da pele. Esse risco muda com base na quantidade de exposição solar relativa em uma área geográfica e certos problemas socioeconômicos. As questões socioeconômicas incluem acesso restrito a protetor solar, educação limitada sobre medidas de proteção solar, diferenças culturais na indumentária, acesso limitado aos profissionais de saúde para vigilância, que leve à apresentação tardia e tratamento tardio, incapacidade de cumprir ou de completar os cursos de tratamento.
Em regiões com problemas socioeconômicos, geralmente há um estigma palpável associado ao albinismo, e os indivíduos com esse distúrbio genético podem ser vítimas de perseguição, preconceito, violência e exclusão social.
Albinos têm inteligência normal em comparação com a população em geral. Há algum atraso na maturação visual, e isso pode levar a atrasos educacionais se as questões oculares não forem abordadas com antecedência suficiente. Além disso, a baixa autoestima e a alienação social podem levar a sentimentos de isolamento e depressão. Os albinos têm uma taxa aumentada de distúrbio de déficit de atenção.11,118,121
Considerações finaisMedidas para prevenir e controlar o câncer da pele em albinos devem incluir a instituição de programas médicos de rastreio com vistas a identificar lesões cutâneas actínicas potencialmente malignas e a detecção precoce do câncer, bem como disponibilizar medidas eficazes e imediatas de tratamento dermatológico e psicológico.63 Embora a causa mais comum de morte precoce em albinos seja o câncer da pele, os pacientes acometidos podem ter uma expectativa de vida normal com a instituição de cuidado adequado da pele.7
Independentemente da localização geográfica, o albinismo pode fazer com que os pacientes se tornem estigmatizados e isolados. Iniciativas para a conscientização sobre o albinismo são de extrema importância em todos os lugares do mundo. A qualidade de vida de um paciente pode ser notavelmente melhorada com acesso à saúde, apoio e orientação adequada. A atenção em relação ao AOC objetiva reduzir a morbimortalidade pelo câncer da pele avançado e afecções oculares. Isso é possível por meio de ações de prevenção primária dermatológica e oftalmológica e medidas de prevenção secundária. Com a assistência adequada ao paciente albino, podemos modificar o curso da doença, tratar as comorbidades quando presentes, bem como compreender melhor a afecção e a forma que incide no Brasil, promovendo assim benefícios ao paciente e a seus familiares, que muitas vezes não têm informações adequadas e desconhecem completamente sua própria condição. Por meio da informação, conseguimos também minimizar o estigma e o preconceito relacionados à doença.
Suporte financeiroNenhum.
Contribuição dos autoresCarolina Reato Marçon: Análise estatística; aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Marcus Antonio Maia de Olivas Ferreira: Participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito.
Conflito de interessesNenhum.
Questões- 1.
A principal causa de morbimortalidade para os albinos que vivem em regiões geográficas com alta incidência de radiação solar é:
- a)
Melanoma
- b)
Baixa acuidade visual
- c)
Câncer dos ceratinócitos
- d)
Complicações sistêmicas
- 2.
As principais formas sindrômicas de albinismo são:
- a)
Waardenburg e Prader‐Willi
- b)
Hermansky‐Pudlak e Chediak‐Higashi
- c)
Chediak‐Higashi e Angelman
- d)
Hermansky‐Pudlak e Waardenburg
- 3.
Existem atualmente 19 genes relacionados às diferentes apresentações clínicas do albinismo, incluindo sete para o albinismo oculocutâneo. Os genes responsáveis pelos quatro principais tipos de albinismo não sindrômico‐AOC1, AOC2, AOC3, AOC4‐são, respectivamente:
- a)
TYR, AOC2, TYRP1e SLC45A2
- b)
TYRP1, AOC2, SLC24A5e C10orf1
- c)
TYR, AOC2, SLC45A2 e C10orf1
- d)
TYR, AOC2, TYRP1e SLC24A5
- 4.
Os dados epidemiológicos atualmente disponíveis revelam que a incidência do albinismo é provavelmente maior no seguinte continente:
- a)
América do Sul
- b)
Ásia
- c)
África
- d)
América do Norte
- 5.
Em relação aos tipos genéticos de albinismo oculocutâneo (AOC) mais prevalentes no mundo, podemos considerar:
- a)
AOC1 e AOC3
- b)
AOC3 e AOC4
- c)
AOC2 e AOC4
- d)
AOC1 e AOC2
- 6.
Os melanócitos têm origem ectodérmica, na crista neural, evoluindo com migração cutânea ou extracutânea. Alguns genes controlam a proliferação e a diferenciação das células da crista neural e regulam a migração dos melanócitos precursores para suas posições finais. Os locais de migração extracutânea dos melanócitos e o principal gene regulador do desenvolvimento, função e sobrevivência dos melanócitos são, respectivamente:
- a)
Olhos, leptomeninge, pleura e MC1R
- b)
Olhos, leptomeninge, hipotálamo e MITF
- c)
Olhos, cóclea, leptomeninge e MITF
- d)
Olhos, adrenal, leptomeninge e SCF/KIT
- 7.
Quanto à fisiopatologia do câncer da pele no albinismo, são fatores diretamente envolvidos e correlacionados com a mutação genética e sua interação com a radiação ultravioleta:
- a)
Quantidade reduzida de melanina, diminuição proporcional ou ausência de eumelanina, disfunção da p53 e estresse oxidativo
- b)
Quantidade reduzida de melanina, diminuição proporcional ou ausência de feomelanina, estresse oxidativo e imunossupressão
- c)
Quantidade reduzida de melanina, aumento proporcional de eumelanina, inflamação e descontrole do ciclo celular/apoptose
- d)
Quantidade reduzida de melanina, aumento proporcional de feomelanina, hiperfunção da p53 e ineficiência dos mecanismos de reparo do DNA
- 8.
Os danos actínicos mais prevalentes reportados nos albinos brasileiros são:
- a)
Queratoses actínicas, lentigos e carcinoma espinocelular
- b)
Queratoses actínicas, elastose solar e carcinoma basocelular
- c)
Elastose solar, carcinoma espinocelular e melanoma
- d)
Elastose solar, queratoses actínicas e melanoma
- 9.
São fatores de risco atualmente considerados para o câncer da pele nos albinos:
- a)
Exposição solar sem proteção, histórico de queimadura solar e idade
- b)
Exposição solar sem proteção, tonalidade do cabelo e idade
- c)
Histórico de queimadura solar, cor da íris e origens étnicas
- d)
Tipo genético, queimadura solar e idade
- 10.
Em relação ao aconselhamento genético, as chances de um casal não albino que já tem um filho albino ter outro filho com albinismo e as chances de seus filhos serem portadores do gene são, respectivamente:
- a)
50% e 50%
- b)
50% e 67%
- c)
75% e 50%
- d)
25% e 50%
Agradecemos à Santa Casa de Misericórdia de São Paulo e à Sociedade Brasileira de Dermatologia pelo suporte ao desenvolvimento, atuação e expansão do Programa Pró‐Albino e pelo apoio incondicional a todas as iniciativas voltadas à causa albina e à diminuição da morbimortalidade e melhora da qualidade de vida dos pacientes albinos brasileiros.
Como citar este artigo: Marçon CR, Maia M. Albinism: epidemiology, genetics, cutaneous characterization, psychosocial factors. An Bras Dermatol. 2019;94:503–20.
Trabalho realizado no Ambulatório de Albinismo, Programa Pró‐Albino, Clínica de Dermatologia, Departamento de Medicina, Santa Casa de Misericórdia de São Paulo, São Paulo, SP, Brasil.