O uso tópico de modificadores da resposta imune, como o imiquimode, tem aumentado na dermatologia. Embora seu uso tópico seja bem tolerado, pode estar associado a exacerbações de doenças inflamatórias cutâneas generalizadas, possivelmente pela circulação sistêmica de citocinas pró‐inflamatórias. Relatamos caso de desenvolvimento de pitiríase rubra pilar, dermatose rara eritêmato‐papuloescamosa, em mulher de 60 anos durante tratamento com imiquimode 5% creme para ceratose actínica. Evoluiu com quadro eritrodérmico e ceratodermia palmoplantar, apresentou resolução clínica progressiva após introdução de metotrexato. Ressaltamos a importância do reconhecimento de possíveis reações sistêmicas associadas ao uso tópico do imiquimode.
Pitiríase rubra pilar (PRP) é uma dermatose eritêmato‐papuloescamosa rara, semelhante clínico‐patologicamente à psoríase. De etiologia não estabelecida, embora descrita como autolimitada, pode afetar intensamente a qualidade de vida do paciente.
Foi relatada em três artigos a associação da PRP ao uso de imiquimode no tratamento de ceratoses actínicas e carcinoma basocelular superficial. Relatamos caso de PRP durante uso de imiquimode para ceratose actínica, com boa resposta ao tratamento com metotrexato.
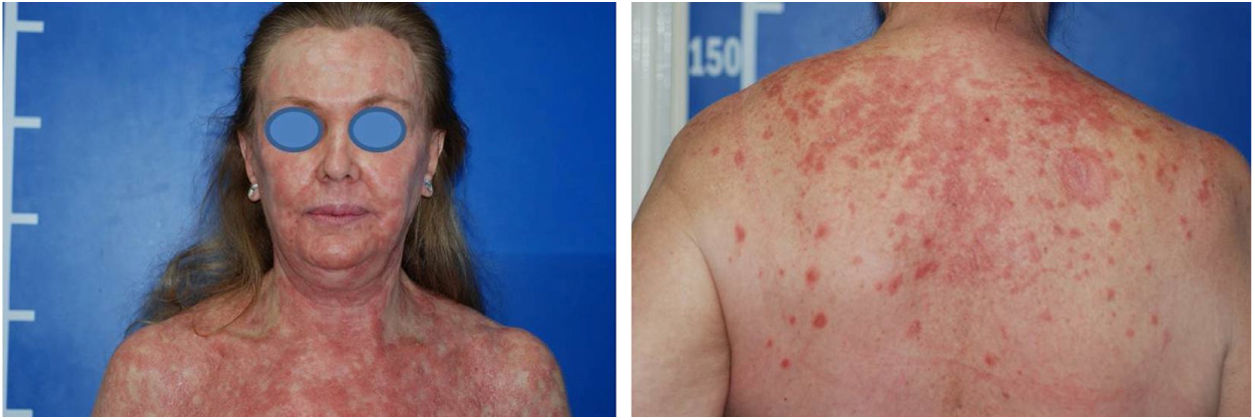
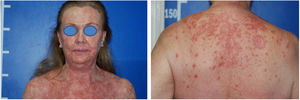
Relato do casoPaciente do sexo feminino, 60 anos, branca, apresentava ceratose actínica havia três meses na região peitoral direita, confirmada por biópsia. Imiquimode creme 5% foi prescrito para o tratamento tópico cinco vezes por semana. Após duas semanas, iniciou quadro de febre, diarreia, mialgia e fadiga associada à exulceração da lesão inicial e surgimento de lesões eritematosas papulodescamativas no couro cabeludo, face e tronco (fig. 1). O tratamento foi suspenso. Exames laboratoriais não evidenciaram alterações.
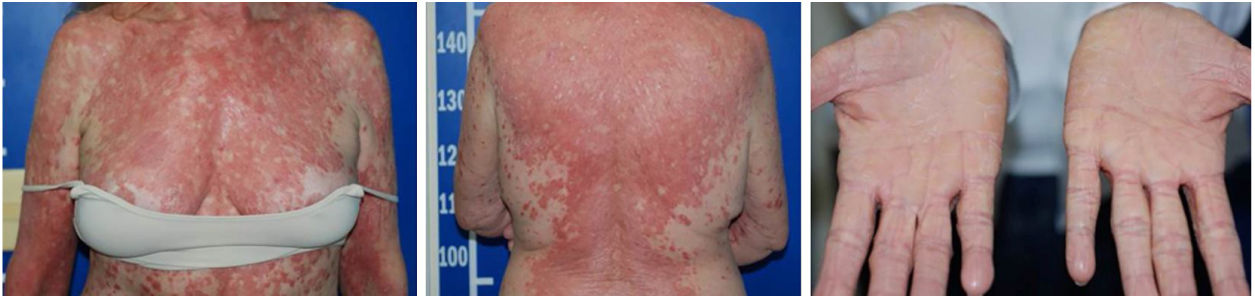
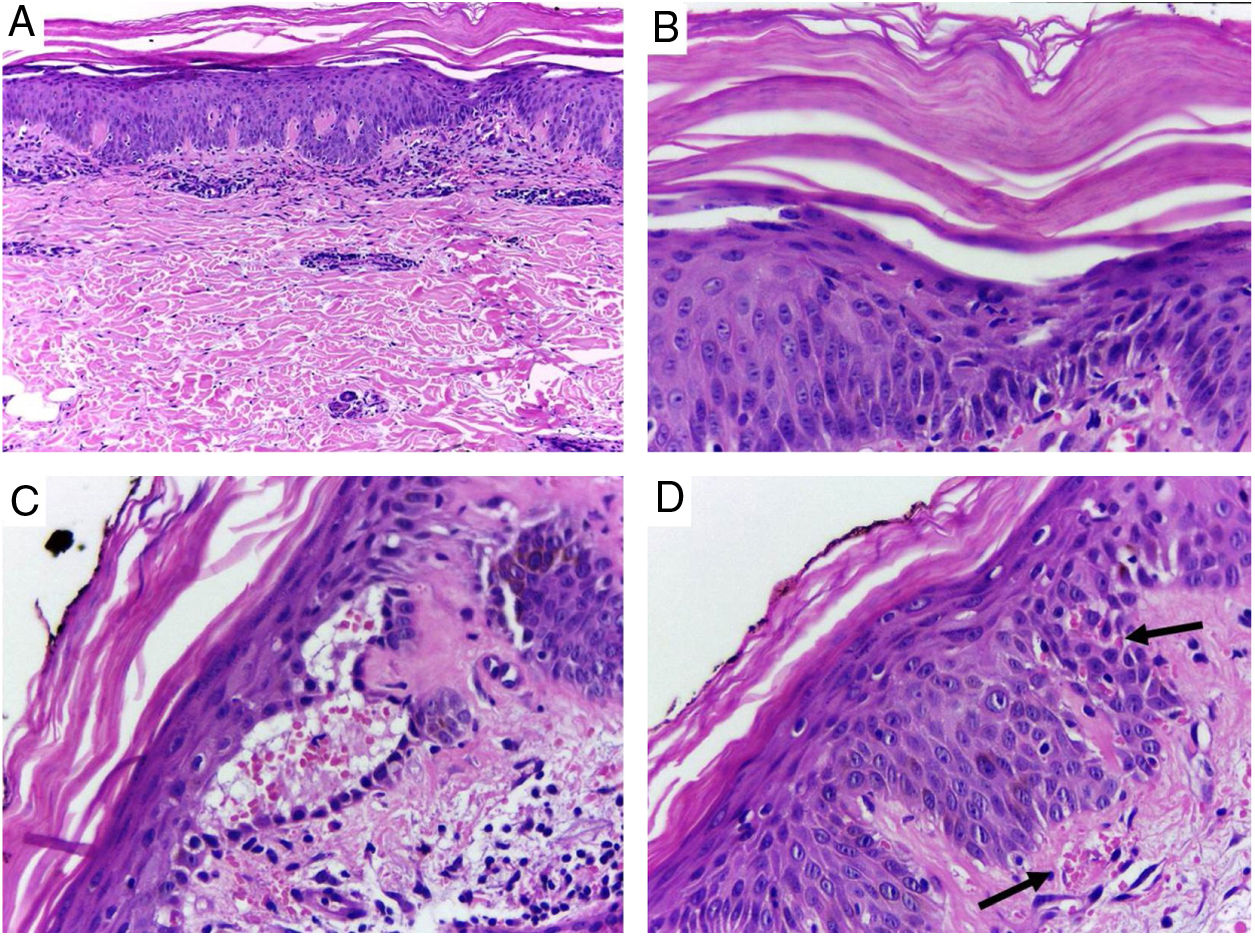
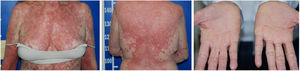
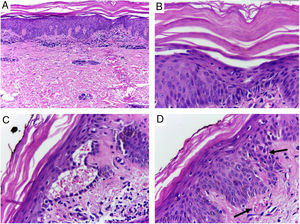
Apesar de introduzido corticoide tópico e anti‐histamínico oral, houve pioria da erupção com espraiamento e confluência das lesões sentido craniocaudal (fig. 2). Feita biópsia de lesões e introduzida prednisona 40 mg/d. Na histologia, observou‐se hiperplasia psoriasiforme da epiderme, hiperparaceratose alternada com ortoceratose, áreas de hipogranulose, moderado infiltrado linfo‐histiocitário perivascular superficial e focos de disceratose acantolítica (fig. 3).
Pele, região abdominal, visão panorâmica: A, hiperceratose, acantose psoriasiforme e moderado infiltrado linfoide perivascular superficial; B, pormenor da imagem anterior, nota‐se hiperparaceratose alternada; C, área de disceratose acantolítica e fenda intraepidérmica suprabasal; D, acentuada congestão (seta) com eliminação transepidérmica de hemácias. Hematoxilina & eosina, aumento original de 100× (A) e 400× (B, C, D).
Após quatro semanas do início da erupção, a paciente apresentava‐se eritrodérmica, com áreas de pele sã, associada a ectrópio e ceratodermia palmoplantar alaranjada. Foi definido o diagnóstico clínico‐histopatológico de (PRP). Metotrexato foi introduzido por via oral, na dose de 15 mg por semana, e o corticoide oral foi retirado gradativamente.
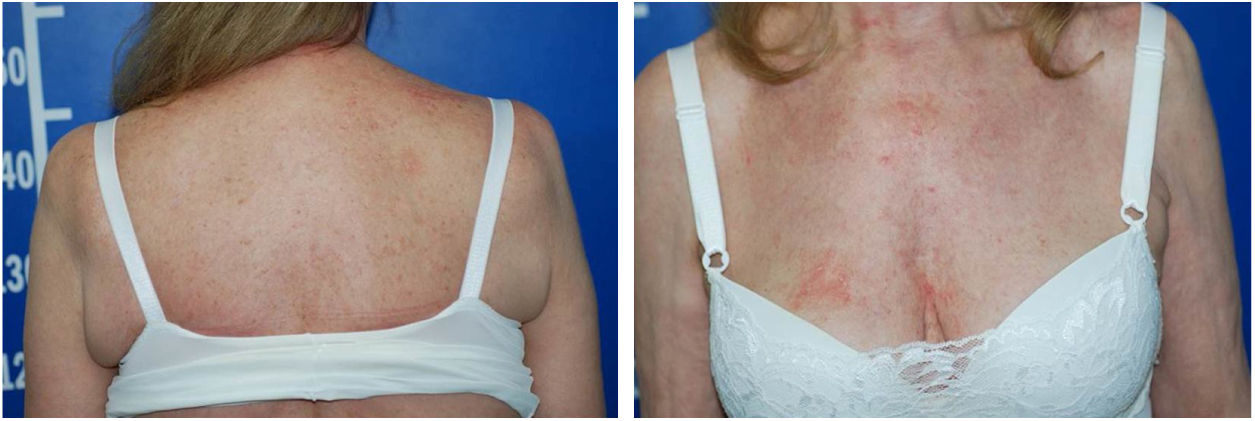
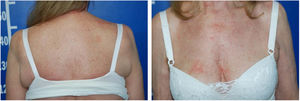
Os exames sorológicos (HIV, hepatites B e C) resultaram negativos, assim como US abdominal e RX de tórax estavam normais. Houve melhoria progressiva do quadro eritrodérmico após três meses, quando foi iniciada a redução do metotrexato. A superfície cutânea normalizou‐se após nove meses do início do quadro (fig. 4).
DiscussãoA PRP é uma desordem rara da queratinização. A forma clássica (Tipo I) ocorre em adultos de ambos os sexos, com erupção de pápulas foliculares que se confluem em placas descamativas eritêmato‐alaranjadas, com espraiamento craniocaudal, geralmente evolui para eritrodermia com ilhotas de pele sã e ceratodermia palmoplantar. São descritas ainda formas atípicas, acometimento de crianças e uma forma associada à infecção pelo HIV.1
A histopatologia evidencia hiperplasia psoriasiforme, hiperceratose folicular, hiperparaceratose alternada com ortoceratose e infiltrado linfocitário perivascular superficial. A ocorrência de disceratose acantolítica, como no presente caso, é comum e pode induzir erros diagnósticos, pela semelhança histológica com doença de Grover, Darier ou pênfigo.2 Magro e Crowson (1997) sugerem que a presença de disceratose acantolítica seja frequente e possa servir como fator preditivo de PRP na diferenciação histopatológica com psoríase.3
Apesar da etiologia não elucidada, uma das principais hipóteses para PRP seria a resposta imune exacerbada a gatilhos antigênicos. Acredita‐se que infecções virais, bacterianas, neoplasias, doenças autoimunes e drogas modificadoras da resposta imune possam desempenhar papel em sua patogênese.1–3 Estudos evidenciam que na PRP, analogamente à psoríase, a via de resposta imune T‐helper 1 (Th1) está ativada com aumento de citocinas pró‐inflamatórias como TNF‐α, INF‐α, IL‐1, IL‐6, IL‐17e IL‐23.4
A ativação da resposta Th1 seria também responsável pela ação deficiente da vitamina A encontrada na pele afetada por PRP. Citocinas inflamatórias alteram a sinalização de receptores retinoides dos queratinócitos, levam à queratinização anormal e hiperplasia epidérmica.3 Dentre as opções terapêuticas para PRP encontram‐se retinoides orais, metotrexato, fototerapia e biológicos com atividade anti‐TNF‐α, anti‐ IL‐17 e anti‐IL‐23.1,2
O imiquimode é um agente estimulador da resposta imunológica, indicado para tratamento tópico de ceratose actínica, carcinoma basocelular superficial e condiloma acuminado. Nos últimos anos, seu uso tem se ampliado para tratamento de outras condições dermatológicas off‐label.5
Como agonista de receptores toll‐like7 (TLR‐7) presentes nas células do sistema imune inato (células dendríticas e macrófagos) e queratinócitos, o imiquimode desempenha ação antitumoral e antiviral. A ligação ao TLR‐7 promove aumento da produção de citocinas pró‐inflamatórias com perfil Th1, como TNF‐α, IFN‐α, IL‐1, IL‐6, IL‐8, entre outras, assim como inibe a via anti‐inflamatória Th2.5
Seu uso tópico é seguro e bem tolerado, com reações locais reversíveis e transitórias, mas efeitos adversos sistêmicos podem ocorrer. Foram descritos sintomas gripais, mialgia, febre, cefaleia e fadiga, reversíveis com a suspensão do medicamento.6 Mais do que à absorção sistêmica do imiquimode, credita‐se à circulação sistêmica de citocinas inflamatórias a etiologia desses efeitos adversos.6
Imiquimode foi associado à exacerbação e ao desencadeamento de erupções cutâneas inflamatórias, como psoríase, dermatite esfoliativa, eritema multiforme, pênfigo e lúpus subagudo.7 Psoríase tem sido induzida por imiquimode tópico em ratos, com aumento de INF‐α e das IL‐1, IL‐6, IL‐17, IL‐23.7
Yang et al. (2008) relataram exacerbação da PRP em paciente de 67 anos sob tratamento com imiquimode tópico 5% para ceratoses actínicas na face e no couro cabeludo. Duas semanas após o início do imiquimode, assim como em nosso relato, o paciente desenvolveu quadro gripal associado ao espraiamento das lesões foliculares eritêmato‐descamativas. Houve melhoria após 26 meses de tratamento com acitretin.8
Gómez‐Moyano et al. (2010) descreveram PRP eritrodérmica em paciente de 56 anos, durante tratamento com imiquimode para CBC superficial no dorso. Como em nosso caso, a histopatologia apresentava focos de disceratose acantolítica. Houve melhoria da PRP após dois meses com acitretin.9
Mesinkovska et al. (2011) publicaram um caso de PRP acantolítica, em paciente de 65 anos, em uso tópico de imiquimode 3,75% para tratamento de ceratoses actínicas. Apresentou melhoria após fototerapia UVB narrowband.10
A relação causal entre imiquimode e PRP permanece desconhecida. O imiquimode pode ter sido gatilho para PRP na medida em que promoveu ativação da via inflamatória Th1 e a circulação sistêmica de citocinas TNF‐α, INF‐α, corroborou a principal teoria para sua patogênese.1,4,5 Sintomas sistêmicos flu‐like ocorreram após uso do imiquimode, sem qualquer evidência de processo infeccioso, configuraram efeito adverso já bem documentado.5,6 Além disso, o uso do metotrexato, com ação antagonista do TNF‐α,4 resultou na regressão das lesões.
O uso de medicamentos com atividade imunológica na dermatologia tem crescido consistentemente. O dermatologista deve estar apto ao reconhecimento de possíveis efeitos colaterais sistêmicos e exacerbação ou deflagração de doenças cutâneas inflamatórias.
Suporte financeiroNenhum.
Contribuição dos autoresOriete Gerin Leite: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; participação efetiva na orientação da pesquisa; revisão crítica da literatura.
Sandra Tagliolatto: Aprovação da versão final do manuscrito; concepção e planejamento do estudo; elaboração e redação do manuscrito; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica do manuscrito.
Elemir Macedo de Souza: Aprovação da versão final do manuscrito; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Maria Letícia Cintra: Aprovação da versão final do manuscrito; elaboração e redação do manuscrito; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Conflitos de interesseNenhum.
Como citar este artigo: Leite OG, Tagliolatto S, Souza EM, Cintra ML. Acantholytic pityriasis rubra pilaris associated with topical use of imiquimod 5%: case report and literature review. An Bras Dermatol. 2020;95:63–6.
Trabalho realizado na Dermoclínica, Campinas, SP, Brasil.