A hanseníase, doença infectocontagiosa ocasionada pelo Mycobacterium leprae, ainda constitui problema de saúde pública no Brasil. Em 2018 foram registrados 28.660 casos novos, o que corresponde a 93% dos pacientes diagnosticados no continente americano. Nesse mesmo ano, Brasil, Índia e Indonésia contribuíram com 80% dos 208.619 casos novos registrados em todo o mundo.1
Para fins operacionais, em 2009 a OMS recomendou classificar a hanseníase segundo o número de lesões cutâneas: paucibacilar (PB), uma a cinco lesões; e multibacilar (MB), mais de cinco lesões.2
O tratamento poliquimioterápico (PQT) recomendado pela OMS em 1982 foi decisivo para a redução global da prevalência da hanseníase. Casos PB são tratados durante seis meses com rifampicina e dapsona; casos MB recebem 12 meses de tratamento com os mesmos fármacos, associados a clofazimina.3
Face ao conhecimento da possibilidade de cura espontânea de casos PB com lesão cutânea única (PB‐LU), em 1998 a OMS recomendou estudos com dose única de rifampicina 600 mg, ofloxacina 400 mg e minociclina 100 mg, associação medicamentosa denominada esquema ROM.4
Um dos primeiros estudos com o esquema ROM foi realizado na Índia, com 1.483 pacientes. Comparou‐se o esquema ROM com o tratamento PQT para casos PB. Nesse ensaio clínico randomizado, 1.381 doentes completaram o estudo e, ao final de 18 meses, verificou‐se a cura clínica de 99,2% dos casos. Não houve diferença entre os índices de cura dos enfermos alocados nos dois esquemas, PQT e ROM.5
No Brasil, no período de outubro de 1997 a novembro de 1998, foi realizado estudo multicêntrico delineado como coorte prospectiva, constituída por 259 pacientes portadores de hanseníase PB‐LU: 75 no estado do Amazonas, 59 em Goiás, 80 no Rio de Janeiro e 45 em Rondônia. Todos foram tratados com o esquema ROM e tiveram mediana de tempo de seguimento de 31 meses. No seguimento, 216 (83,4%) casos foram avaliados como curados.6,7
De acordo com os dados da literatura mundial e os resultados do estudo brasileiro, o Ministério da Saúde do Brasil (MS), em 2002, recomendou o esquema ROM como tratamento alternativo em centros de referência.8
No último guia de controle da hanseníase (MS, 2017) não há referência sobre o tratamento ROM e inexistem explicações sobre sua exclusão.9 Por outro lado, nas recomendações para o tratamento da hanseníase, em 2020, a OMS continua recomendando o esquema ROM.10
Procuramos avaliar a evolução clínica dos 75 pacientes do estado do Amazonas alocados no estudo brasileiro, principalmente com relação à ocorrência de eventos como reações, neurites e retratamento.
Para essa análise, foram realizadas buscas no banco de dados do Sistema de Informação de Agravos de Notificação (SINAN) e seus prontuários. Apenas um prontuário não foi localizado. Procuramos também resgatar pacientes para exame dermatológico, por meio de contato telefônico. Nenhum paciente foi localizado.
Na investigação do banco de dados do SINAM não foi encontrada informação sobre reingresso de pacientes por falha terapêutica.
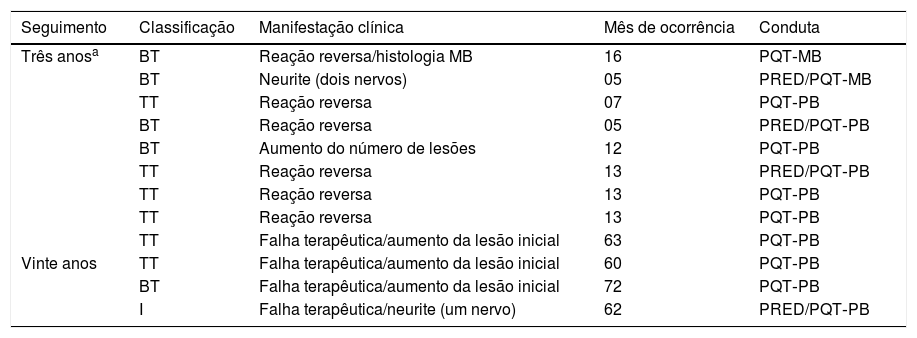
Por meio da análise dos prontuários, verificou‐se que 33 pacientes retornaram ao serviço: 19 com queixas não relacionadas à hanseníase e 14 para reavaliar a enfermidade. De acordo com as informações coletadas, quatro pacientes apresentaram sinais de provável reativação da doença, cinco a seis anos após o tratamento – três casos informavam reativação ou aumento do tamanho da lesão, e um, classificado como indeterminado, desenvolveu neurite (tabela 1). Nos prontuários não havia informações sobre resultados de biópsias ou baciloscopias positivas. Os exames dermatológicos não foram realizados pelos dermatologistas envolvidos na pesquisa. Os critérios de falha terapêutica, após 20 anos, foram exclusivamente clínicos e não tiveram comprovação definitiva da ineficácia do tratamento.
Causas de retratamento de hanseníase lesão única tratados com ROM no estado Amazonas
| Seguimento | Classificação | Manifestação clínica | Mês de ocorrência | Conduta |
|---|---|---|---|---|
| Três anosa | BT | Reação reversa/histologia MB | 16 | PQT‐MB |
| BT | Neurite (dois nervos) | 05 | PRED/PQT‐MB | |
| TT | Reação reversa | 07 | PQT‐PB | |
| BT | Reação reversa | 05 | PRED/PQT‐PB | |
| BT | Aumento do número de lesões | 12 | PQT‐PB | |
| TT | Reação reversa | 13 | PRED/PQT‐PB | |
| TT | Reação reversa | 13 | PQT‐PB | |
| TT | Reação reversa | 13 | PQT‐PB | |
| TT | Falha terapêutica/aumento da lesão inicial | 63 | PQT‐PB | |
| Vinte anos | TT | Falha terapêutica/aumento da lesão inicial | 60 | PQT‐PB |
| BT | Falha terapêutica/aumento da lesão inicial | 72 | PQT‐PB | |
| I | Falha terapêutica/neurite (um nervo) | 62 | PRED/PQT‐PB |
Ressaltamos que o esquema ROM é recomendado pela OMS e deve ser considerado como esquema alternativo para tratamento dos casos PB com lesão única, principalmente nos centros de referência.
Suporte financeiroFundação de Amparo à Pesquisa do Estado do Amazonas (FAPEAM) – bolsa iniciação científica.
Contribuição dos autoresSilmara Navarro Pennini: Concepção e planejamento do estudo; revisão crítica da literatura; obtenção, análise e interpretação dos dados; elaboração, revisão e aprovação da versão final do manuscrito.
Josineide de Oliveira Novo França: Revisão crítica da literatura; obtenção, análise e interpretação dos dados; elaboração e revisão do manuscrito.
Paula Frassinetti Bessa Rebello: Concepção e planejamento do estudo; revisão crítica da literatura; análise e interpretação dos dados; elaboração e revisão crítica do manuscrito.
Sinésio Talhari: Revisão crítica da literatura; análise e interpretação dos dados; elaboração, revisão crítica do manuscrito e aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Pennini SN, França JO, Rebello PF, Talhari S. Single‐lesion paucibacillary leprosy: a retrospective study of 75 cases treated with the ROM scheme. An Bras Dermatol. 2022;97:258–9.
Trabalho realizado na Fundação de Dermatologia Tropical e Venereologia Alfredo da Matta, Manaus, AM, Brasil.