A alopecia areata (AA) afeta principalmente o couro cabeludo, mas pode afetar cílios e pelos corporais. Seu tratamento pode ser tópico (corticoides, minoxidil, antralina, difenciprona) e sistêmico (corticosteroides, azatioprina, metotrexato, ciclosporina e sulfassalazina).1 Há estudos demonstrando benefício da mesalazina2 e, mais recentemente, dos inibidores da Janus Kinase (JAK).3
Até junho de 2022, o Food and Drug Adminstration (FDA) não havia aprovado nenhum tratamento para AA, quando então aprovou o baricitinibe para adultos.4 Até aquele momento, as opções de tratamento eram off‐label,2 e os inibidores da JAK ainda permanecem medicações de difícil acesso em virtude de seu alto custo. Pacientes com doença grave têm benefícios limitados com os tratamentos, e a taxa de recorrência é alta. Por isso, risco‐benefício e segurança dos medicamentos usados devem ser considerados. A AA afeta adultos e crianças, e estima‐se que até 20% dos casos ocorram na infância,5,6 quando tende a ser mais grave e com pior prognóstico.3 Crianças com AA apresentam maiores índices de ansiedade, depressão e diminuição da qualidade de vida.7
Este é um estudo de 18 pacientes, realizado em duas unidades de Dermatologia Pediátrica do Brasil – uma no Hospital Santo Antônio, em Porto Alegre, e outra no Hospital das Clínicas, em Curitiba. O período do estudo, desde a fase de seleção até a avaliação final, deu‐se de janeiro de 2019 a julho de 2020. Dos 18 pacientes, dois não responderam à mesalazina após seis meses de tratamento. Outros dois não puderam finalizar seu acompanhamento e tratamento por motivo de mudança de cidade ou pela pandemia do coronavírus‐19. Assim, 14 indivíduos foram analisados aos 6 e 12 meses após início do tratamento: 10 apresentavam AA em placas com SALT > 40, alopecia universal (AU) ou alopecia total (AT), e quatro com AA difusa. Desses quatro, três tiveram o diagnóstico confirmado por biopsia e um apresentou inicialmente placas, mas evoluiu para difusa. Foram incluídos indivíduos com diagnóstico de AA com SALT ≥ 40 ou com AA difusa, não responsivos ao tratamento tópico e corticoterapia sistêmica, de qualquer sexo, idade entre 2 e 18 anos. O consentimento informado foi obtido de todos os pacientes e/ou de seus responsáveis legais.
Exames laboratoriais foram realizados antes do tratamento, mensalmente nos primeiros seis meses e a cada dois meses até completar 12 meses. Durante o tratamento com mesalazina, os pacientes com teste de tração positivo (indicando doença ativa) utilizaram corticoterapia sistêmica: prednisolona 1mg/kg/dia por cinco dias, com retirada gradual a partir do sexto dia e ao longo de 22 a 30 dias, e manutenção nos finais de semana de 0,5 a 1mg/kg/dia até que o teste de tração fosse negativo. Todos os pacientes do estudo haviam recebido terapia com corticosteroides sistêmicos isoladamente nas mesmas doses descritas por três meses antes de iniciar a mesalazina e não apresentaram sinais de repilação. A mesalazina foi administrada por via oral, na dose inicial de 30mg/kg/dia, dividida em duas doses diárias, aumentada até 50mg/kg/dia.
A resposta ao tratamento foi avaliada por meio de fotografias aplicando a escala SALT.6 A escala varia de zero (ausência de alopecia) a 100 (ausência completa de pelos no couro cabeludo). A resposta ao tratamento foi avaliada aos seis e 12 meses de terapia pela diferença no escore SALT basal (SALT B) e os escores nesses dois tempos (SALT 6 meses; SALT 12 meses). Os pacientes foram classificados em quatro grupos de acordo com o percentual de redução do escore SALT: 5% a 25% (resposta fraca), 26% a 50% (moderada), 51% a 75% (expressiva) e 76% a 100% (notavelmente expressiva).
Para calcular a eficácia do tratamento, foram realizadas comparações das medidas de SALT obtidas por meio do teste t de Student. Os pacientes com AA difusa não puderam ser avaliados com a escala SALT porque essa refere‐se à avaliação em placas. Portanto, o acompanhamento e a melhora foram observados por meio de fotografias (no início, aos seis e 12 meses) e por dermatoscopia procurando pontos pretos, cabelos em ponto de exclamação e pontos amarelos. O grupo com alopecia difusa foi assim classificado: excelente, quando a repilação avaliada pelo exame clínico e dermatoscopia foi maior que 40%; boa, quando foi de 20%‐40%; ruim, quando menor que 10%; e nenhuma resposta, quando sem mudança. Ao comparar resultados dos exames laboratoriais apresentados antes e após o uso da mesalazina, não houve alterações. O SALT basal variou de 40,6 a 100, com média de 86,5 (DP = 22,2). Analisando os resultados, observou‐se eficácia significativa do tratamento com mesalazina tanto aos seis quanto aos 12 meses (tabela 1). A redução média relativa aos seis meses foi de 29,9%, p = 0,003; (intervalo: −67; 0; n = 12), e aos 12 meses foi de 66,8%, p < 0,001 (intervalo: −92,2; −12,0; n = 10). Após 12 meses de terapia com mesalazina, 40% dos pacientes apresentaram resposta altamente expressiva (redução ≥ 76%) – figura 1, 30% tiveram resposta expressiva, 20% resposta moderada e um (10% da amostra) teve baixa resposta à medicação (tabela 2). Os quatro pacientes com AA difusa mostraram melhora significativa e obtiveram excelente resposta aos 12 meses de tratamento (tabela 2).
Resultados dos pacientes aos 6 e 12 meses de tratamento com mesalazina e amplitude no escore
| 6 meses – mudança basal (n = 12) | Basal | 6 meses | 6 meses – mudança basal |
|---|---|---|---|
| Média ± DP | 86,5 ± 22,2 | 60,6 ± 29,8 | −25,8a ± 23,4 |
| Variação | 40,6–100 | 15,2; 100 | −67,2; 0 |
| Redução média (%) | −29,9 |
| 12 meses – mudança basal (n = 10) | Basal | 12 meses | 12 meses – mudança basal |
|---|---|---|---|
| Média ± DP | 83,8 ± 23,6 | 27,8 ± 25,7 | −56,0b ± 28,4 |
| Variação | 40,6; 100 | 0; 88,0 | −92,9; −12,0 |
| Redução Média (%) | −66,8 |
Nota: SALT 100 indica completa ausência de pêlos e SALT 0 indica ausência de perda de pelos no couro cabeludo.
Teste t:
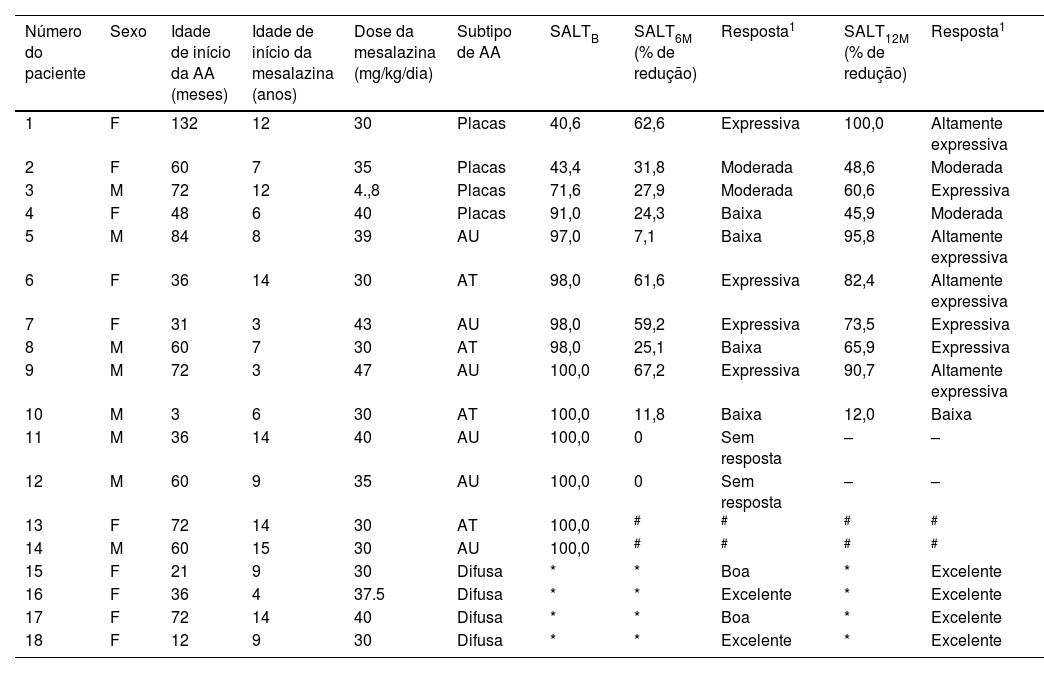
Pacientes com AA e sua resposta à terapia com mesalazina em seis e 12 meses
| Número do paciente | Sexo | Idade de início da AA (meses) | Idade de início da mesalazina (anos) | Dose da mesalazina (mg/kg/dia) | Subtipo de AA | SALTB | SALT6M (% de redução) | Resposta1 | SALT12M (% de redução) | Resposta1 |
|---|---|---|---|---|---|---|---|---|---|---|
| 1 | F | 132 | 12 | 30 | Placas | 40,6 | 62,6 | Expressiva | 100,0 | Altamente expressiva |
| 2 | F | 60 | 7 | 35 | Placas | 43,4 | 31,8 | Moderada | 48,6 | Moderada |
| 3 | M | 72 | 12 | 4.,8 | Placas | 71,6 | 27,9 | Moderada | 60,6 | Expressiva |
| 4 | F | 48 | 6 | 40 | Placas | 91,0 | 24,3 | Baixa | 45,9 | Moderada |
| 5 | M | 84 | 8 | 39 | AU | 97,0 | 7,1 | Baixa | 95,8 | Altamente expressiva |
| 6 | F | 36 | 14 | 30 | AT | 98,0 | 61,6 | Expressiva | 82,4 | Altamente expressiva |
| 7 | F | 31 | 3 | 43 | AU | 98,0 | 59,2 | Expressiva | 73,5 | Expressiva |
| 8 | M | 60 | 7 | 30 | AT | 98,0 | 25,1 | Baixa | 65,9 | Expressiva |
| 9 | M | 72 | 3 | 47 | AU | 100,0 | 67,2 | Expressiva | 90,7 | Altamente expressiva |
| 10 | M | 3 | 6 | 30 | AT | 100,0 | 11,8 | Baixa | 12,0 | Baixa |
| 11 | M | 36 | 14 | 40 | AU | 100,0 | 0 | Sem resposta | – | – |
| 12 | M | 60 | 9 | 35 | AU | 100,0 | 0 | Sem resposta | – | – |
| 13 | F | 72 | 14 | 30 | AT | 100,0 | # | # | # | # |
| 14 | M | 60 | 15 | 30 | AU | 100,0 | # | # | # | # |
| 15 | F | 21 | 9 | 30 | Difusa | * | * | Boa | * | Excelente |
| 16 | F | 36 | 4 | 37.5 | Difusa | * | * | Excelente | * | Excelente |
| 17 | F | 72 | 14 | 40 | Difusa | * | * | Boa | * | Excelente |
| 18 | F | 12 | 9 | 30 | Difusa | * | * | Excelente | * | Excelente |
Escala de resposta em paciente com AA em placas, AU ou AT: −5% a −25% (baixa); −26% a −50%: moderada; −51% a −75%: expressiva; −76% a −100%: altamente expressiva.
Escala de resposta em pacientes com AA difusa: repilação maior que 40% (excelente); 20%‐40% (boa); < 10% (baixa).
Em 2007, um estudo mostrou que um medicamento semelhante à mesalazina, chamado sulfassalazina, manteve a repilação induzida por corticosteroide, sugerindo potencial benefício dessa medicação.8 A sulfassalazina é um pró‐fármaco composto por ácido 5‐aminossalicílico ligado à sulfapiridina por um anel azol. Enquanto o 5‐ASA tem efeitos benéficos em doença inflamatória intestinal, a sulfapiridina é responsável pela maioria dos efeitos colaterais (cefaleia, anorexia, náuseas e vômitos). A mesalazina (liberação lenta de 5‐ASA) não contém sulfapiridina, e é mais bem tolerada. É usada em crianças para tratamento de doença inflamatória intestinal e tem efeito imunomodulador e de imunossupressão, incluindo inibição de interleucinas (IL)‐1 e IL‐2 e do fator de necrose tumoral alfa.2
Em 2018, nosso grupo publicou o primeiro estudo com mesalazina e demonstrou benefício em pacientes pediátricos com AA grave.2 Em 2021, Mahgoob et al. compararam mesalazina com azatioprina em 30 pacientes adultos e crianças com AA grave e mostraram que ambas são eficientes para AA, com a mesalazina apresentando menos efeitos colaterais.9 Nosso estudo observou redução média relativa de SALT de 66,8% após 12 meses de tratamento com mesalazina, resultado semelhante a um estudo que evidenciou redução de 67,7% em adolescentes com AA usando tofacitinibe,10 porém com custo de tratamento bem inferior no caso da mesalazina. O presente estudo destaca os potenciais benefícios da mesalazina para gerenciar pacientes com AA. Parece ser uma possibilidade segura, principalmente na população pediátrica, na qual é imperativo o uso de medicamentos com menor probabilidade de efeitos colaterais. A limitação é o pequeno tamanho da amostra e o uso concomitante de corticoterapia quando a doença estava ativa. Mais estudos, especialmente ensaios clínicos controlados, devem ser feitos.
Suporte financeiroNenhum.
Contribuição dos autoresAnalú Vivian: Elaboração e redação.
Vania Oliveira de Carvalho: Revisão da literatura e redação.
Ana Elisa Kiszewski: Concepção e planejamento do estudo; Revisão crítica do manuscrito e aprovação da versão final.
Conflito de interessesNenhum.
Como citar este artigo: Vivian A, Carvalho VO, Kiszewski AE. Efficacy of mesalazine in children with moderate to severe alopecia areata: case series of 18 patients. An Bras Dermatol. 2023;98:837–40.
Trabalho realizado na Unidade de Dermatologia Pediátrica, Serviço de Dermatologia, Irmandade Santa Casa de Misericórdia de Porto Alegre, Universidade Federal de Ciências da Saúde de Porto Alegre, Porto Alegre, RS, Brasil.