Os cosméticos são produtos utilizados de maneira ampla por todas as faixas etárias, fazendo com que as reações adversas sejam um problema de saúde pública. O evento adverso mais comum é a dermatite de contato irritativa; porém, frequentemente a dermatite de contato alérgica (DCA) recebe maior atenção por relacionar‐se a reações mais graves.1 Constituintes de cosméticos, como fragrâncias e preservativos, respondem por uma boa parte dos casos de DCA, e o diagnóstico é feito por meio da história clínica e de exame físico, corroborado pelo teste de contato (TC).2,3 No Brasil, a bateria padrão contém 30 substâncias, das quais pelo menos 18 elementos são encontrados em cosméticos, além da bateria de cosméticos com mais 10 alérgenos. O rendimento do TC pode ser ampliado com uso dos cosméticos in natura, especialmente quando há dificuldade de acesso a diferentes baterias e alérgenos individuais. Este trabalho avaliou a prevalência de alergia a cosméticos, os alérgenos implicados, características da população acometida, e o rendimento do teste com cosméticos in natura.
Conduziu‐se um estudo seccional a partir dos TC aplicados entre 2013‐2017 em um Serviço de Dermatologia Relacionada ao Trabalho e em um Ambulatório de Dermatoses Alérgicas, na cidade do Rio de Janeiro. Todos os pacientes foram submetidos ao TC com as baterias padrão e de cosméticos brasileiras (FDA Allergenic e Asac Pharma). Naqueles em que havia suspeita de DCA induzida por cosméticos de uso pessoal, caso o produto fosse não enxaguável, foi testado in natura. Destaca‐se que os esmaltes foram aplicados diretamente nos contensores, e as fitas foram coladas no dorso dos pacientes apenas após secarem. As leituras foram realizadas com 48 e 96 horas.
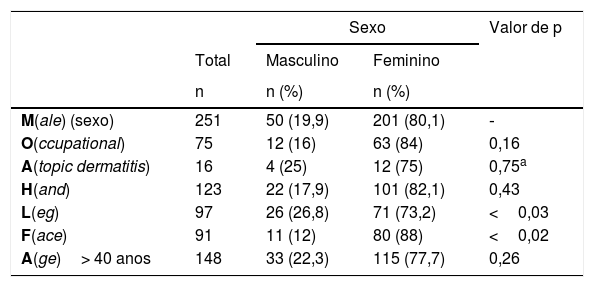
Dentre os 768 testes realizados, 251 (32,7%) tiveram o diagnóstico de DCA a cosméticos, predominando mulheres (201/80,1%) com idade média de 43,7 anos (SD=14,7). No geral, as mãos foram o local mais acometido pela DCA a cosméticos (123/49%); observou‐se eczema nas palmas em 31,5% (79) dos casos, e no dorso das mãos em 29,5% (74). Comparando com o sexo masculino, pacientes do sexo feminino apresentaram maior prevalência de lesões na face (p<0,02) e nos membros inferiores (p <0,03) – tabela 1.
Características demográficas e clínicas dos pacientes com dermatite de contato alérgica a cosméticos, segundo o índice MOAHLFA
| Sexo | Valor de p | |||
|---|---|---|---|---|
| Total | Masculino | Feminino | ||
| n | n (%) | n (%) | ||
| M(ale) (sexo) | 251 | 50 (19,9) | 201 (80,1) | ‐ |
| O(ccupational) | 75 | 12 (16) | 63 (84) | 0,16 |
| A(topic dermatitis) | 16 | 4 (25) | 12 (75) | 0,75a |
| H(and) | 123 | 22 (17,9) | 101 (82,1) | 0,43 |
| L(eg) | 97 | 26 (26,8) | 71 (73,2) | <0,03 |
| F(ace) | 91 | 11 (12) | 80 (88) | <0,02 |
| A(ge)> 40 anos | 148 | 33 (22,3) | 115 (77,7) | 0,26 |
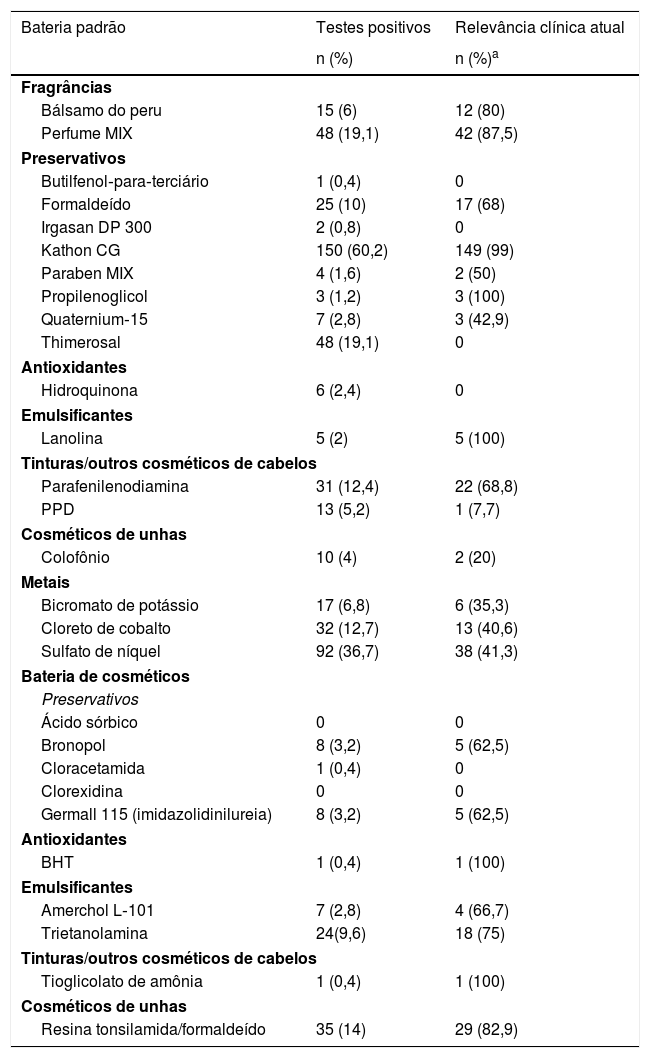
A análise dos resultados positivos dos TC mostrou que o preservativo Kathon CG (150/60,2%) foi o alérgeno mais prevalente da bateria padrão entre os pacientes com DCA por cosméticos, seguido de sulfato de níquel (91/36,5%), perfume MIX (47/18,9%), thimerosal (47/18,9%), parafenilenodiamina (31/12,4%), cloreto de cobalto (31/12,4%) e formaldeído (25/10%). Já na bateria de cosméticos, as substâncias com maior prevalência de resultado positivo foram resina tonsilamida/formaldeído (35/14,1%), trietanolamina (24/9,6%), bronopol (8/3,2%), Germall 115 (8/3,2%) e Amerchol L‐101 (7/2,8%). Ressalta‐se, no entanto, que entre os alérgenos mais prevalentes da bateria padrão, os únicos que mostraram relevância clínica atual> 50% foram o Kathon CG (99%), perfume MIX (87,5%), parafenilenodiamina (68,8%) e formaldeído (68%), enquanto todas as substâncias mais prevalentes da bateria de cosméticos evidenciaram relevância significativa (tabela 2).
Prevalência de testes de contato positivos e relevância clínica atual de alérgenos de cosméticos presentes na bateria padrão e dos elementos constituintes da bateria de cosméticos
| Bateria padrão | Testes positivos | Relevância clínica atual |
|---|---|---|
| n (%) | n (%)a | |
| Fragrâncias | ||
| Bálsamo do peru | 15 (6) | 12 (80) |
| Perfume MIX | 48 (19,1) | 42 (87,5) |
| Preservativos | ||
| Butilfenol‐para‐terciário | 1 (0,4) | 0 |
| Formaldeído | 25 (10) | 17 (68) |
| Irgasan DP 300 | 2 (0,8) | 0 |
| Kathon CG | 150 (60,2) | 149 (99) |
| Paraben MIX | 4 (1,6) | 2 (50) |
| Propilenoglicol | 3 (1,2) | 3 (100) |
| Quaternium‐15 | 7 (2,8) | 3 (42,9) |
| Thimerosal | 48 (19,1) | 0 |
| Antioxidantes | ||
| Hidroquinona | 6 (2,4) | 0 |
| Emulsificantes | ||
| Lanolina | 5 (2) | 5 (100) |
| Tinturas/outros cosméticos de cabelos | ||
| Parafenilenodiamina | 31 (12,4) | 22 (68,8) |
| PPD | 13 (5,2) | 1 (7,7) |
| Cosméticos de unhas | ||
| Colofônio | 10 (4) | 2 (20) |
| Metais | ||
| Bicromato de potássio | 17 (6,8) | 6 (35,3) |
| Cloreto de cobalto | 32 (12,7) | 13 (40,6) |
| Sulfato de níquel | 92 (36,7) | 38 (41,3) |
| Bateria de cosméticos | ||
| Preservativos | ||
| Ácido sórbico | 0 | 0 |
| Bronopol | 8 (3,2) | 5 (62,5) |
| Cloracetamida | 1 (0,4) | 0 |
| Clorexidina | 0 | 0 |
| Germall 115 (imidazolidinilureia) | 8 (3,2) | 5 (62,5) |
| Antioxidantes | ||
| BHT | 1 (0,4) | 1 (100) |
| Emulsificantes | ||
| Amerchol L‐101 | 7 (2,8) | 4 (66,7) |
| Trietanolamina | 24(9,6) | 18 (75) |
| Tinturas/outros cosméticos de cabelos | ||
| Tioglicolato de amônia | 1 (0,4) | 1 (100) |
| Cosméticos de unhas | ||
| Resina tonsilamida/formaldeído | 35 (14) | 29 (82,9) |
Em 93 casos (37,1%) realizou‐se o teste com o cosmético in natura. Os maiores rendimentos (testes positivos/n° total de testes) foram obtidos com esmaltes (61,8%), hidratante facial/corporal (53,8%), filtro solar (41,7%) e perfumes/colônia (36%) – tabela 3. Destaca‐se que entre os pacientes que testaram esmaltes in natura e tiveram resultado positivo (21), oito foram negativos para a resina tonsilamida/formaldeído e não apresentaram testes positivos relevantes para outros alérgenos da bateria padrão. Nesses casos, se o esmalte não tivesse sido testado, não teria sido possível definir o agente da DCA.
Rendimento dos testes de contato realizados com cosméticos in natura
| Tipo de cosmético | Total de testes | Resultados positivos | Rendimento |
|---|---|---|---|
| n | n | % | |
| Hidratante facial/corporal | 39 | 21 | 53,8 |
| Esmalte | 34 | 21 | 61,8 |
| Perfumes/colônia | 25 | 9 | 36 |
| Creme para pentear os cabelos | 20 | 2 | 10 |
| Desodorante | 17 | 2 | 11,8 |
| Filtro solar | 12 | 5 | 41,7 |
| Batom/hidratante labial | 8 | 2 | 25 |
| Blush | 4 | 1 | 25 |
| Base facial | 7 | 2 | 28,6 |
| Lápis/delineador de olhos | 4 | 1 | 25 |
Fonte: Elaborada com base nas informações do banco de dados dos pacientes submetidas ao teste de contato entre 2013‐2017.
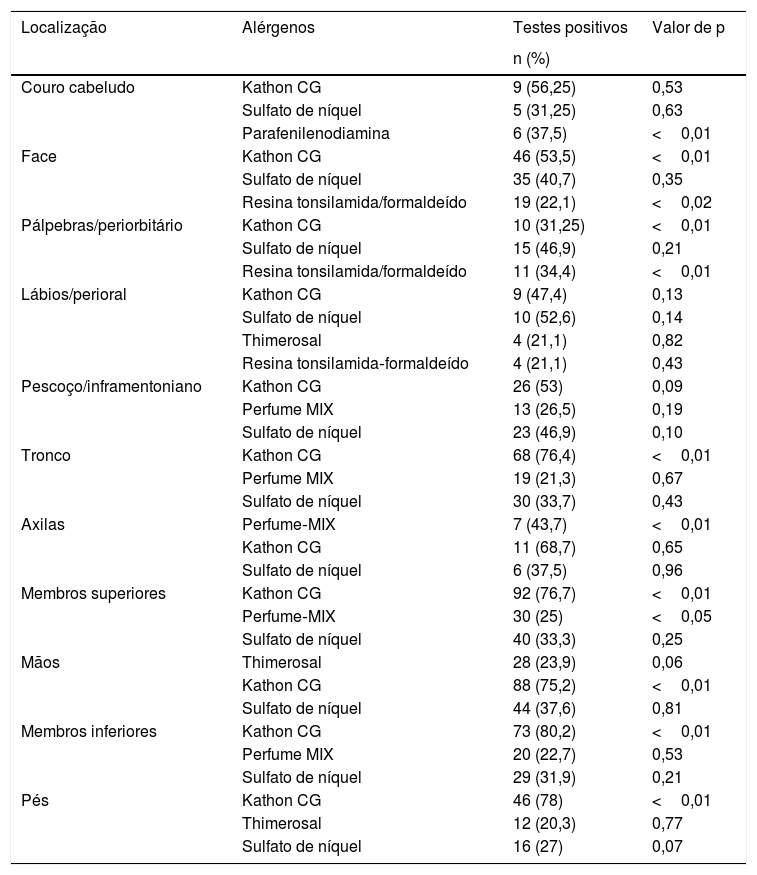
Novamente, Kathon CG foi o alérgeno que mais apresentou associação significativa com o acometimento de segmentos corporais específicos (tabela 4). O conhecimento da relação dos alérgenos com os sítios mais acometidos orienta a busca dos possíveis cosméticos implicados no quadro e auxilia na restrição de produtos antes da aplicação do TC.
Associação entre localização das lesões e os alérgenos mais prevalentes por segmento corporal das baterias padrão e de cosméticos brasileiras, que apresentaram relevância clínica atual
| Localização | Alérgenos | Testes positivos | Valor de p |
|---|---|---|---|
| n (%) | |||
| Couro cabeludo | Kathon CG | 9 (56,25) | 0,53 |
| Sulfato de níquel | 5 (31,25) | 0,63 | |
| Parafenilenodiamina | 6 (37,5) | <0,01 | |
| Face | Kathon CG | 46 (53,5) | <0,01 |
| Sulfato de níquel | 35 (40,7) | 0,35 | |
| Resina tonsilamida/formaldeído | 19 (22,1) | <0,02 | |
| Pálpebras/periorbitário | Kathon CG | 10 (31,25) | <0,01 |
| Sulfato de níquel | 15 (46,9) | 0,21 | |
| Resina tonsilamida/formaldeído | 11 (34,4) | <0,01 | |
| Lábios/perioral | Kathon CG | 9 (47,4) | 0,13 |
| Sulfato de níquel | 10 (52,6) | 0,14 | |
| Thimerosal | 4 (21,1) | 0,82 | |
| Resina tonsilamida‐formaldeído | 4 (21,1) | 0,43 | |
| Pescoço/inframentoniano | Kathon CG | 26 (53) | 0,09 |
| Perfume MIX | 13 (26,5) | 0,19 | |
| Sulfato de níquel | 23 (46,9) | 0,10 | |
| Tronco | Kathon CG | 68 (76,4) | <0,01 |
| Perfume MIX | 19 (21,3) | 0,67 | |
| Sulfato de níquel | 30 (33,7) | 0,43 | |
| Axilas | Perfume‐MIX | 7 (43,7) | <0,01 |
| Kathon CG | 11 (68,7) | 0,65 | |
| Sulfato de níquel | 6 (37,5) | 0,96 | |
| Membros superiores | Kathon CG | 92 (76,7) | <0,01 |
| Perfume‐MIX | 30 (25) | <0,05 | |
| Sulfato de níquel | 40 (33,3) | 0,25 | |
| Mãos | Thimerosal | 28 (23,9) | 0,06 |
| Kathon CG | 88 (75,2) | <0,01 | |
| Sulfato de níquel | 44 (37,6) | 0,81 | |
| Membros inferiores | Kathon CG | 73 (80,2) | <0,01 |
| Perfume MIX | 20 (22,7) | 0,53 | |
| Sulfato de níquel | 29 (31,9) | 0,21 | |
| Pés | Kathon CG | 46 (78) | <0,01 |
| Thimerosal | 12 (20,3) | 0,77 | |
| Sulfato de níquel | 16 (27) | 0,07 |
Fonte: Elaborada com base nas informações do banco de dados dos pacientes submetidas ao teste de contato entre 2013‐2017.
O Kathon CG é um preservativo que consiste na mistura de metilcloroisotiazolinona e metilisotiazolinona (MI), na proporção 3:1, respectivamente; é encontrado em cosméticos, produtos de uso industrial, de limpeza e tintas. A alta prevalência de testes positivos para essa mistura, chegando a 60% dos casos de DCA a cosméticos, possivelmente reflete a ocorrência no país da epidemia de sensibilização à porção MI, relatada em todo o mundo desde 2010.4 Apesar disso, a MI isolada ainda não foi adicionada à bateria padrão nacional.5 Os metais podem ser encontrados em sombra para os olhos (cromo e níquel), rímel (cromo), tintura de cabelo (cobalto e níquel), esmalte (cobalto), entre outros. Apesar de o teste de contato positivo com o sulfato de níquel ser prevalente, frequentemente sua relevância clínica para DCA a cosmético é difícil de ser estabelecida.6 A triagem de DCA a fragrâncias na bateria padrão é feita por meio do perfume MIX e do bálsamo do Peru. Essas substâncias estão presentes também em produtos de limpeza, tecidos, condimentos, entre outros, ampliando possíveis fontes de exposição.
Neste trabalho, a prevalência de testes positivos para o perfume MIX foi de 19,1%, enquanto a média mundial de testes positivos para essa mistura varia entre 4 a 11%.7 A maior prevalência observada pode ser justificada pela amostra analisada ser constituída apenas por pacientes sabidamente com DCA a cosméticos. Em relação ao thimerosal, apesar da alta prevalência de testes positivos, nenhum deles apresentou relevância clínica. Por isso, esse alérgeno já foi excluído das baterias padrão norte‐americana e europeia. A parafenilenodiamina é adicionada a tinturas de cabelo para intensificar a coloração e aumentar a durabilidade do tingimento, o que acaba justificando sua associação com lesões no couro cabeludo.8 A sensibilização ao formaldeído e seus liberadores, como quaternium 15, bronopol e Germall‐115, ocorre de maneira isolada ou combinada. Neste trabalho, quatro alérgicos ao formaldeído apresentavam também sensibilização a pelo menos um de seus liberadores. No Brasil, o formaldeído é tolerado como conservante de cosméticos e endurecedor de unhas, nas concentrações máximas de 0,2% e 5% respectivamente.9
A realização rotineira da série de cosméticos é preconizada apenas quando há a suspeita de DCA a esse tipo de produto, visando aumentar a acurácia do teste epicutâneo. No entanto, neste estudo, ambas as baterias foram testadas consecutivamente porque a série nacional não sofre atualização há alguns anos e objetivou‐se aumentar o rendimento do teste. A European Society of Contact Dermatitis preconiza que um alérgeno deva ser incluído na bateria padrão de um país quando a sensibilização a este exceder 0,5‐1% dos testes realizados e for clinicamente relevante.10 Assim, poderia ser considerada a adição à bateria padrão brasileira de alguns elementos da série de cosméticos para testagem regular. Ressalta‐se, no entanto, que seria necessário avaliar se a amostra escolhida neste estudo é representativa da população brasileira. Além disso, outros preservativos empregados em cosméticos e de alta prevalência de sensibilização em outros países, como MI, metildibromo glutaronitrila e cocamidopropil betaina poderiam ser considerados.
Suporte financeiroNenhum.
Contribuição dos autoresAna Luiza Castro Fernandes Villarinho: Análise estatística; concepção e planejamento do estudo; elaboração e redação do manuscrito; obtenção, análise e interpretação dos dados; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura.
Maria das Graças Mota Melo: Elaboração e redação do manuscrito; participação efetiva na orientação da pesquisa; participação intelectual em conduta propedêutica e/ou terapêutica de casos estudados; revisão crítica da literatura; revisão crítica do manuscrito.
Liliane Reis Teixeira: Análise estatística; aprovação da versão final do manuscrito; participação efetiva na orientação da pesquisa; revisão crítica do manuscrito.
Conflito de interesseNenhum
Como citar este artigo: Villarinho ALCF, Melo MGM, Teixeira LR. Application of the Brazilian patch test panel in the diagnosis of allergic contact dermatitis to cosmetics. An Bras Dermatol. 2022;97:656–60.
Trabalho realizado na Escola Nacional de Saúde Pública Sergio Arouca, Fundação Oswaldo Cruz, Rio de Janeiro, RJ, Brasil.