Revisões sistemáticas de ensaios clínicos randomizados (ECRs) são consideradas evidências de alto nível para apoiar uma decisão sobre intervenções terapêuticas, e sua qualidade metodológica é essencial para fornecer resultados confiáveis e aplicáveis.
ObjetivoEste estudo metaepidemiológico teve como objetivo mapear e avaliar criticamente revisões sistemáticas que avaliam tratamentos para doenças de pele vesicobolhosas.
MétodosFoi conduzida estratégia de busca abrangente no banco de dados MEDLINE (via Pubmed) em dezembro de 2022, sem restrições, para encontrar revisões sistemáticas avaliando intervenções farmacológicas para doenças vesicobolhosas. A qualidade metodológica foi avaliada por meio da ferramenta AMSTAR‐2 e informações adicionais foram extraídas. Foram identificadas nove revisões sistemáticas publicadas entre 2002 e 2021, sete delas avaliando pênfigo.
ResultadosDe acordo com a ferramenta AMSTAR‐2, 55,6% foram classificadas como tendo qualidade criticamente baixa, 22,2% como qualidade moderada, 11,1% como baixa e 11,1% como alta qualidade. Nenhuma revisão avaliou a certeza das evidências (GRADE); 86% das revisões de pênfigo tiveram pelo menos dois ECRs sobrepostos. Houve algumas limitações em relação às falhas metodológicas e ao uso da ferramenta AMSTAR‐2.
ConclusõesEsses achados revelam qualidade metodológica frágil das revisões sistemáticas sobre o tratamento das doenças vesicobolhosas, que pode impactar os resultados. Portanto, o rigor metodológico é obrigatório para futuras revisões sistemáticas, a fim de evitar duplicação de esforços e aumentar a certeza das evidências que apoiam a tomada de decisão.
Revisões sistemáticas de ensaios clínicos randomizados (ECRs) são estudos elaborados para identificar, resumir e avaliar criticamente as melhores evidências disponíveis sobre intervenções terapêuticas e fornecer subsídios para a decisão sobre o cuidado do paciente e a política de saúde.1,2 Esse desenho de estudo visa evitar a produção desnecessária e redundante de estudos primários, fornecer respostas rápidas a questões de saúde e pode combinar resultados de estudos semelhantes em metanálises, aumentando o poder estatístico e a confiança nos efeitos estimados.1 Ao aplicar recomendações metodológicas adequadas para o desenvolvimento de uma revisão sistemática de intervenção, é realizada cuidadosa avaliação dos ECRs incluídos, implicando diretamente na confiabilidade da evidência por meio dos resultados obtidos, já que o ECR é o desenho de estudo primário mais adequado para responder a uma questão de tratamento clínico. Assim, a aplicabilidade dos resultados sobre a eficácia e segurança dos tratamentos na prática clínica pode ajudar os profissionais de saúde, legisladores, pacientes e criadores de diretrizes.1
Evidências rigorosamente desenvolvidas em dermatologia aumentaram ao longo do tempo, principalmente em virtude de preocupações sobre o impacto das falhas metodológicas nos efeitos estimados das intervenções avaliadas em ensaios clínicos. Como resultado das inúmeras publicações de ECRs sobre tratamentos dermatológicos, um número crescente de revisões sistemáticas tem sido publicado nessa área, e as recomendações metodológicas adequadas para preparar e conduzir uma revisão sistemática, como recomendado pela Cochrane, nem sempre são seguidas pelos autores, levando a erros sistemáticos e resultados com viés, na maioria das vezes superestimando o tratamento avaliado.1,3,4
Nesse sentido, nos últimos anos, estudos metaepidemiológicos têm sido realizados para avaliar o impacto de algumas limitações metodológicas dos estudos clínicos nos resultados observados. Além disso, esses estudos de metapesquisa verificam a qualidade metodológica para apoiar pesquisas futuras, evitando a ocorrência dos mesmos vieses e extraindo evidências confiáveis a fim de estabelecer processos de tomada de decisão em saúde. A unidade de análise em um estudo metaepidemiológico são os estudos individuais e não os pacientes, como na pesquisa clínica tradicional.5,6
O tratamento de dermatoses, como as doenças vesicobolhosas, tem sido investigado por diversos estudos. Essas condições clínicas cutâneas têm o aparecimento de vesículas ou bolhas como manifestações clínicas primárias, afetando diretamente a qualidade de vida do paciente. São afecções de etiologia variável e podem resultar de infecção, alterações genéticas ou metabólicas, hipersensibilidade a medicamentos e condições autoimunes.7–9 Desde o surgimento da corticoterapia, esses pacientes têm tido acesso a recursos de tratamento, que podem associar outras classes de medicamentos, como imunossupressores.10 A gravidade das doenças e a necessidade de tratamentos eficazes e seguros reforçam a exigência de estudos clínicos com alta qualidade metodológica. Assim, o objetivo deste estudo metaepidemiológico é mapear e avaliar criticamente revisões sistemáticas que avaliaram tratamentos farmacológicos para doenças vesicobolhosas.
MétodosEste estudo metaepidemiológico segue as recomendações propostas por Murad et al., em 2017, para relatar estudos metaepidemiológicos,4 além dos itens pertinentes do método Preferred Reporting Items for Systematic Reviews and Meta‐Analyses (PRISMA 2020).11
Critérios para inclusão de estudosTipos de estudosForam consideradas revisões sistemáticas que incluem apenas ensaios clínicos randomizados (ECRs) sobre intervenções para o tratamento de doenças de pele vesicobolhosas, isto é com acantólise e/ou bolhas, tais como dermatite herpetiforme, epidermólise bolhosa, eritema multiforme, síndrome de Stevens‐Johnson, impetigo bolhoso, hidroa vaciniforme, dermatose bolhosa por IgA linear, penfigoide e pênfigo. Não foram incluídos protocolos ou versões anteriores da mesma revisão sistemática. Não foram considerados artigos que não tivessem o termo revisão sistemática no título ou no corpo do texto. Não foram consideradas revisões sistemáticas disponíveis apenas como resumos, formatos incompletos ou em andamento.
Análise de dados- 1.
Características das revisões sistemáticas incluídas: ano de publicação, número de ECRs primários incluídos, tipo de doença vesicobolhosa, tipos de intervenções farmacológicas.
- 2.
Qualidade metodológica das revisões sistemáticas incluídas de acordo com os itens da ferramenta AMSTAR‐2.12
- 3.
Relatório de adequação das estratégias de busca aplicando os seguintes aspectos: data completa da busca apresentada (dia/mês/ano), estratégia de busca apresentada (termos MeSH utilizados), buscas manuais adicionais realizadas, restrições aplicadas (idioma e data) e bases de dados pesquisadas.13
- 4.
Número de revisões sistemáticas que avaliaram a certeza das evidências usando a abordagem Grading of Recommendations Assessment, Development and Evaluation (GRADE).14 Vale ressaltar que a abordagem GRADE foi implementada em 2013, e as revisões sistemáticas publicadas antes disso certamente não utilizaram essa ferramenta.
- 5.
Número de revisões sistemáticas que identificam e relatam “estudos aguardando classificação” (um estudo encontrado na busca não fornece informações suficientes para analisar o cumprimento dos critérios de elegibilidade – p. ex., texto completo indisponível). Esse estudo permanece aguardando avaliação até que informações adicionais sejam obtidas e estudos em andamento (ensaios clínicos randomizados ainda em andamento, registrados em bases de dados como Clinical Trials.gov, que poderão contribuir com os resultados quando finalizados).13
- 6.
Verificar quantos ECRs foram incluídos em mais de uma revisão sistemática para identificar a sobreposição de estudos.
As revisões sistemáticas foram identificadas na base de dados Medical Literature Analysis and Retrieval System Online (MEDLINE, via PubMed; 1° de dezembro de 2022), com limites de filtragem para desenho do estudo (revisão sistemática). Nenhuma restrição foi aplicada quanto à data de publicação ou idioma. Por se tratar de estudo metaepidemiológico e que busca amostra de revisões sistemáticas sobre o tratamento de dermatoses vesicobolhosas, foi considerada suficiente a busca no banco de dados MEDLINE (via Pubmed). A estratégia de busca está detalhada na tabela 1.
Estratégias de busca na base de dados MEDLINE (via PubMed)
| Estratégia de busca |
|---|
| (“Skin Diseases, Vesiculobullous”[Mesh] OR (Skin Disease, Vesiculobullous) AND (Vesiculobullous Skin Disease) OR (Vesiculobullous Skin Diseases) OR (Vesiculobullous Dermatoses) OR (Dermatoses, Vesiculobullous) OR (Skin Diseases, Bullous) OR (Bullous Skin Disease) OR (Skin Disease, Bullous) OR (Bullous Skin Diseases) OR (Bullous Dermatoses) OR (Dermatoses, Bullous) OR (Vesicular Skin Diseases) OR (Skin Disease, Vesicular) OR (Vesicular Skin Disease) OR (Skin Diseases, Vesicular) OR (Pustular Dermatosis, Subcorneal) OR (Dermatoses, Subcorneal Pustular) OR (Dermatosis, Subcorneal Pustular) OR (Pustular Dermatoses, Subcorneal) OR (Subcorneal Pustular Dermatoses) OR (Sneddon‐Wilkinson Disease) OR (Sneddon Wilkinson Disease) OR (Subcorneal Pustular Dermatosis)) AND (systematic [sb]) |
O processo de seleção dos estudos foi realizado na plataforma Rayyan.15 Dois revisores avaliam de modo independente todos os títulos e resumos recuperados pelas estratégias de busca. Primeiramente, os estudos potencialmente elegíveis foram analisados em texto completo para confirmar a elegibilidade. As inconsistências entre revisores foram resolvidas consultando um terceiro revisor. Os estudos excluídos após a segunda etapa foram apresentados na “tabela de estudos excluídos”, assim como os motivos de cada exclusão.
Extração de dadosOs procedimentos de extração de dados foram realizados por uma dupla independente de revisores, utilizando ficha de dados preestabelecida. As inconsistências durante esse processo foram resolvidas por meio de consulta com um terceiro revisor.
Avaliação da qualidade metodológica das revisões sistemáticas incluídasA qualidade metodológica das revisões foi avaliada por um escore baseado na ferramenta AMSTAR‐2,12 que inclui 16 itens que abordam (1) se as questões de pesquisa e os critérios de inclusão da revisão incluem os componentes PICO; (2) se existe um protocolo a priori; (3) se há justificativas para a seleção do desenho do estudo; (4) quais foram as estratégias de busca; (5) se foram selecionados estudos duplicados; (6) se foram extraídos dados duplicados; (7) se foram apresentados os estudos excluídos e os motivos da exclusão; (8) quais foram as características dos estudos incluídos; (9) quais foram os métodos de avaliação do risco de viés (RoB, do inglês risk of bias) dos estudos incluídos; (10) se foi informada a fonte de financiamento dos estudos incluídos; (11) se os métodos de combinação dos resultados foram adequados; (12) se houve avaliação do impacto do RoB nos resultados da metanálise; (13) se o RoB foi considerado na interpretação e discussão dos resultados; (14) se há discussão e explicação da heterogeneidade; (15) se houve investigação de viés de publicação; e (16) se houve declaração de conflito de interesses dos autores da revisão. Sete desses itens são considerados críticos (itens 1, 4, 7, 9, 11, 13 e 15) e, ao final, a revisão é classificada como tendo um dos seguintes graus de confiança: criticamente baixo (mais de uma falha crítica), baixa (uma falha crítica), moderada (mais de uma falha não crítica) e alta (nenhuma falha crítica ou uma falha não crítica). A confiança geral será gerada utilizando a ferramenta de lista de verificação disponível no site AMSTAR‐2 (http://amstar.ca/Amstar_Checklist.ph). O julgamento dos itens AMSTAR‐2 das revisões incluídas foi aplicado em cada revisão sistemática incluída por dois autores de maneira independente, e um terceiro autor resolveu as divergências.
Análise e apresentação de dadosAs estatísticas descritivas foram apresentadas com frequências absolutas e relativas (em porcentagens) e resumidas em gráficos e tabelas. As análises foram realizadas utilizando o Microsoft Excel®.
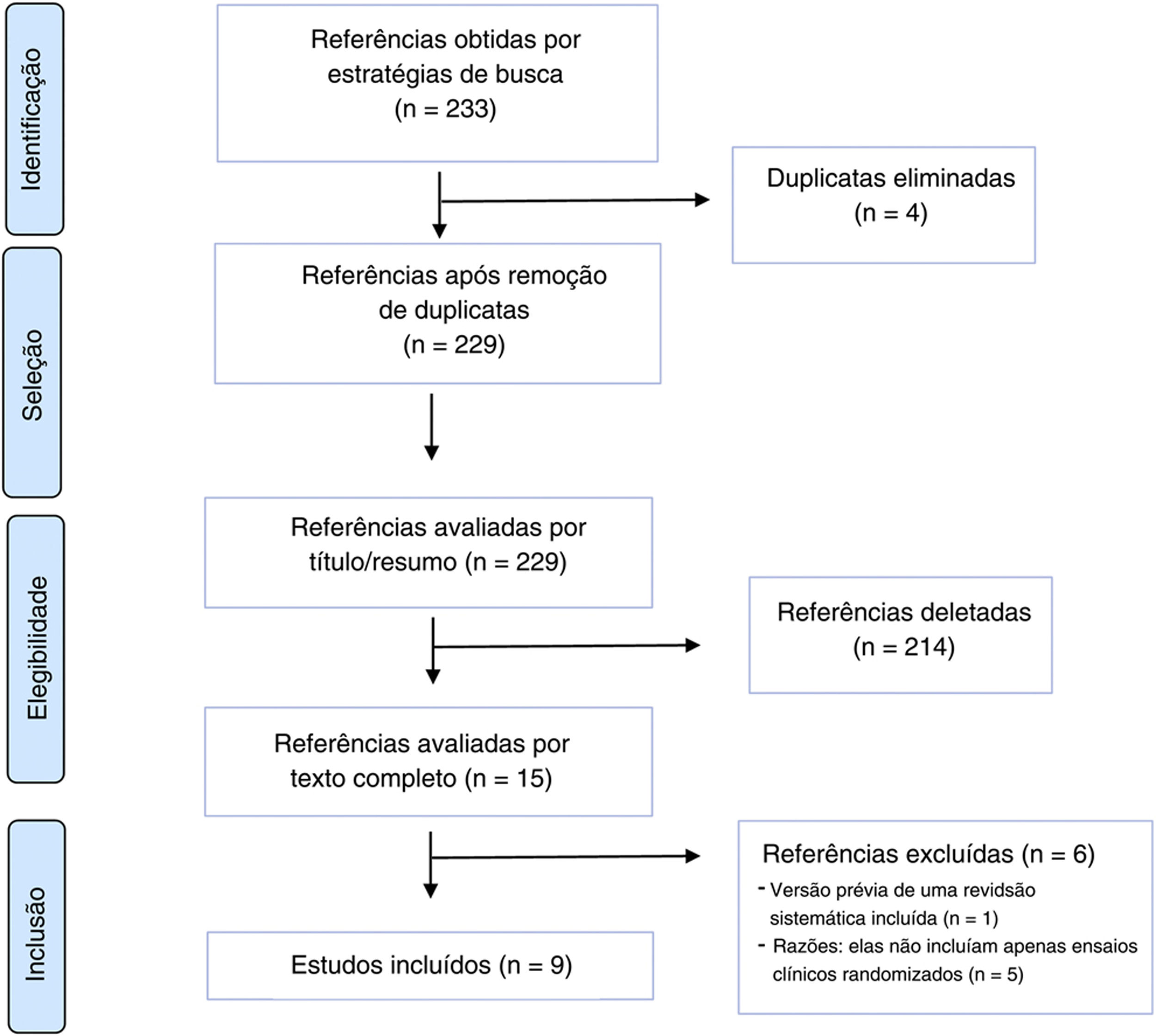
ResultadosResultados da buscaA busca eletrônica recuperou 233 referências. Após a remoção de quatro duplicatas, foram triados 229 títulos e resumos, dos quais 214 não contemplavam os critérios de elegibilidade. Assim, 15 estudos foram analisados em texto completo e seis foram excluídos: um era a versão mais antiga de uma revisão sistemática incluída16 e cinco porque não incluíam apenas ECRs.17–21 Portanto, nove revisões sistemáticas22–30 foram incluídas (fig. 1).
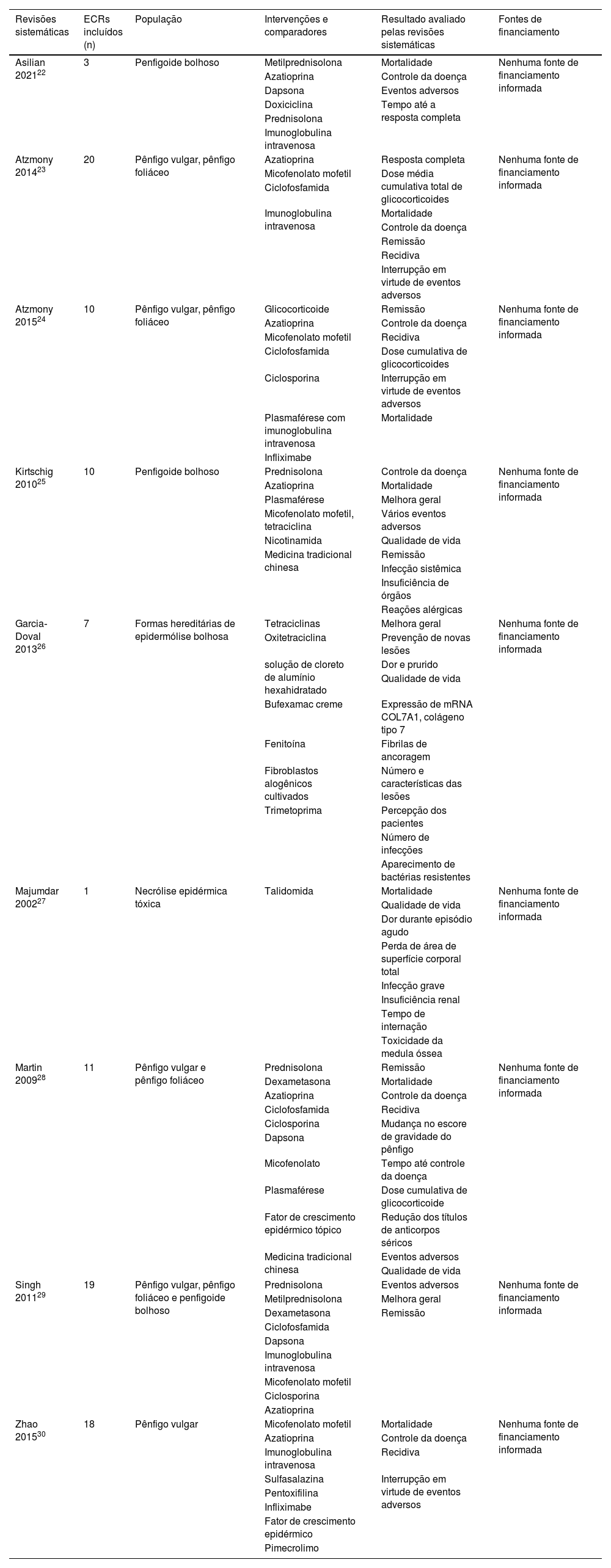
Características das revisões sistemáticas incluídasAs nove revisões sistemáticas foram publicadas entre 2002 e 2021 e avaliaram apenas ECRs como estudo primário, incluindo entre um e 20 ECRs. Além disso, três revisões (33,3%)25,27,28 são revisões Cochrane. A tabela 2 apresenta as principais características das revisões sistemáticas incluídas.
Características das revisões sistemáticas incluídas
| Revisões sistemáticas | ECRs incluídos (n) | População | Intervenções e comparadores | Resultado avaliado pelas revisões sistemáticas | Fontes de financiamento |
|---|---|---|---|---|---|
| Asilian 202122 | 3 | Penfigoide bolhoso | Metilprednisolona | Mortalidade | Nenhuma fonte de financiamento informada |
| Azatioprina | Controle da doença | ||||
| Dapsona | Eventos adversos | ||||
| Doxiciclina | Tempo até a resposta completa | ||||
| Prednisolona | |||||
| Imunoglobulina intravenosa | |||||
| Atzmony 201423 | 20 | Pênfigo vulgar, pênfigo foliáceo | Azatioprina | Resposta completa | Nenhuma fonte de financiamento informada |
| Micofenolato mofetil | Dose média cumulativa total de glicocorticoides | ||||
| Ciclofosfamida | |||||
| Imunoglobulina intravenosa | Mortalidade | ||||
| Controle da doença | |||||
| Remissão | |||||
| Recidiva | |||||
| Interrupção em virtude de eventos adversos | |||||
| Atzmony 201524 | 10 | Pênfigo vulgar, pênfigo foliáceo | Glicocorticoide | Remissão | Nenhuma fonte de financiamento informada |
| Azatioprina | Controle da doença | ||||
| Micofenolato mofetil | Recidiva | ||||
| Ciclofosfamida | Dose cumulativa de glicocorticoides | ||||
| Ciclosporina | Interrupção em virtude de eventos adversos | ||||
| Plasmaférese com imunoglobulina intravenosa | Mortalidade | ||||
| Infliximabe | |||||
| Kirtschig 201025 | 10 | Penfigoide bolhoso | Prednisolona | Controle da doença | Nenhuma fonte de financiamento informada |
| Azatioprina | Mortalidade | ||||
| Plasmaférese | Melhora geral | ||||
| Micofenolato mofetil, tetraciclina | Vários eventos adversos | ||||
| Nicotinamida | Qualidade de vida | ||||
| Medicina tradicional chinesa | Remissão | ||||
| Infecção sistêmica | |||||
| Insuficiência de órgãos | |||||
| Reações alérgicas | |||||
| Garcia‐Doval 201326 | 7 | Formas hereditárias de epidermólise bolhosa | Tetraciclinas | Melhora geral | Nenhuma fonte de financiamento informada |
| Oxitetraciclina | Prevenção de novas lesões | ||||
| solução de cloreto de alumínio hexahidratado | Dor e prurido | ||||
| Qualidade de vida | |||||
| Bufexamac creme | Expressão de mRNA COL7A1, colágeno tipo 7 | ||||
| Fenitoína | Fibrilas de ancoragem | ||||
| Fibroblastos alogênicos cultivados | Número e características das lesões | ||||
| Trimetoprima | |||||
| Percepção dos pacientes | |||||
| Número de infecções | |||||
| Aparecimento de bactérias resistentes | |||||
| Majumdar 200227 | 1 | Necrólise epidérmica tóxica | Talidomida | Mortalidade | Nenhuma fonte de financiamento informada |
| Qualidade de vida | |||||
| Dor durante episódio agudo | |||||
| Perda de área de superfície corporal total | |||||
| Infecção grave | |||||
| Insuficiência renal | |||||
| Tempo de internação | |||||
| Toxicidade da medula óssea | |||||
| Martin 200928 | 11 | Pênfigo vulgar e pênfigo foliáceo | Prednisolona | Remissão | Nenhuma fonte de financiamento informada |
| Dexametasona | Mortalidade | ||||
| Azatioprina | Controle da doença | ||||
| Ciclofosfamida | Recidiva | ||||
| Ciclosporina | Mudança no escore de gravidade do pênfigo | ||||
| Dapsona | |||||
| Micofenolato | Tempo até controle da doença | ||||
| Plasmaférese | Dose cumulativa de glicocorticoide | ||||
| Fator de crescimento epidérmico tópico | Redução dos títulos de anticorpos séricos | ||||
| Medicina tradicional chinesa | Eventos adversos | ||||
| Qualidade de vida | |||||
| Singh 201129 | 19 | Pênfigo vulgar, pênfigo foliáceo e penfigoide bolhoso | Prednisolona | Eventos adversos | Nenhuma fonte de financiamento informada |
| Metilprednisolona | Melhora geral | ||||
| Dexametasona | Remissão | ||||
| Ciclofosfamida | |||||
| Dapsona | |||||
| Imunoglobulina intravenosa | |||||
| Micofenolato mofetil | |||||
| Ciclosporina | |||||
| Azatioprina | |||||
| Zhao 201530 | 18 | Pênfigo vulgar | Micofenolato mofetil | Mortalidade | Nenhuma fonte de financiamento informada |
| Azatioprina | Controle da doença | ||||
| Imunoglobulina intravenosa | Recidiva | ||||
| Sulfasalazina | Interrupção em virtude de eventos adversos | ||||
| Pentoxifilina | |||||
| Infliximabe | |||||
| Fator de crescimento epidérmico | |||||
| Pimecrolimo |
n, número de ensaios clínicos randomizados (ECRs) incluídos.
Foram analisadas as seguintes intervenções para o tratamento de dermatose vesicobolhosa: corticosteroides, ciclosporina, imunoglobulina intravenosa, plasmaférese, dapsona, doxiciclina, tetraciclina, micofenolato mofetil, ciclofosfamida, tetraciclinas, oxitetraciclina, solução de cloreto de alumínio hexahidratado, bufexamac creme, fenitoína, fator de crescimento epidérmico, pimecrolimo, cultura de fibroblastos alogênicos, trimetoprima e talidomida.
Das nove revisões sistemáticas analisadas, 55,6% (5/7)23,24,28–30 estudaram pacientes com pênfigo bolhoso (pênfigo foliáceo e/ou vulgar), 22,2% (2/9)22,25 com penfigoide bolhoso; 11,1% (1/9)26 com epidermólise e 11,1% (1/9)27 com necrólise epidérmica tóxica.
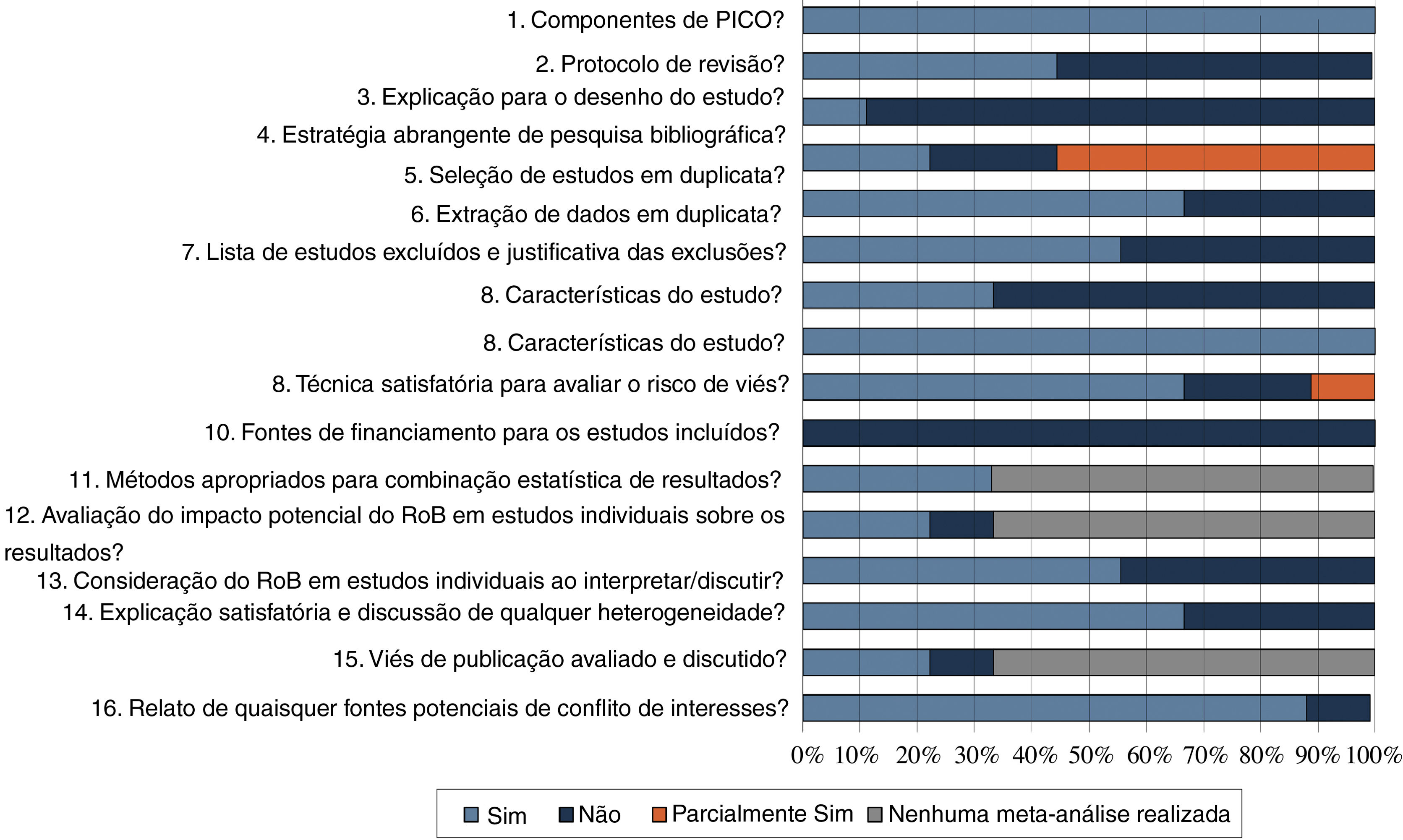
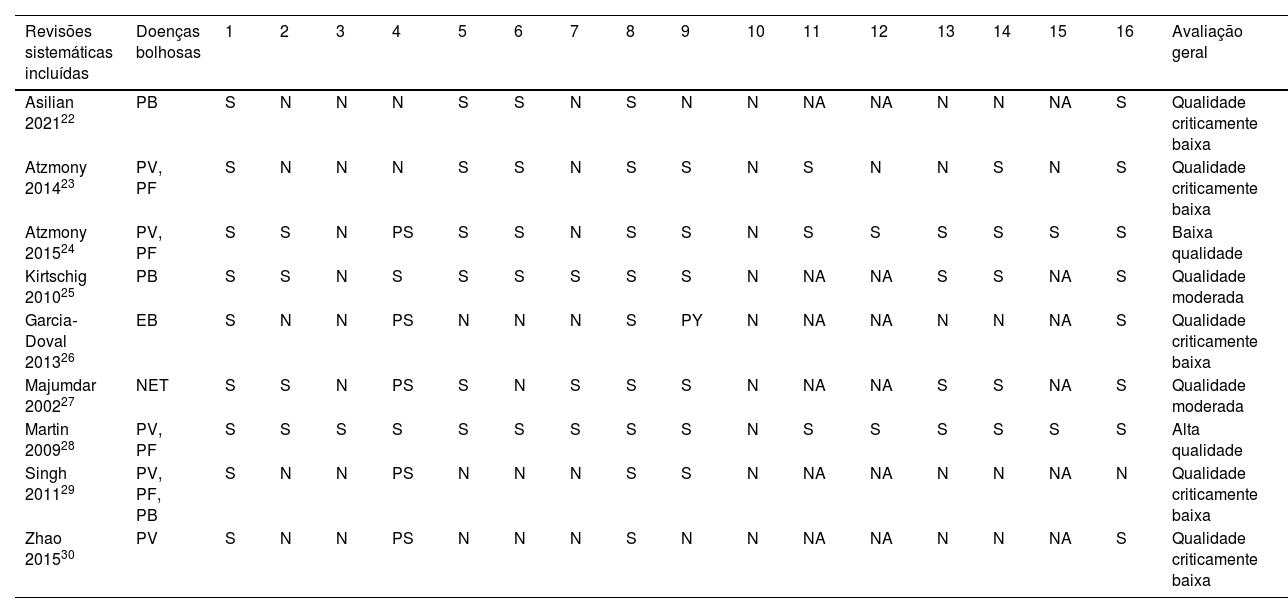
Avaliação da qualidade metodológicaA qualidade metodológica das revisões foi analisada por meio da ferramenta AMSTAR‐2. Na avaliação, 55,6% (5/9)22,23,26,29,30 das revisões foram classificadas como tendo qualidade criticamente baixa, 22,2% (2/9)25,27 como qualidade moderada, 11,1% (1/9)24 como baixa qualidade e 11,1% (1/9)28 como alta qualidade. A figura 2 descreve um resumo dos resultados separando a avaliação AMSTAR‐2 por itens.
As revisões sistemáticas classificadas como de qualidade criticamente baixa22,23,26,29,30 apresentaram resposta negativa em quase os mesmos itens. Nenhuma delas relatou registro do protocolo de revisão (item 2), explicação da seleção do desenho do estudo primário (item 3), lista de estudos excluídos com motivos (item 7) e fontes de financiamento de cada ECR incluído (item 10). Dessas revisões, 40% (2/5)22,23 não apresentaram estratégia de busca abrangente (item 4); 60% (3/5)26,29,30 não realizaram seleção dos estudos e extração de dados por dois autores independentes (itens 5 e 6); e 40% (2/5)22,30 não utilizaram técnica satisfatória para avaliação do RoB em ECRs individuais (item 9). O único estudo nessa classificação que realizou metanálise23 não avaliou o impacto do RoB de estudos individuais na metanálise (item 12) e não realizou investigação de viés de publicação (item 15). Quatro das cinco revisões22,23,29,30 (80%) não levaram em conta o RoB em estudos individuais ao interpretar/discutir os resultados da revisão (item 13), e três22,29,30 (60%) não relataram a investigação da heterogeneidade (item 14).
Na classificação de baixa qualidade, uma revisão sistemática24 recebeu sim parcial para estratégia de busca (item 4), não justificou os estudos primários excluídos (item 7) e não descreveu as fontes de financiamento dos estudos incluídos (item 10). As revisões de qualidade moderada25,27 não realizaram os itens 3 e 10, e uma não realizou extração de dados em duplicata (item 6). A revisão classificada como de alta qualidade28 falhou apenas no item 10.
Uma análise detalhada da avaliação da qualidade metodológica das revisões sistemáticas incluídas está disponível na tabela 3.
Avaliação da qualidade metodológica das revisões sistemáticas incluídas (AMSTAR‐2)
| Revisões sistemáticas incluídas | Doenças bolhosas | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | Avaliação geral |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Asilian 202122 | PB | S | N | N | N | S | S | N | S | N | N | NA | NA | N | N | NA | S | Qualidade criticamente baixa |
| Atzmony 201423 | PV, PF | S | N | N | N | S | S | N | S | S | N | S | N | N | S | N | S | Qualidade criticamente baixa |
| Atzmony 201524 | PV, PF | S | S | N | PS | S | S | N | S | S | N | S | S | S | S | S | S | Baixa qualidade |
| Kirtschig 201025 | PB | S | S | N | S | S | S | S | S | S | N | NA | NA | S | S | NA | S | Qualidade moderada |
| Garcia‐Doval 201326 | EB | S | N | N | PS | N | N | N | S | PY | N | NA | NA | N | N | NA | S | Qualidade criticamente baixa |
| Majumdar 200227 | NET | S | S | N | PS | S | N | S | S | S | N | NA | NA | S | S | NA | S | Qualidade moderada |
| Martin 200928 | PV, PF | S | S | S | S | S | S | S | S | S | N | S | S | S | S | S | S | Alta qualidade |
| Singh 201129 | PV, PF, PB | S | N | N | PS | N | N | N | S | S | N | NA | NA | N | N | NA | N | Qualidade criticamente baixa |
| Zhao 201530 | PV | S | N | N | PS | N | N | N | S | N | N | NA | NA | N | N | NA | S | Qualidade criticamente baixa |
S, sim; N, não; PS, parcialmente sim; NA, não aplicado (nenhuma metanálise realizada). (http://amstar.ca/Amstar_Checklist.ph); PB, penfigoide bolhoso; PV, pênfigo vulgar; PF, pênfigo foliáceo; EB, epidermólise bolhosa; NET, necrólise epidérmica tóxica.
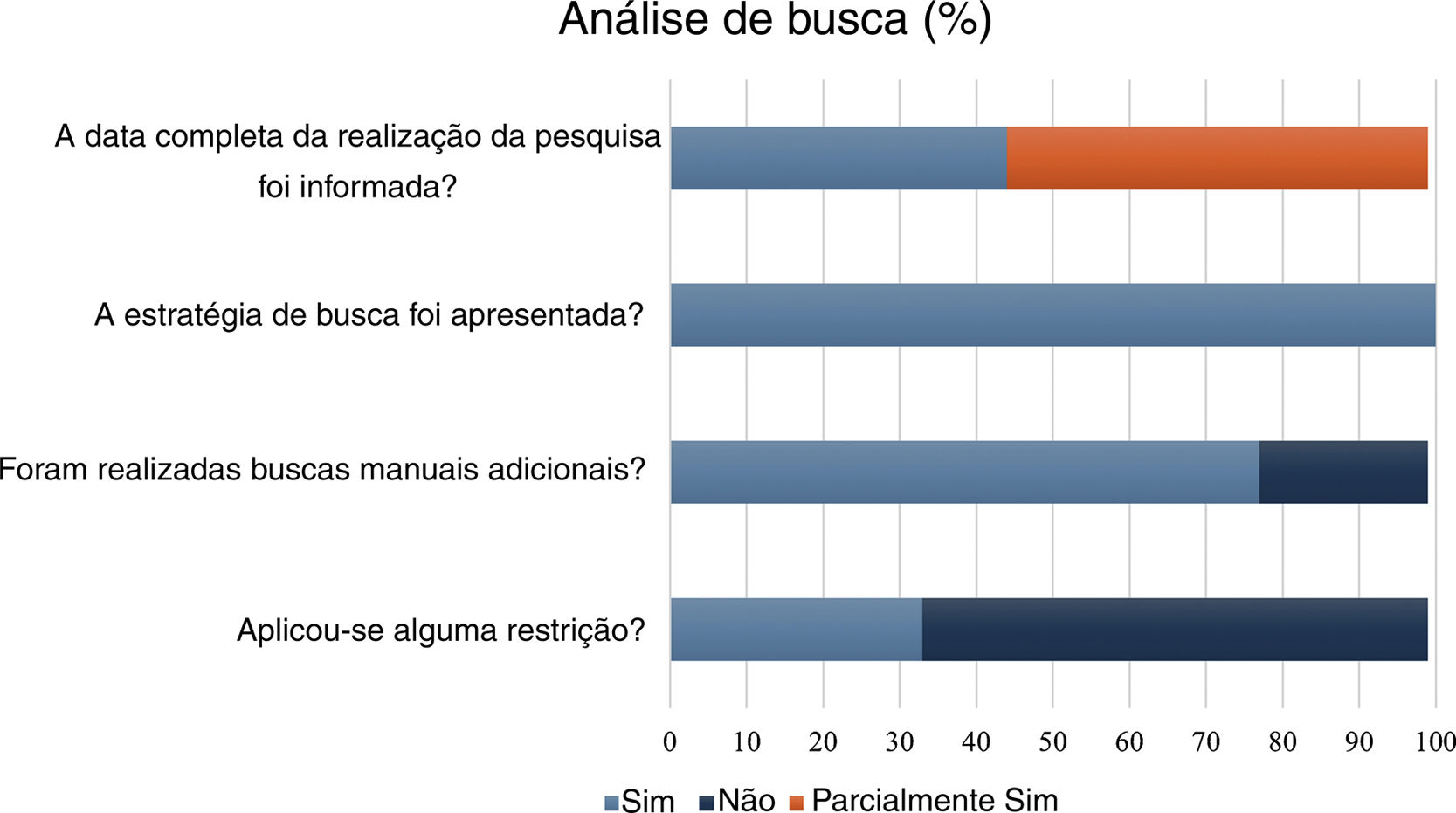
Para avaliar a adequação das estratégias de busca apresentadas pelas revisões sistemáticas incluídas, avaliamos os dados utilizando cinco questões não incluídas na ferramenta AMSTAR‐2. Ao verificar o relatório da data de busca, 44,4% (4/9) apresentaram data completa e 55,5% (5/9) parcialmente preenchida. Todos os estudos mostraram as estratégias de busca nas bases de dados e 77,7% (7/9) realizaram buscas manuais adicionais. Em 33,3% (3/9) dos estudos foram aplicadas restrições de idioma e/ou linguagem. As bases de dados mais acessadas foram Cochrane Central Register of Controlled Trials (77,7%), MEDLINE (via Pubmed; 66,6%), Embase (55,5%), plataformas de registro de ECRs (44,4%), LILACS (44,4%) e Cochrane Skin Group Specialised Register (33,3%; fig. 3).
Número de revisões sistemáticas que avaliaram a certeza das evidências (GRADE)Todas as quatro revisões22–24,29 nas quais a abordagem GRADE poderia ter sido aplicada para avaliar a certeza do conjunto de evidências (a partir da data de conclusão e data de publicação do GRADE) não o fizeram.
Número de revisões sistemáticas que identificam e relatam estudos pendentes de classificação e em andamentoUma revisão28 identificou e relatou estudos classificados como “aguardando classificação” em virtude da ausência de artigos de texto completo, e sete revisões23–28,30 relataram os ECRs em andamento identificados após pesquisa em plataformas de registro como ClinicalTrials.gov.
Sobreposição de ECRs nas revisões sistemáticas incluídasSete22–25,28–30 de nove incluíram revisões sistemáticas (80%) que avaliaram pênfigo e penfigoide, resultando em 40 ECRs incluídos sobre essa condição. Dessas, seis23–25,28–30 tiveram pelo menos dois ECRs sobrepostos, com 65% (26/40) do total de ECRs em pelo menos duas revisões. A revisão mais recente, publicada em 2021,22 incluiu apenas três ECRs publicados entre 2016 e 2017, enquanto as revisões publicadas entre 2009 e 2015 tiveram pelo menos nove ECRs publicados entre 1988 e 2015, não identificados pela primeira.
DiscussãoDado o crescente número de publicações envolvendo o tratamento das doenças vesicobolhosas, este estudo metaepidemiológico teve como objetivo analisar a qualidade metodológica das revisões sistemáticas publicadas sobre essa condição. Considerando apenas o alto nível de evidência, foram identificadas nove revisões sistemáticas de ECRs, avaliando diferentes intervenções para doenças cutâneas vesicobolhosas. Infelizmente, a maioria foi classificada como criticamente baixa e de baixa qualidade, de acordo com os critérios AMSTAR‐2. Além disso, algumas revisões não apresentaram componentes de estratégia de busca adequados e não avaliaram a certeza das evidências por meio da abordagem GRADE e não conseguiram identificar e relatar estudos com classificação pendente e em andamento, como recomendado pelo Cochrane Handbook of Systematic Reviews of Interventions.13 A sobreposição de ECRs também foi avaliada, simultaneamente mostrando repetições em pelo menos cinco revisões.
O uso de ferramenta como o AMSTAR‐2 permite aos leitores identificarem a qualidade metodológica das evidências derivadas de uma revisão sistemática de ensaios clínicos randomizados e não randomizados, impactando diretamente no uso pretendido desses resultados para a tomada de decisões clínicas. É essencial verificar o significado dos desvios cometidos pelos autores das revisões que foram categorizadas como de qualidade baixa ou criticamente baixa.11
As revisões sistemáticas estão sujeitas a vieses; entretanto, o uso de metodologia rigorosa possibilita aos pesquisadores acessar erros sistemáticos mínimos em seus resultados.13 Neste estudo metaepidemiológico, as revisões sistemáticas classificadas como de qualidade baixa ou criticamente baixa apresentaram fragilidades metodológicas, como nenhum relato publicado de protocolo de revisão de registros. A elaboração e publicação de um protocolo de revisão anterior reduzem a possibilidade de viés de relato, ou seja, quando um estudo se desvia dos componentes metodológicos do planejamento e apresenta apenas resultados selecionados que geralmente beneficiam a intervenção de interesse.31 A elaboração do protocolo protege os resultados, mesmo que sejam prejudiciais; quaisquer diferenças de protocolo justificadas no artigo publicado também contribuem para a confiabilidade dos resultados.
Nenhuma das revisões sistemáticas incluídas explicou a seleção dos desenhos de estudo para a revisão, critério importante quando há ensaios clínicos randomizados disponíveis sobre a questão pesquisada, mas há uma tendência de incluir aqueles não randomizados que podem apresentar resumos incompletos dos verdadeiros efeitos do tratamento.11 Além disso, nenhuma das revisões sistemáticas incluídas forneceu uma lista de estudos excluídos na segunda etapa de seleção com justificativas, criando o risco de que eles permaneçam invisíveis e o impacto de sua exclusão na revisão seja desconhecido. O financiamento individual dos ECRs incluídos nas revisões sistemáticas também não foi descrito em nenhuma revisão, podendo inferir viés quanto ao conflito de interesses financeiros.
A discussão e interpretação do impacto do RoB dos ECRs nos achados da revisão são essenciais para apoiar a tomada de decisão clínica, assim como a análise desses riscos ao agrupar estudos em metanálises. A heterogeneidade entre os ECRs incluídos também deve ser avaliada por meio da variação das questões clínicas (PICO) e de considerações metodológicas para obter estudos tão homogêneos quanto possível.11
Foi possível observar um intervalo de datas de publicação entre as revisões sistemáticas incluídas. A revisão mais recente foi publicada em 2021, classificada como de qualidade criticamente baixa e não incluiu todos os ECRs disponíveis com a questão PICO analisada, incluída em revisões mais antigas. Além disso, mais da metade dos ECRs incluídos sobre pênfigo são duplicados entre revisões sistemáticas. Esse fato reflete a necessidade de realizar revisões sistemáticas praticamente simultâneas, mas metodologicamente heterogêneas, que possam sobrestimar os efeitos da intervenção e confundir profissionais de saúde, legisladores e pacientes. Vale ressaltar que um dos papéis de uma revisão sistemática é evitar a duplicação de esforços, reunindo todos os estudos primários publicados sobre determinado assunto. Este estudo observou que a qualidade criticamente baixa de diversas revisões duplica esforços desnecessariamente e inviabiliza o uso dos achados para apoiar a prática clínica. No final, apesar das várias revisões identificadas e dos vários ECRs publicados, ainda é necessário rigor metodológico para esclarecer os melhores tratamentos para as doenças vesicobolhosas.
Além disso, análises adicionais sobre estratégias de busca e a avaliação da certeza das evidências utilizando a abordagem GRADE são critérios metodológicos que poderiam ser incorporados em uma versão atualizada da ferramenta AMSTAR‐2, dado o impacto substancial que essas etapas tiveram nos resultados derivados de uma revisão sistemática de intervenções.
O presente estudo tem a vantagem de realizar busca abrangente em bases de dados sem qualquer restrição de data ou idioma, tornando difícil não encontrar revisões sistemáticas publicadas que incluam a questão clínica, e uma metodologia rigorosa para selecionar e avaliar criticamente as revisões incluídas, além de empregar ferramenta validada utilizada no mundo todo para analisar a avaliação metodológica de revisões sistemáticas. Que seja de conhecimento dos autores, este é o primeiro estudo metaepidemiológico a avaliar a qualidade das revisões sistemáticas sobre o tratamento de doenças cutâneas vesicobolhosas.
Há escassez de revisões sistemáticas com ensaios clínicos randomizados em algumas dermatoses bolhosas como dermatite herpetiforme, epidermólise bolhosa, eritema multiforme, síndrome de Stevens‐Johnson, impetigo bolhoso, hidroa vaciniforme, e dermatose bolhosa por IgA linear. Isso se deve à baixa incidência dessas doenças, o que torna um desafio a concepção de ensaios clínicos randomizados, o desenho de estudo mais adequado para questões de tratamento. Portanto, não foram incluídas revisões sistemáticas que avaliaram outros desenhos de estudo.
Em relação às revisões incluídas, existem limitações relacionadas a falhas metodológicas e baixa qualidade das evidências. Além disso, a ferramenta AMSTAR‐2 apresenta algumas limitações relacionadas ao seu uso. A ferramenta foi criada em 2007 e atualizada em 2017, exigindo adaptação e mais tempo para aplicação,32 e uma descrição não tão detalhada da busca, necessitando de análises adicionais para avaliá‐la.
ConclusõesConsiderando a qualidade metodológica das revisões sistemáticas sobre tratamento de doenças vesicobolhosas, cinco (55,6%) avaliaram penfigoide bolhoso, epidermólise bolhosa, pênfigo vulgar e foliáceo, e foram classificadas como de qualidade criticamente baixa. Uma revisão (11,1%) avaliando pênfigo vulgar e foliáceo foi classificada como de alta qualidade; duas (22,2%) sobre necrólise epidérmica tóxica e penfigoide bolhoso como qualidade moderada; e uma revisão (11,1%) avaliando pênfigo vulgar e foliáceo foi classificada como de baixa qualidade. Além disso, 26 ensaios clínicos randomizados apresentaram sobreposição nas revisões incluídas, as estratégias de busca não foram relatadas na íntegra na maioria delas e a abordagem GRADE não foi utilizada para avaliar a certeza das evidências em nenhuma das revisões. Portanto, há urgência em melhorar a qualidade metodológica de futuras revisões sistemáticas de doenças vesicobolhosas a fim de evitar esforços desnecessários e aumentar a confiabilidade dessas evidências para apoiar a decisão clínica.
Suporte financeiroNenhum.
Contribuição dos autoresKamilla Mayr Martins Sá: Concepção e planejamento do estudo, levantamento de dados, elaboração e redação do artigo, obtenção, análise e interpretação dos dados, revisão crítica da literatura e aprovação da versão final do manuscrito.
Juliana Cavaleiro Rodrigues: Obtenção, análise e interpretação dos dados, revisão crítica da literatura, aprovação da versão final do manuscrito.
Lígia Borges da Silva: Obtenção, análise e interpretação dos dados, revisão crítica da literatura, aprovação da versão final do manuscrito.
Giovanna Marcılio Santos: Revisão crítica da literatura, revisão crítica de conteúdo intelectual importante, aprovação da versão final do manuscrito.
Mileny Esbravatti Stephano Colovati: Revisão crítica da literatura, revisão crítica de conteúdo intelectual importante, aprovação da versão final do manuscrito.
Ana Luiza Cabrera Martimbianco: Concepção e planejamento do estudo, participação efetiva na orientação da pesquisa, elaboração e redação do artigo e revisão crítica de conteúdo intelectual importante, obtenção, análise e interpretação dos dados, revisão crítica da literatura, aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: Sá KMM, Rodrigues JC, da Silva LB, Santos GM, Colovati MES, Martimbianco ALC. Quality of systematic reviews on the treatment of vesiculobullous skin diseases. A meta‐epidemiological study. An Bras Dermatol. 2024;99:223–32.
Trabalho realizado na Universidade Metropolitana de Santos, Santos, SP, Brasil.