Úlceras crônicas de membros inferiores (UCMI) são lesões que ocorrem abaixo do joelho com duração superior a seis semanas. As principais causas são: úlceras venosas (60%‐70%), arterial ou mista (10%‐25%) e neuropática. As UCMI afetam 1%‐7% da população com idade> 65 anos e representam importante problema de saúde pública.1
Nas UCMI, a dermatite de contato alérgica (DCA) acontece em torno de 50% dos pacientes, o que pode prejudicar a cicatrização.2 DCA ocorre por contato repetido com alérgenos de baixo peso molecular, quebra da barreira cutânea e, particularmente, pelo uso prolongado de terapêuticas tópicas para o tratamento das UCMI.3 O teste de contato está indicado em pacientes com eczema peri‐úlcera.
Os alérgenos mais prevalentes variam de acordo com a região geográfica, com práticas populares e características genéticas de cada população. Como há poucos estudos sobre o tema e, até agora, nenhum brasileiro, este estudo objetivou identificar a prevalência de positividade aos testes de contato e a reatividade a substâncias presentes nos principais curativos utilizados para pacientes com UCMI.
Realizou‐se estudo transversal com pacientes com UCMI atendidos no ambulatório de úlceras crônicas do Serviço de Dermatologia do Hospital das Clínicas da Faculdade de Medicina de Botucatu‐UNESP. O projeto foi aprovado pelo Comitê de Ética em Pesquisa local (CAAE 47938715.9.0000.5411) e os participantes selecionados assinaram o termo de consentimento livre e esclarecido. O critério de inclusão foi diagnóstico de UCMI independentemente da etiologia. Os critérios de exclusão foram: utilização de imunossupressores sistêmicos nos últimos 30 dias; presença de dermatoses que impossibilitavam a realização do teste de contato no dorso e gestação.
O teste de contato foi realizado com a bateria padronizada para a população brasileira (FDA Allergenic, Rio de Janeiro, Brasil), composta de 30 substâncias e fixados em contensores tipo Finn Chambers®. Também foi realizado com os 12 principais curativos e produtos tópicos utilizados para UCMI e pele peri‐úlcera: óleo de ácidos graxos essenciais, sulfadiazina de prata, colagenase com cloranfenicol, mupirocina, hidrogéis, hidrocoloides, faixa elástica compressiva, bota de Unna, hidrofibra com prata, carvão ativado com prata, alginato de cálcio e micropore. As leituras foram realizadas em 48 horas e 72 horas.
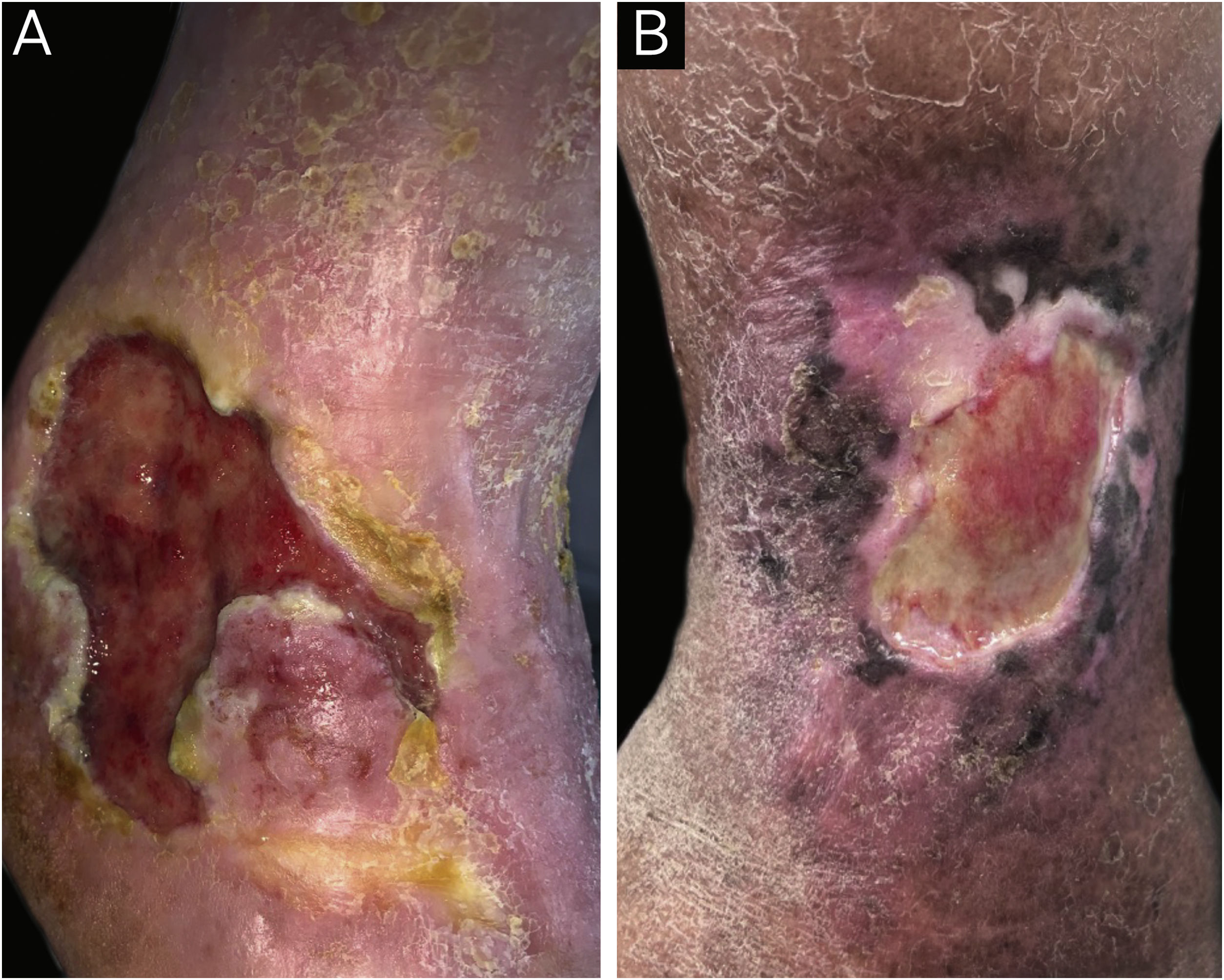
Foram incluídos 78 participantes com UCMI, predominou o gênero feminino (47/78 ‐ 60,9%) e idade média (desvio‐padrão) de 68,4 (12,5) anos. A etiologia das úlceras foi venosa em 67/78 (85,9%), mista (venosa e arterial) em 9/78 (11,5%) e arterial em um participante (1,3%). A mediana (p25‐p75) de duração das úlceras foi de 24 (10‐120) meses. Eczema peri‐úlcera estava presente em 56/78 participantes (71,8%; fig. 1). Houve antecedente pessoal de eczema peri‐úlcera em 27/78 (34,5%) participantes; 17/78 (21,8%) tinham história de eczema em outros locais além da região peri‐úlcera e 11/78 (14,1%) tinham antecedente de atopia. Na tabela 1 estão os principais produtos e curativos que foram relatados como já utilizados na úlcera e região peri‐úlcera.
(A) Paciente com úlcera venosa com eczema peri‐úlcera caracterizado por prurido, eritema e descamação. Ao teste de contato, apresentou na leitura de 72 horas, teste positivo com relevância para lanolina, mistura de parabenos, hidrogel, sulfadiazina de prata, faixa elástica, bota de Unna, colagenase com cloranfenicol e hidrofibra com prata. (B) Paciente com úlcera venosa com eczema peri‐úlcera. Ao teste de contato não apresentou teste positivo na bateria padrão, entretanto ao teste de contato com curativos, apresentou na leitura de 72 horas, teste positivo para hidrogel e colagenase com cloranfenicol.
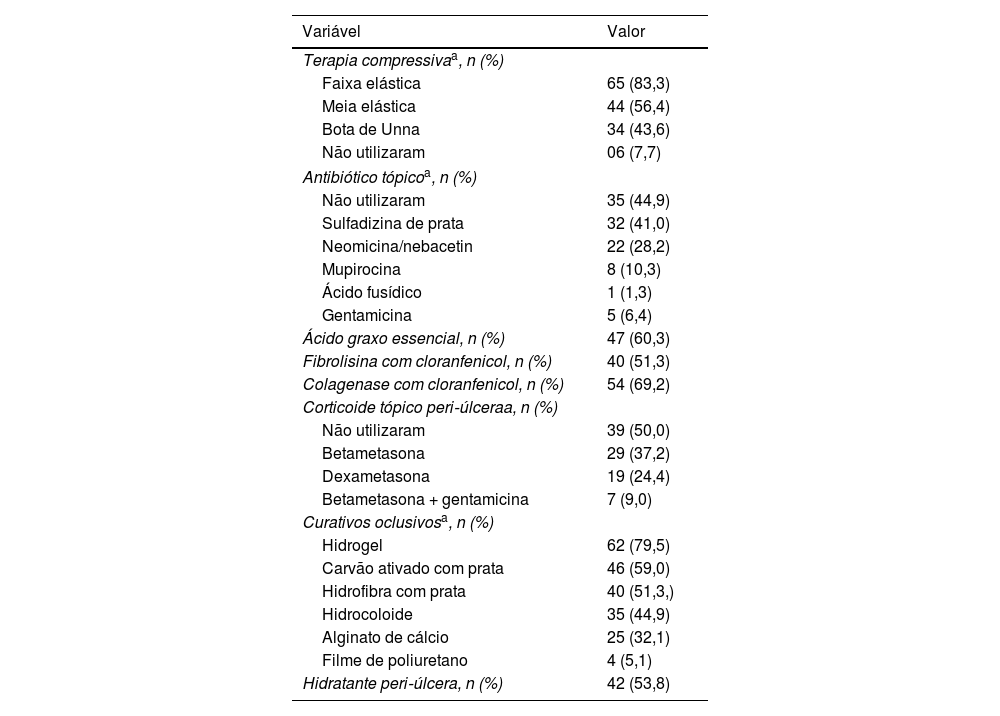
Terapia compressiva, curativos e produtos que foram relatados como já utilizados pelos 78 participantes na região da úlcera e peri‐úlcera
| Variável | Valor |
|---|---|
| Terapia compressivaa, n (%) | |
| Faixa elástica | 65 (83,3) |
| Meia elástica | 44 (56,4) |
| Bota de Unna | 34 (43,6) |
| Não utilizaram | 06 (7,7) |
| Antibiótico tópicoa, n (%) | |
| Não utilizaram | 35 (44,9) |
| Sulfadizina de prata | 32 (41,0) |
| Neomicina/nebacetin | 22 (28,2) |
| Mupirocina | 8 (10,3) |
| Ácido fusídico | 1 (1,3) |
| Gentamicina | 5 (6,4) |
| Ácido graxo essencial, n (%) | 47 (60,3) |
| Fibrolisina com cloranfenicol, n (%) | 40 (51,3) |
| Colagenase com cloranfenicol, n (%) | 54 (69,2) |
| Corticoide tópico peri‐úlceraa, n (%) | |
| Não utilizaram | 39 (50,0) |
| Betametasona | 29 (37,2) |
| Dexametasona | 19 (24,4) |
| Betametasona + gentamicina | 7 (9,0) |
| Curativos oclusivosa, n (%) | |
| Hidrogel | 62 (79,5) |
| Carvão ativado com prata | 46 (59,0) |
| Hidrofibra com prata | 40 (51,3,) |
| Hidrocoloide | 35 (44,9) |
| Alginato de cálcio | 25 (32,1) |
| Filme de poliuretano | 4 (5,1) |
| Hidratante peri‐úlcera, n (%) | 42 (53,8) |
O teste de contato com a bateria padrão (tabela 2) foi positivo em 72 horas em 31/78 (39,7%, 95% IC 30%‐49%) participantes. Os principais alérgenos foram: mistura de parabenos (9/78 ‐ 11,5%), sulfato de níquel (5/78 ‐ 6,4%) e lanolina (3/78 – 3,8%). Algumas substâncias que foram positivas não são relevantes aos pacientes com eczema peri‐úlcera, pois não são relacionadas aos curativos e produtos usualmente utilizados por esses pacientes.
Resultado do teste de contato positivo (+ a +++) com a bateria padrão após 72 horas e sua relevância em relação ao eczema peri‐úlcera, em 78 participantes
| Substância | Teste positivo na leitura de 72ha, n (%) | Relevância em relação ao eczema peri‐úlcera |
|---|---|---|
| Mistura de parabenos | 9 (11,5) | Sim |
| Sulfato de níquel | 5 (6,4) | Sim |
| Lanolina | 3 (3,8) | Sim |
| Bálsamo do Peru | 2 (2,6) | Não |
| Kathon CG | 2 (2,6) | Sim |
| Thimerosal | 2 (2,6) | Sim |
| Colofônio | 2 (2,6) | Sim |
| Formaldeído | 2 (2,6) | Não |
| Propilenoglicol | 1 (1,3) | Sim |
| Cloreto de cobalto | 1 (1,3) | Sim |
| Tiuram (MIX) | 1 (1,3) | Não |
| Etilenodiamina | 1 (1,3) | Não |
| Quinolina | 1 (1,3) | Não |
As seguintes substâncias da bateria padrão não tiveram positividade em nenhum paciente em 72 horas: bicromato de postássio, neomicina, perfume mix, quartenium 15, nitrofurazona, terebentina, carba mix, parafenilenodiamina, antraquinona, PPD, hidroquinona, butilfenol para terciário, igarsan, mercapto mix, resina epóxi, benzocaína e prometazina.
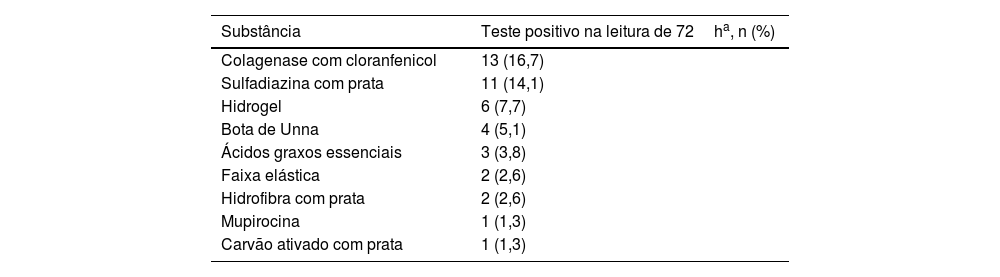
Na testagem com as substâncias dos curativos (tabela 3), 22/78 (28,2%; 95% IC 18%‐37%) participantes apresentaram reatividade a esses componentes em 72 horas. Os principais alérgenos foram: colagenase com cloranfenicol (13/78 ‐ 16,7%), sulfadiazina de prata (11/78 – 14,1%) e hidrogel (6/78 – 7,7%). Outro aspecto relevante foi que 5/78 (6,4%) participantes apresentaram reação ao micropore, porém com leitura positiva apenas nas primeiras 48 horas, negativando‐se na leitura de 72 horas, demonstrando reação irritativa e não DCA.
Resultado do teste de contato positivo em 72 horas (+ a +++) referente aos produtos e curativos utilizados em 78 participantes
| Substância | Teste positivo na leitura de 72ha, n (%) |
|---|---|
| Colagenase com cloranfenicol | 13 (16,7) |
| Sulfadiazina com prata | 11 (14,1) |
| Hidrogel | 6 (7,7) |
| Bota de Unna | 4 (5,1) |
| Ácidos graxos essenciais | 3 (3,8) |
| Faixa elástica | 2 (2,6) |
| Hidrofibra com prata | 2 (2,6) |
| Mupirocina | 1 (1,3) |
| Carvão ativado com prata | 1 (1,3) |
Quando analisamos os resultados do teste de contato para a bateria padrão e para os curativos, concomitantemente, 39/78 (50%; 95% IC 39%‐59%) dos participantes reagiram para alguma das substâncias testadas; 14/78 (17,9%; 95% IC 10%‐24%) participantes reagiram tanto na bateria padrão quanto para curativos (fig. 1A).
Evidenciou‐se alta porcentagem de testes de contato alérgicos positivos concordante com a literatura recente,3 entretanto, menor positividade que os estudos mais antigos que variavam entre 75% e 80%, levando à hipótese que substâncias sabidamente mais alergênicas têm sido evitadas na composição de curativos e produtos para tratamento de úlceras.4,5
As substâncias do teste de contato padrão que mais foram reativas no nosso estudo foram: mistura de parabenos, sulfato de níquel e lanolina. Outros alérgenos que tiveram reação em poucos participantes deste estudo, mas apresentaram grande significância em outras amostras foram: neomicina, perfume mix, carbamix, benzocaína e hidroquinona.5
Mistura de parabenos é um conservante utilizado na indústria cosmética, farmacêutica e alimentícia. É descrito que os pacientes com UCMI podem reagir aos parabenos utilizados nos cosméticos aplicados na pele peri‐úlcera, mas tolerá‐los em pele saudável.6 Em relação à lanolina, a qual é utilizada em dermocosméticos como cremes e xampus, nosso estudo apresentou positividade semelhante as relatadas em outros estudos. Já quanto ao sulfato de níquel, os estudos mostraram baixa positividade, apesar de ter sido alta no presente estudo (12,8%). Na população geral com suspeita de DCA, sua prevalência é cerca de 36%.7
Quanto aos testes com os curativos, nosso estudo identificou 28,2% com pelo menos um teste positivo, resultado semelhante ao de outras séries,3,5 o que demonstra a importância de se realizar teste de contato com as substâncias específicas dos curativos, além da bateria padrão.
Os curativos mais reativos nesta amostra foram: colagenase com cloranfenicol, sulfadiazina de prata e hidrogel. A colagenase contém enzima proteolítica capaz de digerir o colágeno, sendo muito utilizada para o desbridamento de úlceras. Entretanto, é difícil diferenciar se a reatividade é decorrente da clostridiopeptidase A ou do cloranfenicol.8 Os hidrogéis e hidrocoloides são citados como alergênicos, com positividade em outros estudos até 23% dos pacientes testados para hidrogel e 52% dos testados para o hidrocoloide.3,9 A sensibilização aos hidrogéis parece estar relacionada ao propilenoglicol, e a sensibilização aos hidrocoloides pode ser decorrente da carboximetilcelulose e de derivados de colofônio.10
As limitações do nosso estudo foram principalmente a inclusão majoritária de úlceras venosas, com pouca representatividade de outras causas de UCMI. Não testamos todos os produtos e curativos existentes no mercado nacional, e sim os principais produtos utilizados no tratamento de UCMI, assim como a colagenase não foi testada isoladamente. Também não realizamos testes de controle com os curativos, e como eram de determinadas marcas comerciais, houve dificuldade de identificar o real alérgeno.
Em conclusão, houve alta positividade ao teste de contato nos pacientes com UCMI, com destaque para a mistura de parabenos, sulfato de níquel, lanolina, colagenase com cloranfenicol, sulfadiazina de prata e hidrogel. Esses resultados destacam a relevância de se realizar testes de contato com bateria padrão e com os curativos/produtos usualmente utilizados nos pacientes que apresentam eczema peri‐úlcera.
Suporte financeiroNenhum.
Contribuição dos autoresÍsis Fiorello de Oliveira Mesquita: Concepção e planejamento do estudo; coleta de dados, análise e interpretação dos dados; redação do artigo; revisão crítica de literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Larissa Pierri Carvalho Fonseca: Concepção e planejamento do estudo; coleta de dados, análise e interpretação dos dados redação do artigo; revisão crítica de literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Maria Rita Parise Fortes: Coleta de dados; análise e interpretação dos dados; redação do artigo; revisão crítica de literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Hélio Amante Miot: Análise e interpretação dos dados; análise estatística; redação do artigo; revisão crítica de literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Luciana Patricia Fernandes Abbade: Concepção e planejamento do estudo; análise e interpretação dos dados; redação do artigo; revisão crítica de literatura; revisão crítica do manuscrito; aprovação da versão final do manuscrito.
Conflito de interessesNenhum.
Como citar este artigo: de Oliveira Mesquita ÍF, Carvalho Fonseca LP, Parise Fortes MR, Miot HA, Abbade LP. Prevalence of positivity in patch tests and reactivity to substances present in the main dressings in patients with chronic leg ulcers. An Bras Dermatol. 2025;100:162–5.
Trabalho realizado no Departamento de Infectologia, Dermatologia, Diagnóstico por Imagem e Radioterapia, Faculdade de Medicina, Universidade Estadual Paulista, Botucatu, SP, Brasil.